Clear Sky Science · ru
Продвинутые in vitro кардиальные модели для оценки лекарств: интеграция органоидов, инженерных тканей и микрофизиологических систем
Почему важно выращивать мини‑сердца
Сердечные заболевания — ведущая причина смерти в мире, и многие перспективные лекарства терпят неудачу на поздних стадиях разработки, потому что современные лабораторные тесты и исследования на животных часто не выявляют вредных эффектов для человеческого сердца. В этой статье объясняется, как учёные создают всё более реалистичные «мини‑сердца» в лаборатории — от плоских слоёв клеток до крошечных бьющихся тканей, органоидов и систем «сердце‑на‑чипе» — чтобы надежнее и безопаснее предсказывать, как человеческое сердце отреагирует на новые препараты.
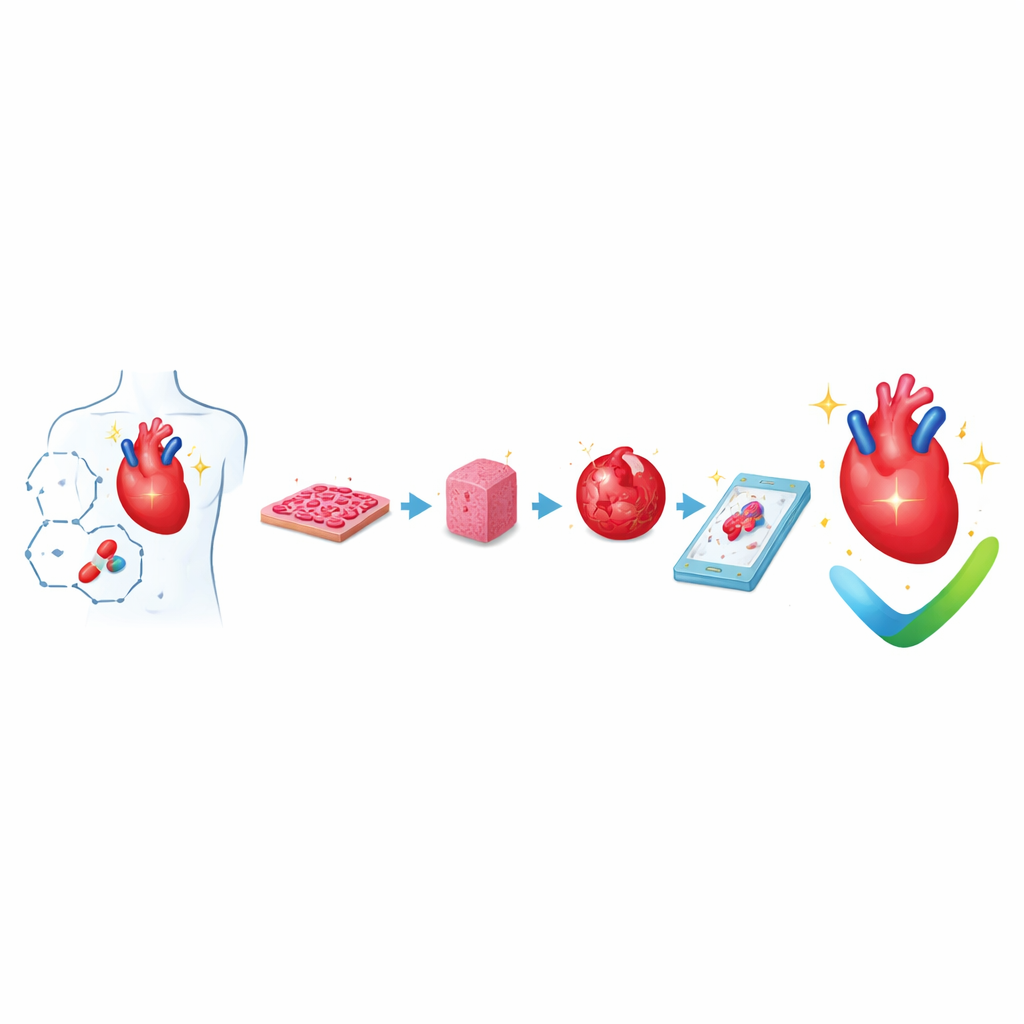
От простых слоёв клеток до крошечных бьющихся тканей
Исследователи теперь регулярно получают клетки сердечной мышцы человека из перепрограммированных взрослых клеток, так называемых индуцированных плюрипотентных стволовых клеток. Эти клетки можно распространять тонкими пластами или направлять в определённые формы с помощью микроскопических шаблонов. Даже на этом базовом уровне управление формой клеток, их выравниванием и жёсткостью поверхности меняет силу сокращений и скорость распространения электрических сигналов между ними. Такие плоские культуры легко выращивать в больших масштабах и измерять с помощью автоматизированных камер и сенсоров, поэтому их широко используют для первичного отбора по безопасности, в особенности для обнаружения препаратов, способных нарушать ритм сердца.
Создание трёхмерной сердечной мышцы и полостей
Чтобы ближе имитировать настоящие сердце, учёные собирают трёхмерные сердечные ткани, смешивая сердечные клетки с гелеобразными материалами, напоминающими природный матрикс сердца. Эти инженерные сердечные ткани часто формуют вокруг опорных стержней или колец, чтобы можно было измерять их крошечные сокращения по тому, как они тянут за опоры. При регулярной механической растяжке и электрической стимуляции ткани постепенно развивают структуру и насосную функцию, более похожие на взрослое сердце. Более крупные пласты и конструкции в форме камер могут даже имитировать наполнение и выброс желудочка, позволяя измерять изменения давление‑объём, аналогичные клиническим измерениям. Добавление клеток сосудов и вспомогательных клеток помогает этим тканям дольше выживать и лучше интегрироваться при трансплантации в сердца животных.
Самосборные мини‑сердца и раннее развитие
Другой подход сосредоточен на органоидах — саморганизующихся скоплениях клеток, напоминающих ранние стадии развития сердца. Начиная со стволовых клеток, исследователи регулируют во времени и по интенсивности сигналы роста так, чтобы клетки спонтанно сортировались в слои и формировали полые, бьющиеся структуры с ранними участками, похожими на камеры, внешними покровными клетками и примитивными сосудами. Некоторые органоиды даже формируют кроветворные и печенеподобные ткани рядом с сердечными областями, давая представление о том, как разные органы развиваются совместно. Эти модели особенно ценны для изучения врождённых пороков, наследственных заболеваний сердца и того, как различные типы клеток в сердце взаимодействуют в процессе развития.
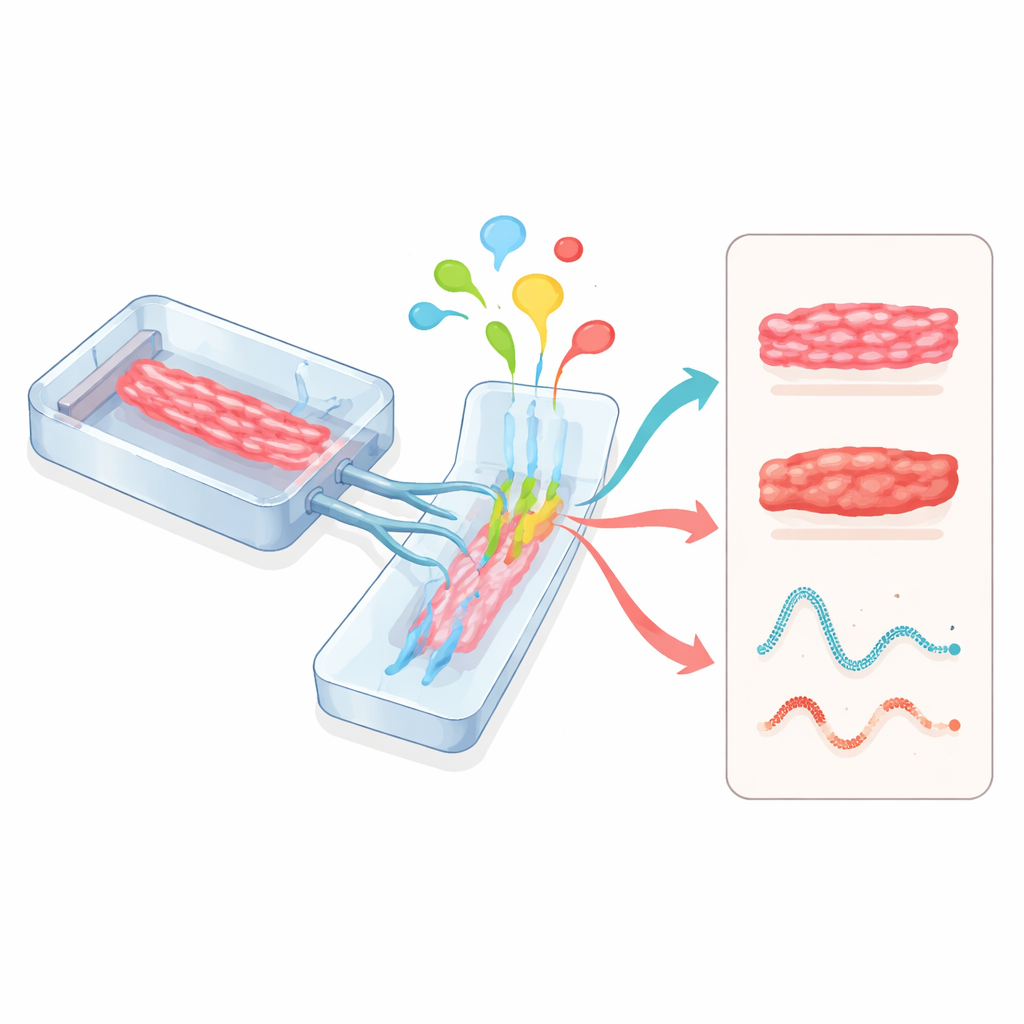
Сердца‑на‑чипе и межорганные соединения
Микрофизиологические системы, часто называемые органами‑на‑чипе, используют ещё один подход. Сердечные ткани выращивают внутри небольших прозрачных устройств с выгравированными каналами для потока жидкости и гибкими стенками, которые можно растягивать. Такие чипы точно контролируют питание, кислород, механическое напряжение и электрическую стимуляцию, пока сенсоры в реальном времени отслеживают силу сокращений и электрическую активность. Когда сердечные модули соединяют с печёночными, сосудистыми или другими органными модулями в одной цепи, учёные могут увидеть, как метаболиты печени влияют на сердце или как воспаление и иммунные клетки модифицируют функцию сердца. Регуляторы, такие как Управление по контролю за продуктами и лекарствами США (FDA), начинают признавать эти основанные на человеке чипы как перспективный инструмент для оценки безопасности лекарств.
Что это значит для будущих лекарств и терапий
Вместе плоские слои клеток, инженерные ткани, органоиды и органы‑на‑чипе образуют набор инструментов, который делает тестирование на сердце намного ближе к человеческой реальности, чем традиционные модели на животных. Каждая модель по‑своему балансирует реализм и практичность, а их комбинирование даёт более полное представление о том, как препарат может помочь или навредить человеческому сердцу. Хотя остаются вызовы — например, полноценное созревание этих мини‑сердец, обеспечение реалистичного кровотока и стандартизация методов между лабораториями — эти достижения закладывают основу для более безопасных лекарств, более персонализированных терапий и в конечном итоге лабораторно выращенных сердечных тканей, которые смогут помочь в восстановлении повреждённых сердец.
Цитирование: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
Ключевые слова: heart-on-a-chip, кардиальные органоиды, инженерная сердечная ткань, кардиотоксичность лекарств, кардиомиоциты от hiPSC