Clear Sky Science · nl
Geavanceerde in vitro cardiale modellen voor geneesmiddelbeoordeling: integratie van organoïden, geconstrueerde weefsels en microfysiologische systemen
Waarom het kweken van mini-harten ertoe doet
Hartziekten zijn de belangrijkste doodsoorzaak wereldwijd, maar veel veelbelovende medicijnen vallen laat in de ontwikkelingsfase af omdat de huidige laboratoriumtests en dierstudies vaak schadelijke effecten op het menselijk hart missen. Dit artikel legt uit hoe wetenschappers steeds realistischer wordende "mini-harten" in het laboratorium bouwen — van platte celmonolagen tot kleine kloppende weefsels, organoïden en heart-on-a-chip-systemen — om veiliger en nauwkeuriger te voorspellen hoe onze harten op nieuwe medicijnen reageren.
Van eenvoudige cellagen naar kleine kloppende weefsels
Onderzoekers kweken tegenwoordig routinematig menselijke hartspiercellen uit gereprogrammeerde volwassen cellen, zogenaamde geïnduceerde pluripotente stamcellen. Deze cellen kunnen als dunne vellen worden verdeeld of met microscopische patronen in specifieke vormen worden geleid. Zelfs op dit basale niveau verandert het beheersen van celvorm, uitlijning en de zachtheid van het oppervlak hoe krachtig de cellen kloppen en hoe elektrische signalen ertussen reizen. Deze platte culturen zijn gemakkelijk in grote aantallen te kweken en te meten met geautomatiseerde camera’s en sensoren, waardoor ze veel worden gebruikt voor de eerste veiligheidscontroles, vooral om geneesmiddelen te detecteren die het hartritme kunnen verstoren.
Het bouwen van driedimensionaal hartweefsel en kamers
Om een echt hart beter na te bootsen, assembleren wetenschappers driedimensionale hartweefsels door hartcellen te mengen met gelachtige materialen die lijken op het natuurlijke raamwerk van het hart. Deze geengineerde hartweefsels worden vaak gegoten rond pilaren of ringen zodat hun kleine contracties kunnen worden gemeten terwijl ze aan de steunen trekken. Door regelmatige rekking en elektrische pulsen toe te passen, ontwikkelen de weefsels geleidelijk een meer volwassen structuur en pompgedrag. Grotere pleisters en constructies in kamer-vorm kunnen zelfs nabootsen hoe een ventrikel zich vult en vloeistof uitwerpt, waardoor druk–volume veranderingen kunnen worden gemeten die vergelijkbaar zijn met klinische metingen. Het toevoegen van bloedvatcellen en ondersteunende cellen helpt deze weefsels langer te overleven en beter te integreren wanneer ze in dierlijke harten worden getransplanteerd.
Zelfsamengestelde mini-harten en vroege ontwikkeling
Een andere onderzoekslijn richt zich op organoïden — zelforganiserende clusters van cellen die lijken op vroege stadia van een zich ontwikkelend hart. Beginnend vanaf stamcellen stemmen onderzoekers de timing en sterkte van groeisignalen zo af dat de cellen spontaan in lagen sorteren en holle, kloppende structuren vormen met vroege kamerachtige regio’s, buitenste bedekkingscellen en primitieve bloedvaten. Sommige organoïden genereren zelfs bloedvormende en leverachtige weefsels naast de hartregio’s, wat een inkijk biedt in hoe verschillende organen zich samen ontwikkelen. Deze modellen zijn bijzonder krachtig om aangeboren afwijkingen, erfelijke hartaandoeningen en hoe verschillende celtypen in het hart tijdens de ontwikkeling met elkaar communiceren te bestuderen.
Hearts-on-chips en multi-orgaanverbindingen
Microfysiologische systemen, vaak organs-on-chips genoemd, volgen weer een andere benadering. Hartweefsels worden gekweekt in kleine, transparante apparaten met geëtste kanalen voor vloeistofstroom en flexibele wanden die kunnen worden gerekt. Deze chips kunnen voedingsstoffen, zuurstof, mechanische spanning en elektrische stimulatie nauwkeurig regelen terwijl sensoren in realtime de kloppende kracht en elektrische activiteit volgen. Wanneer hartmodules worden gekoppeld aan lever-, bloedvat- of andere organenmodules op hetzelfde circuit, kunnen wetenschappers zien hoe door de lever verwerkte geneesmiddelen het hart beïnvloeden, of hoe ontsteking en immuuncellen de hartfunctie veranderen. Regelgevende instanties zoals de Amerikaanse Food and Drug Administration beginnen deze op menselijke cellen gebaseerde chips te erkennen als veelbelovende instrumenten voor de beoordeling van geneesmiddelveiligheid.
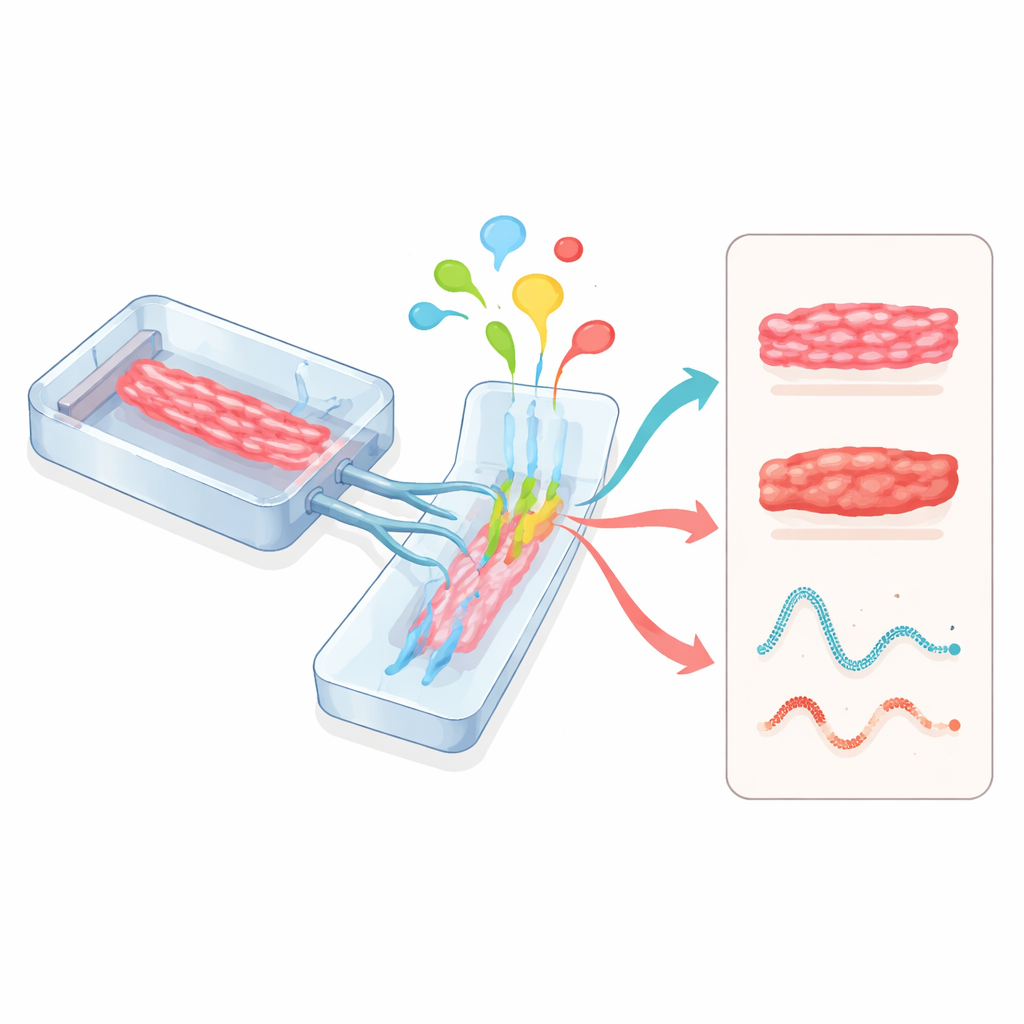
Wat dit betekent voor toekomstige medicijnen en therapieën
Samen vormen platte cellagen, geengineerde weefsels, organoïden en organs-on-chips een gereedschapskist die harttesten veel dichter bij de menselijke realiteit brengt dan traditionele diermodellen alleen. Elk model balanceert realisme en praktische toepasbaarheid op een eigen manier, en het combineren van deze modellen biedt een completer beeld van hoe een geneesmiddel het menselijk hart kan helpen of schaden. Hoewel er uitdagingen blijven — zoals het volledig rijpen van deze mini-harten, het voorzien van realistische bloedstroom en het standaardiseren van methoden tussen laboratoria — leggen deze vooruitgangen de basis voor veiligere medicijnen, meer gepersonaliseerde behandelingen en uiteindelijk laboratoriumgekweekte hartweefsels die beschadigde harten kunnen helpen repareren.
Bronvermelding: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
Trefwoorden: heart-on-a-chip, cardiale organoïden, geengineerd hartweefsel, geneesmiddel-cardiotoxiciteit, hiPSC cardiomyocyten