Clear Sky Science · fr
Modèles cardiaques in vitro avancés pour l’évaluation des médicaments : intégration d’organoïdes, de tissus ingénierés et de systèmes microphysiologiques
Pourquoi faire pousser des mini-cœurs est important
Les maladies cardiaques sont la première cause de mortalité dans le monde, et pourtant de nombreux médicaments prometteurs échouent tard dans le développement parce que les tests de laboratoire et les études animales actuels passent souvent à côté d’effets nocifs sur le cœur humain. Cet article explique comment les scientifiques construisent des « mini-cœurs » de plus en plus réalistes en laboratoire — des couches cellulaires plates aux petits tissus battants, en passant par les organoïdes et les systèmes heart-on-a-chip — afin de mieux prédire la réponse de nos cœurs aux nouveaux médicaments, de manière plus sûre et plus précise.
Des couches cellulaires simples aux petits tissus battants
Les chercheurs cultivent désormais de routine des cellules du muscle cardiaque humain à partir de cellules adultes reprogrammées, appelées cellules souches pluripotentes induites. Ces cellules peuvent être étalées en nappes fines ou guidées dans des formes spécifiques à l’aide de motifs microscopiques. Même à ce stade élémentaire, le contrôle de la forme cellulaire, de l’alignement et de la souplesse du support modifie la force des contractions et la façon dont les signaux électriques se propagent entre les cellules. Ces cultures plates sont faciles à produire en grand nombre et à mesurer avec des caméras et des capteurs automatisés, elles sont donc largement utilisées pour un premier criblage de sécurité, notamment pour détecter les médicaments susceptibles de perturber le rythme cardiaque.
Construire du muscle cardiaque tridimensionnel et des cavités
Pour mieux imiter un cœur réel, les scientifiques assemblent des tissus cardiaques tridimensionnels en mélangeant des cellules cardiaques avec des matériaux gélifiés qui ressemblent à l’échafaudage naturel du cœur. Ces tissus cardiaques ingénierés sont souvent coulés autour de poteaux ou d’anneaux afin que leurs minuscules contractions puissent être mesurées lorsqu’ils tirent sur les supports. En appliquant des étirements réguliers et des impulsions électriques, les tissus développent progressivement une structure et un comportement de pompage plus proches de l’état adulte. Des patchs plus grands et des structures en forme de cavité peuvent même imiter la façon dont un ventricule se remplit et éjecte du fluide, permettant de mesurer des variations pression‑volume similaires à celles utilisées en clinique. L’ajout de cellules vasculaires et de cellules de soutien aide ces tissus à survivre plus longtemps et à mieux s’intégrer lorsqu’ils sont transplantés dans des cœurs d’animaux.
Mini-cœurs auto-assemblés et développement précoce
Une autre voie de recherche se concentre sur les organoïdes — des amas cellulaires auto-organisés qui ressemblent aux premiers stades du développement cardiaque. À partir de cellules souches, les chercheurs ajustent le calendrier et l’intensité des signaux de croissance pour que les cellules se trient spontanément en couches et forment des structures creuses et battantes avec des régions précoces semblables à des cavités, des cellules couvrantes externes et de primitifs vaisseaux sanguins. Certains organoïdes produisent même des tissus hématopoïétiques et des tissus de type hépatique aux côtés des régions cardiaques, offrant une fenêtre sur la co-développement des différents organes. Ces modèles sont particulièrement puissants pour étudier les malformations congénitales, les maladies cardiaques héréditaires et la communication entre types cellulaires pendant le développement.
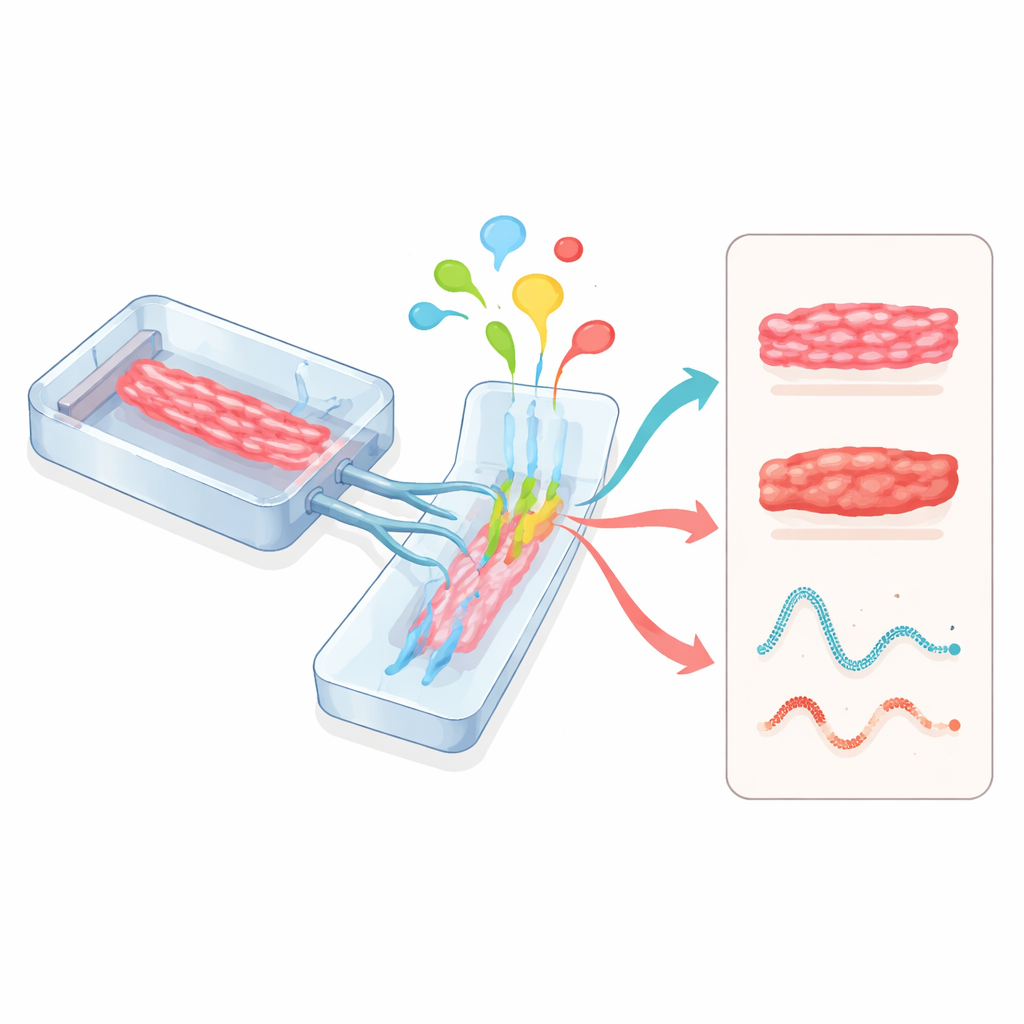
Heart-on-chips et connexions multi-organes
Les systèmes microphysiologiques, souvent appelés organs-on-chips, adoptent une approche différente. Des tissus cardiaques sont cultivés à l’intérieur de petits dispositifs transparents gravés de canaux pour le flux de fluide et de parois flexibles pouvant être étirées. Ces puces permettent de contrôler précisément les nutriments, l’oxygène, la contrainte mécanique et la stimulation électrique tandis que des capteurs suivent en temps réel la force des contractions et l’activité électrique. Lorsque des modules cardiaques sont reliés à des modules de foie, de vaisseaux sanguins ou d’autres organes sur le même circuit, les chercheurs peuvent observer comment des médicaments métabolisés par le foie affectent le cœur, ou comment l’inflammation et les cellules immunitaires influent sur la fonction cardiaque. Des autorités de régulation comme la Food and Drug Administration des États-Unis commencent à reconnaître ces puces humaines comme des outils prometteurs pour l’évaluation de la sécurité des médicaments.
Ce que cela signifie pour les futurs médicaments et thérapies
Ensemble, les couches cellulaires plates, les tissus ingénierés, les organoïdes et les organs-on-chips constituent une boîte à outils qui rapproche fortement les tests cardiaques de la réalité humaine par rapport aux modèles animaux traditionnels. Chaque modèle équilibre réalisme et praticité de façon différente, et leur combinaison offre une vision plus complète de la manière dont un médicament pourrait aider ou nuire au cœur humain. Bien que des défis subsistent — comme la maturation complète de ces mini-cœurs, la fourniture d’un flux sanguin réaliste et la standardisation des méthodes entre laboratoires — ces avancées posent les bases de médicaments plus sûrs, de traitements plus personnalisés et, à terme, de tissus cardiaques cultivés en laboratoire susceptibles d’aider à réparer des cœurs endommagés.
Citation: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
Mots-clés: heart-on-a-chip, organoïdes cardiaques, tissu cardiaque ingénieré, cardiotoxicité des médicaments, cardiomyocytes hiPSC