Clear Sky Science · he
מודלים מתקדמים של לב במבחנה להערכת תרופות: שילוב של אורגאנואידים, רקמות מהונדסות ומערכות מיקרופיזיולוגיות
מדוע חשיבות גידול לבבות מיניאטוריים
מחלת הלב היא הגורם המוביל למוות בעולם, ועדיין תרופות מבטיחות רבות נכשלות בשלב מאוחר של הפיתוח כי בדיקות מעבדה וניסויים בבעלי חיים כיום לעיתים מפספסים השפעות מזיקות על הלב האנושי. מאמר זה מסביר כיצד מדענים בונים "לבבות מיניאטוריים" במעבדה — משכבות תאים שטוחות ועד לרקמות פעימות זעירות, אורגנואידים ומערכות לב-על-צ׳יפ — כדי לחזות כיצד לבבותינו יגיבו לתרופות חדשות בצורה בטוחה ומדויקת יותר.
משכבות תאים פשוטות לרקמות פעימות זעירות
חוקרים מגדלים כיום באופן שגרתי תאי שריר לב אנושיים מתאים בוגרים שהופרו, הנקראים תאי גזע ספציפיים-מופעלים (induced pluripotent stem cells). תאים אלה ניתנים לפריסה בשכבות דקות או לכוון לצורות מסוימות בעזרת תבניות מיקרוסקופיות. אפילו ברמה הבסיסית הזו, שליטה בצורת התאים, בכיוונם וברכות המשטח משנה את עוצמת הפעימות ואת אופן הולכת האות החשמלי ביניהם. תרביות שטוחות אלה קלות לגידול בכמויות גדולות ולמדידה בעזרת מצלמות וחיישנים אוטומטיים, ולכן משמשות באופן רחב לבדיקת בטיחות ראשונית, במיוחד לזהות תרופות שעשויות להפריע לקצב הלב.
בניית רקמת לב תלת-ממדית וחללים לבביים
כדי לחקות קרוב יותר לב אמיתי, מדענים מרכיבים רקמות לב תלת־ממדיות על ידי ערבוב תאי לב עם חומרים ג׳לטיניים הדומים לסקלה הטבעית של הלב. רקמות לב מהונדסות אלה לרוב יוצרות סביב עמודים או טבעות כך שניתן למדוד את כווצתן הקטנה כשהן מושכות על התמיכות. על ידי יישום מתיחה סדירה ודפיקות חשמליות, הרקמות מפתחות בהדרגה מבנה והתנהגות שאופייניים לב מבוגר יותר. טלאים גדולים יותר ומבנים בצורת חלל יכולים אפילו לחקות כיצד חדר מתמלא ודוחף נוזל החוצה, מה שמאפשר מדידה של שינויים בלחץ–נפח דומים לאלה שבשימוש קליני. הוספת תאי כלי דם ותאי תמיכה מסייעת לרקמות אלה לשרוד זמן רב יותר ולהשתלב טוב יותר כאשר שתולים בלב בעלי חיים.
לבבות מיניאטוריים המתארגנים בעצמם והתפתחות מוקדמת
ענף מחקר נוסף מתמקד באורגנואידים — אשכולות של תאים המתארגנים בעצמם וידמו שלבים מוקדמים בהתפתחות הלב. מתוך תאי גזע, החוקרים מתאימים את התזמון ועוצמת אותות הגדילה כך שהתאים ימוינו באופן ספונטני לשכבות וייצרו מבנים חלולים ופועמים עם אזורים ראשוניים הדומים לחללים, תאי כיסוי חיצוניים וכלי דם פרימיטיביים. חלק מהאורגנואידים אפילו מייצרים רקמות מייצרות דם ודמויות כבד לצד אזורי הלב, ומספקים חלון על אופן התפתחותם המשותפת של איברים שונים. המודלים האלה חזקים במיוחד לחקר מומים מולדים, מצבים קרדיאליים תורשתיים ואופן התקשורת בין סוגי תאים שונים בלב במהלך ההתפתחות.
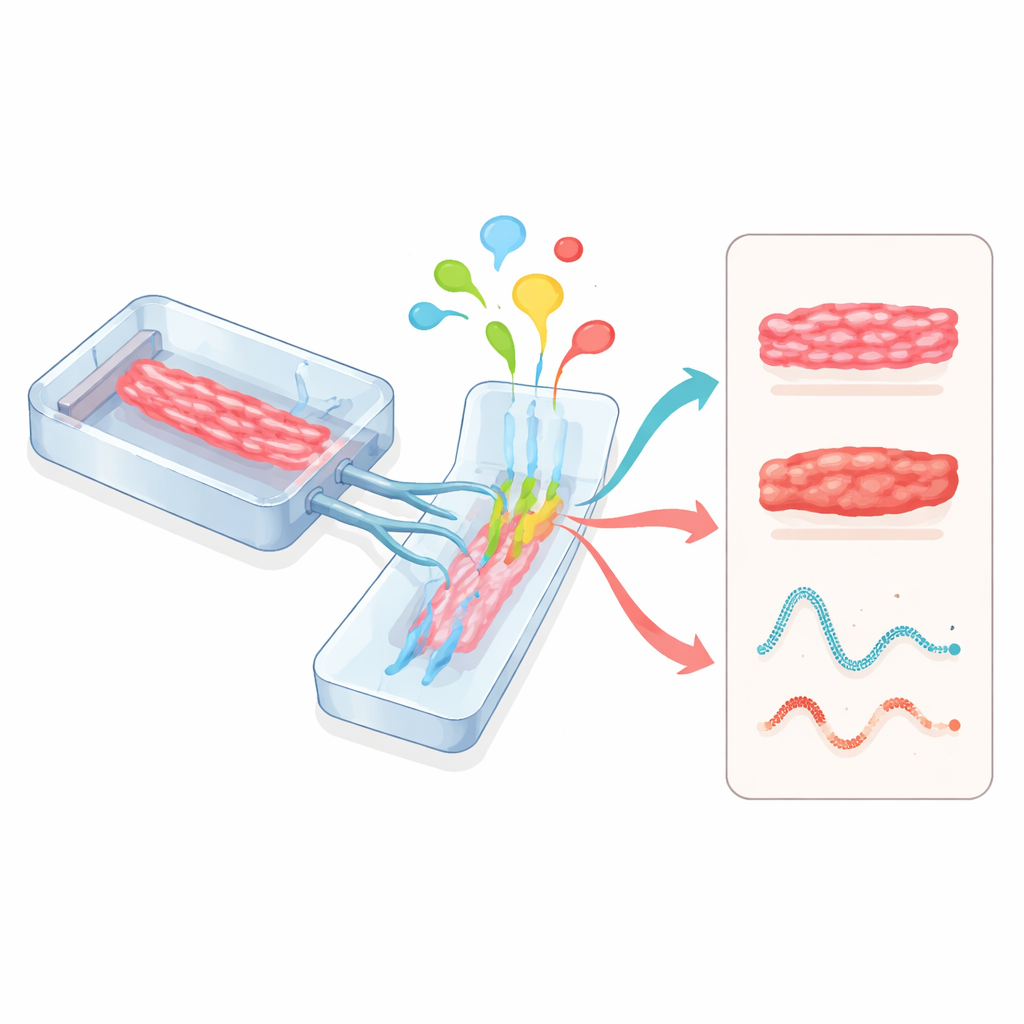
לב-על-צ׳יפ וקישוריות רב-איברית
מערכות מיקרופיזיולוגיות, הנקראות לעתים ״איבר-על-צ׳יפ״, נוקטות בגישה נוספת. רקמות לב גדלות בתוך התקנים קטנים ושקופים עם חריצים לזרימת נוזלים ודוּרים גמישים שניתן למתוח. הצ׳יפים האלה יכולים לשלוט בדיוק בחומרים מזינים, בחמצן, במתח מכאני ובקצב חשמלי בזמן שׁחיישנים עוקבים בזמן אמת אחרי עוצמת הפעימות והפעילות החשמלית. כאשר מודולי לב מקושרים עם מודולים של כבד, כלי דם או איברים אחרים באותו מעגל, החוקרים יכולים לראות כיצד תרופות המועברות על־ידי הכבד משפיעות על הלב, או כיצד דלקת ותאי חיסון משפיעים על תפקוד הלב. רגולטורים כגון מנהל המזון והתרופות האמריקאי החלו להכיר בצ׳יפים מבוססי-אדם אלה ככלים מבטיחים להערכת בטיחות תרופות.
מה המשמעות לכך עבור תרופות וטיפולים עתידיים
ביחד, שכבות תאים שטוחות, רקמות מהונדסות, אורגנואידים ואיבר-על-צ׳יפ מהווים ארגז כלים שמקרב את בדיקות הלב למציאות האנושית הרבה יותר מאשר מודלים של בעלי חיים לבדם. לכל מודל יש איזון משלו בין מציאותיות ופירקטיות, ושילובם מציע תמונה יותר שלמה של איך תרופה עשויה לעזור או להזיק ללב האנושי. למרות שעדיין יש אתגרים — כגון בישולם המלא של הלבבות המיניאטוריים, אספקת זרימת דם מציאותית ואחידות שיטות בין מעבדות — ההתקדמויות הללו מניחות את היסודות לתרופות בטוחות יותר, טיפולים מותאמים אישית יותר ובסופו של דבר רקמות לב שגודלו במעבדה שעשויות לסייע לתקן לבבות פגועים.
ציטוט: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
מילות מפתח: לב-על-צ׳יפ, אורגנואידים קרדיאליים, רקמת לב מהונדסת, קרדיוטוקסיות של תרופות, קרדיומיוציטים מ-hiPSC