Clear Sky Science · de
Fortgeschrittene in vitro-Kardio-Modelle zur Arzneimittelbewertung: Integration von Organoiden, konstruierten Geweben und mikrophysiologischen Systemen
Warum das Züchten von Mini-Herzen wichtig ist
Herzkrankheiten sind die weltweit häufigste Todesursache, dennoch scheitern viele vielversprechende Medikamente spät in der Entwicklung, weil heutige Labortests und Tierstudien oft schädliche Effekte auf das menschliche Herz übersehen. Dieser Artikel erklärt, wie Forschende zunehmend realistische „Mini-Herzen“ im Labor herstellen – von flachen Zellschichten über winzige schlagende Gewebe und Organoide bis hin zu Heart-on-a-Chip-Systemen – um besser und sicherer vorherzusagen, wie unsere Herzen auf neue Wirkstoffe reagieren.
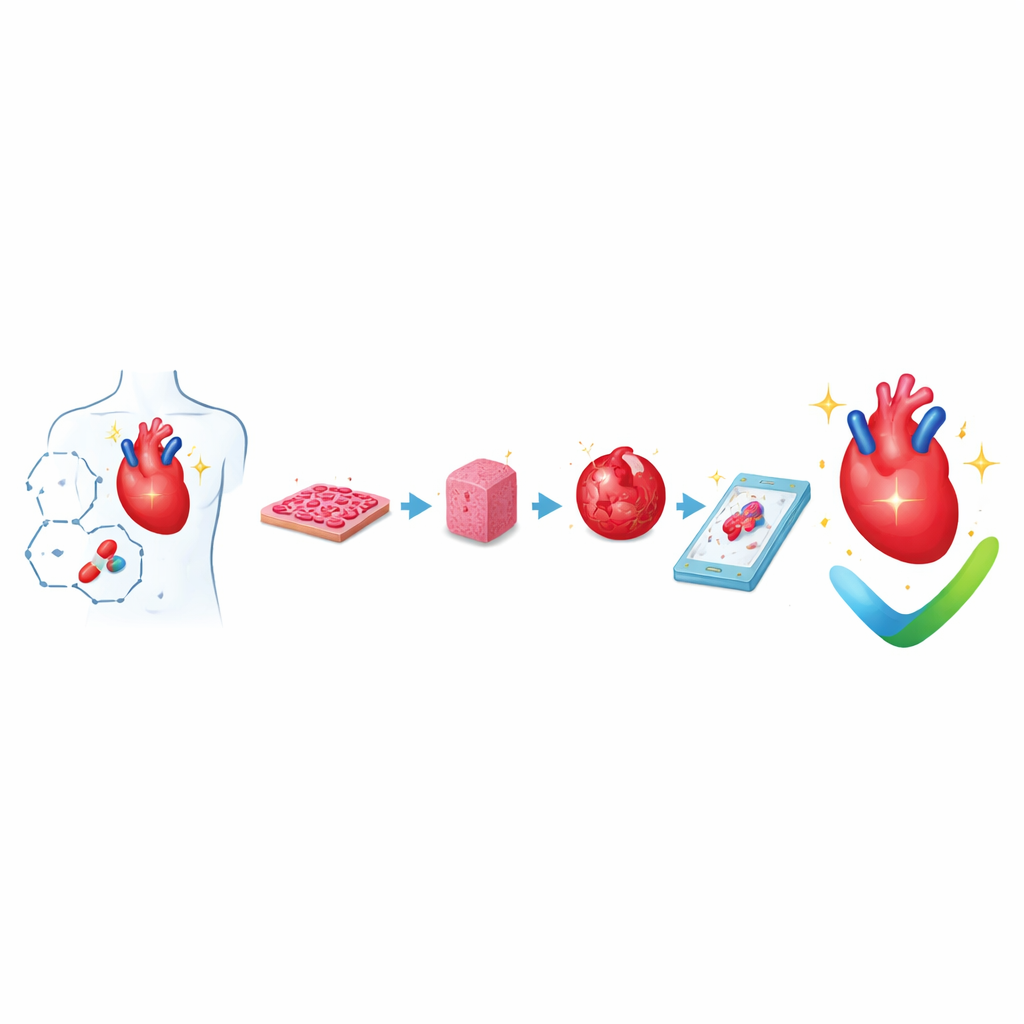
Von einfachen Zellschichten zu winzigen schlagenden Geweben
Forschende züchten inzwischen routinemäßig menschliche Herzmuskelzellen aus umprogrammierten Körperzellen, sogenannten induzierten pluripotenten Stammzellen. Diese Zellen lassen sich als dünne Schichten ausbreiten oder mithilfe mikroskopischer Muster in bestimmte Formen lenken. Schon auf diesem einfachen Niveau beeinflussen Kontrolle über Zellform, Ausrichtung und die Weichheit der Oberfläche, wie kräftig die Zellen schlagen und wie elektrische Signale zwischen ihnen weitergeleitet werden. Diese flachen Kulturen sind leicht in großer Zahl zu erzeugen und mit automatisierten Kameras und Sensoren zu messen, weshalb sie häufig für erste Sicherheitstests verwendet werden – insbesondere, um Arzneimittel zu erkennen, die den Herzrhythmus stören könnten.
Aufbau dreidimensionalen Herzmuskels und von Kammern
Um ein echtes Herz näher nachzubilden, setzen Wissenschaftler dreidimensionale Herzgewebe zusammen, indem sie Herz-Zellen mit gelartigen Materialien mischen, die dem natürlichen Gerüst des Herzens ähneln. Diese konstruierten Herzgewebe werden oft um Pfosten oder Ringe gegossen, sodass ihre winzigen Kontraktionen messbar werden, wenn sie an den Halterungen ziehen. Durch regelmäßiges Dehnen und elektrische Impulse entwickeln die Gewebe allmählich eine erwachsenere Struktur und Pumpleistung. Größere Patches und kammerförmige Konstrukte können sogar nachahmen, wie ein Ventrikel sich füllt und Flüssigkeit auswirft, wodurch Druck–Volumen-Änderungen messbar werden, ähnlich denen, die in der Klinik verwendet werden. Das Hinzufügen von Gefäßzellen und Stütz-Zellen verlängert das Überleben dieser Gewebe und verbessert ihre Integration, wenn sie in Tierherzen transplantiert werden.
Selbstorganisierende Mini-Herzen und frühe Entwicklung
Ein weiterer Forschungszweig konzentriert sich auf Organoide – selbstorganisierende Zellcluster, die frühe Stadien eines sich entwickelnden Herzens nachahmen. Ausgehend von Stammzellen passen Forschende Zeitpunkt und Stärke von Wachstums‑signalen so an, dass sich die Zellen spontan in Schichten sortieren und hohle, schlagende Strukturen mit frühen kammerähnlichen Bereichen, äußerer Deckzellschicht und primitiven Blutgefäßen bilden. Einige Organoide entwickeln sogar blutbildende und leberähnliche Gewebe neben den Herzregionen, was Einblicke gibt, wie verschiedene Organe gemeinsam entstehen. Diese Modelle sind besonders geeignet, um angeborene Fehlbildungen, vererbte Herzkrankheiten und die Kommunikation unterschiedlicher Zelltypen im Herzen während der Entwicklung zu untersuchen.
Hearts-on-Chips und multiorganische Verbindungen
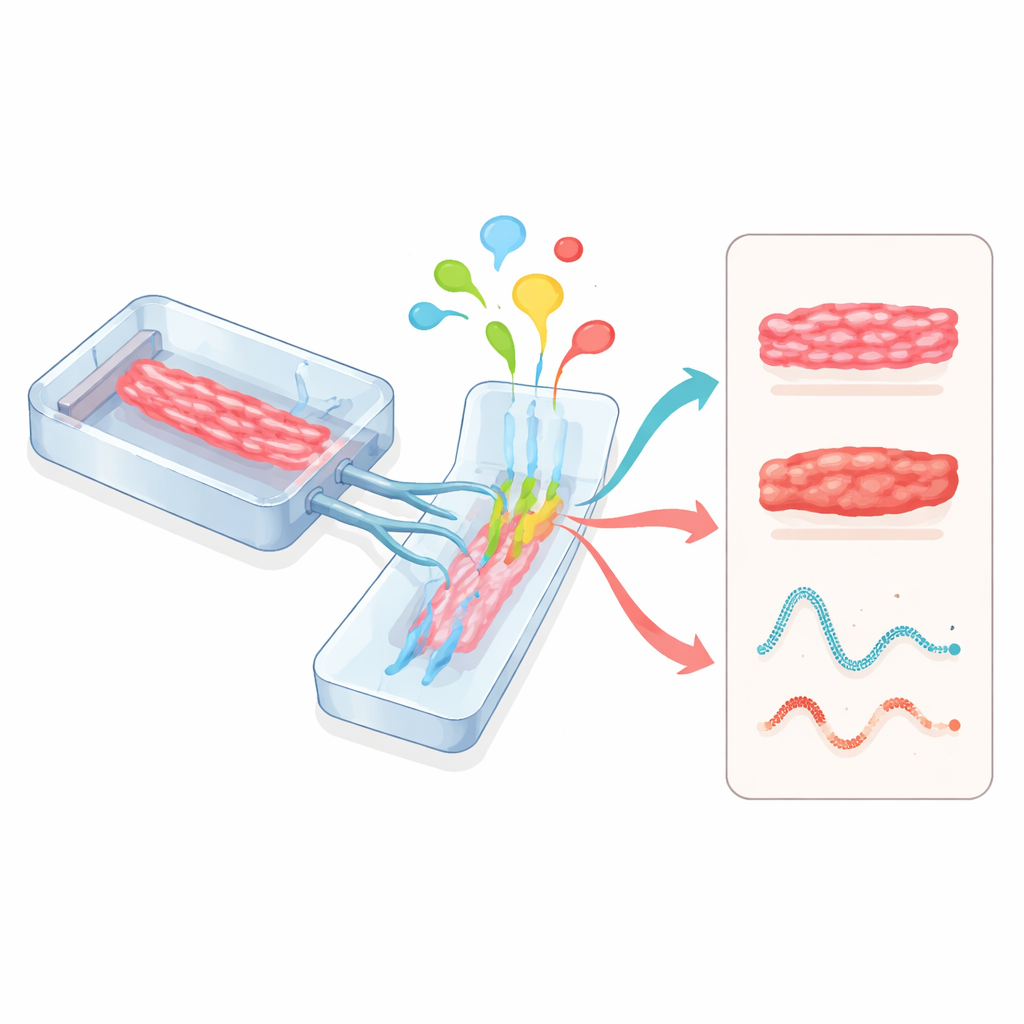
Mikrophysiologische Systeme, oft Organs-on-Chips genannt, verfolgen einen weiteren Ansatz. Herzgewebe werden in kleinen, transparenten Geräten gezüchtet, die Kanäle für Flüssigkeitsfluss und flexible Wände zum Dehnen enthalten. Diese Chips ermöglichen präzise Kontrolle von Nährstoffen, Sauerstoff, mechanischer Belastung und elektrischer Stimulation, während Sensoren Schlagkraft und elektrische Aktivität in Echtzeit verfolgen. Werden Herzmodule mit Leber-, Gefäß- oder anderen Organmodulen im selben Kreislauf verbunden, können Forschende sehen, wie in der Leber verstoffwechselte Medikamente das Herz beeinflussen oder wie Entzündungen und Immunzellen die Herzfunktion verändern. Regulierungsbehörden wie die US-amerikanische Food and Drug Administration erkennen diese menschenbasierten Chips zunehmend als vielversprechende Werkzeuge für die Arzneimittelsicherheit an.
Was das für künftige Medikamente und Therapien bedeutet
Zusammen bilden flache Zellschichten, konstruiertes Gewebe, Organoide und Organs-on-Chips ein Werkzeugset, das Herztests deutlich näher an die menschliche Realität bringt als traditionelle Tiermodelle allein. Jedes Modell balanciert Realismus und Praktikabilität auf seine Weise, und ihre Kombination liefert ein umfassenderes Bild davon, wie ein Medikament dem menschlichen Herzen nützen oder schaden könnte. Obwohl Herausforderungen bestehen bleiben – etwa die vollständige Reifung dieser Mini‑Herzen, eine realistische Blutversorgung und die Standardisierung von Methoden zwischen Laboren – bereiten diese Fortschritte den Boden für sicherere Medikamente, stärker personalisierte Therapien und schließlich im Labor gezüchtete Herzgewebe, die beschädigte Herzen reparieren könnten.
Zitation: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
Schlüsselwörter: heart-on-a-chip, kardiale Organoide, konstruiertes Herzgewebe, Arzneimittel-Kardiotoxizität, hiPSC-Kardiomyozyten