Clear Sky Science · es
Modelos cardíacos in vitro avanzados para la evaluación de fármacos: integración de organoides, tejidos diseñados y sistemas microfisiológicos
Por qué importa cultivar pequeños corazones
Las enfermedades cardiacas son la principal causa de muerte en el mundo, sin embargo muchos fármacos prometedores fracasan en fases avanzadas del desarrollo porque las pruebas de laboratorio y los estudios en animales actuales a menudo no detectan efectos nocivos sobre el corazón humano. Este artículo explica cómo los científicos están construyendo “mini corazones” cada vez más realistas en el laboratorio —desde capas celulares planas hasta pequeños tejidos palpitantes, organoides y sistemas corazón-en-un-chip— para predecir de forma más segura y precisa cómo responderá nuestro corazón a nuevos medicamentos.
De capas celulares simples a pequeños tejidos palpitantes
Hoy los investigadores cultivan de forma rutinaria células del músculo cardíaco humano a partir de células adultas reprogramadas, llamadas células madre pluripotentes inducidas. Estas células pueden disponerse en láminas delgadas o guiarse hacia formas concretas mediante patrones microscópicos. Incluso en este nivel básico, el control de la forma celular, la alineación y la rigidez de la superficie modifica la fuerza con que las células laten y la forma en que las señales eléctricas se propagan entre ellas. Estos cultivos planos son fáciles de producir en gran cantidad y de medir con cámaras y sensores automatizados, por lo que se usan ampliamente en la primera fase de pruebas de seguridad, especialmente para detectar fármacos que pueden alterar el ritmo cardíaco.
Construir músculo cardíaco tridimensional y cámaras
Para imitar más de cerca un corazón real, los científicos ensamblan tejidos cardíacos tridimensionales mezclando células cardíacas con materiales gelatinosos que se parecen al andamiaje natural del corazón. Estos tejidos cardíacos diseñados a menudo se moldean alrededor de postes o anillos para que sus pequeñas contracciones puedan medirse al tirar de los soportes. Aplicando estiramientos regulares y pulsos eléctricos, los tejidos desarrollan gradualmente una estructura y un comportamiento de bombeo más similares a los del corazón adulto. Parche más grandes y constructos con forma de cámara pueden incluso reproducir cómo un ventrículo se llena y expulsa fluido, lo que permite medir cambios presión–volumen parecidos a los utilizados en la clínica. Añadir células vasculares y células de soporte ayuda a que estos tejidos sobrevivan más tiempo e integren mejor cuando se trasplantan en corazones de animales.
Mini corazones autoensamblados y desarrollo temprano
Otra línea de investigación se centra en los organoides —agrupaciones de células que se autoorganizan y recuerdan etapas tempranas del desarrollo cardíaco. A partir de células madre, los investigadores ajustan el tiempo y la intensidad de las señales de crecimiento para que las células se ordenen espontáneamente en capas y formen estructuras huecas y palpitantes con regiones temprano-similares a cámaras, células de recubrimiento externo y vasos sanguíneos primitivos. Algunos organoides incluso generan tejidos formadores de sangre y parecidos al hígado junto a las regiones cardíacas, ofreciendo una ventana sobre cómo se co-desarrollan diferentes órganos. Estos modelos son especialmente potentes para estudiar malformaciones congénitas, afecciones cardíacas hereditarias y cómo se comunican distintos tipos celulares en el corazón durante el desarrollo.
Corazones-en-chips y conexiones multiórgano
Los sistemas microfisiológicos, llamados a menudo órganos-en-chips, adoptan otro enfoque. Los tejidos cardíacos se cultivan dentro de pequeños dispositivos transparentes grabados con canales para el flujo de fluidos y paredes flexibles que pueden estirarse. Estos chips pueden controlar con precisión nutrientes, oxígeno, esfuerzo mecánico y estimulación eléctrica mientras sensores registran la fuerza de latido y la actividad eléctrica en tiempo real. Cuando módulos cardíacos se conectan con módulos de hígado, vasos sanguíneos u otros órganos en el mismo circuito, los científicos pueden ver cómo los fármacos metabolizados por el hígado afectan al corazón, o cómo la inflamación y las células inmunitarias influyen en la función cardíaca. Reguladores como la Administración de Alimentos y Medicamentos de EE. UU. comienzan a reconocer estos chips basados en modelos humanos como herramientas prometedoras para la evaluación de la seguridad de fármacos.
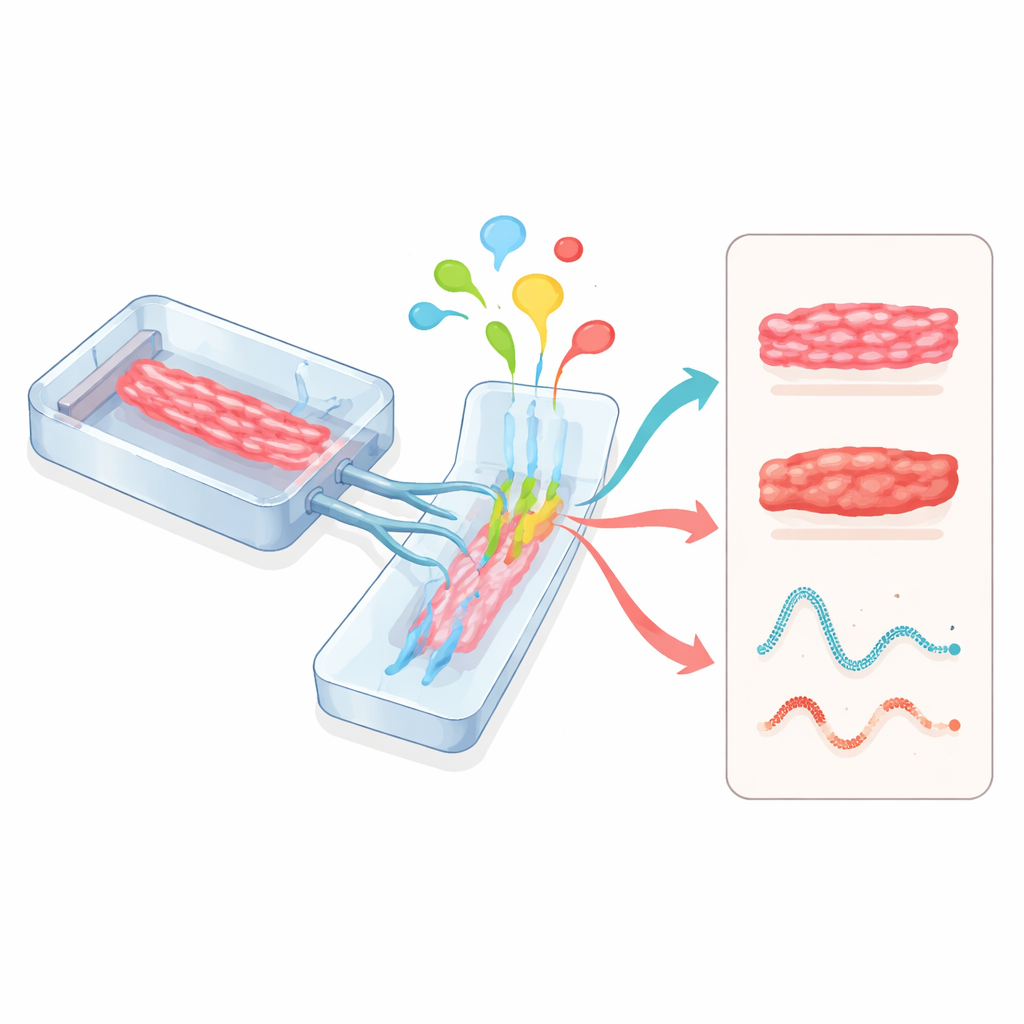
Qué significa esto para futuros medicamentos y terapias
En conjunto, capas celulares planas, tejidos diseñados, organoides y órganos-en-chips forman una caja de herramientas que acerca las pruebas cardíacas mucho más a la realidad humana que los modelos animales tradicionales por sí solos. Cada modelo equilibra de forma distinta realismo y practicidad, y combinarlos ofrece una visión más completa de cómo un fármaco podría ayudar o dañar el corazón humano. Aunque persisten desafíos —como madurar completamente estos mini corazones, suministrarles un flujo sanguíneo realista y estandarizar métodos entre laboratorios— estos avances están sentando las bases para fármacos más seguros, tratamientos más personalizados y, eventualmente, tejidos cardíacos cultivados en laboratorio que podrían ayudar a reparar corazones dañados.
Cita: Kim, Y.H., Son, Y.H., Choi, Y. et al. Advanced in vitro cardiac models for drug evaluation: integration of organoids, engineered tissues, and microphysiological systems. Microsyst Nanoeng 12, 162 (2026). https://doi.org/10.1038/s41378-026-01249-6
Palabras clave: corazón-en-un-chip, organoides cardíacos, tejido cardíaco diseñado, cardiotoxicidad de fármacos, cardiomiocitos hiPSC