Clear Sky Science · pt
Aprendizado profundo molecular na fronteira do espaço químico
Por que previsões de fármacos mais inteligentes importam
A descoberta moderna de fármacos recorre cada vez mais à inteligência artificial para vasculhar enormes bibliotecas de compostos e apontar candidatos promissores. Mas há um problema: muitos modelos de aprendizado de máquina funcionam bem apenas com moléculas que se assemelham bastante às que já viram antes. Quando são chamados a avaliar compostos mais incomuns — justamente aqueles que podem se tornar medicamentos inéditos — esses modelos podem ficar excessivamente confiantes e errar. Este estudo introduz uma nova forma de detectar quando um modelo está em terreno instável, ajudando pesquisadores a avançar de forma segura em regiões inexploradas do espaço químico.
Quando o mapa se esgota
Na descoberta de fármacos em estágio inicial, cientistas procuram “hits”: pequenas moléculas que afetam um alvo biológico, como uma proteína ligada a uma doença. Como executar experimentos de laboratório em bilhões de moléculas possíveis é impossível, modelos de aprendizado de máquina são treinados com algumas centenas ou milhares de compostos conhecidos e depois usados para prever quais novos compostos valem ser testados. No entanto, esses modelos tendem a falhar com moléculas diferentes das presentes nos dados de treinamento — um problema conhecido como deslocamento de distribuição. Salvaguardas existentes ou delimitam rigidamente a região conhecida, bloqueando moléculas mais ousadas, ou estimam a incerteza da previsão de maneiras que ainda podem enganar quando o modelo vê algo realmente novo.
Um novo senso de estranheza
Os autores propõem uma estratégia diferente baseada em um tipo de sistema de aprendizado profundo chamado autoencoder. Seu “modelo molecular conjunto” aprende duas tarefas ao mesmo tempo: prever se uma molécula é ativa contra um alvo e reconstruir a molécula a partir de um código interno comprimido. Se o modelo tem dificuldade em reconstruir uma molécula com precisão, essa molécula é considerada “estranha” (unfamiliar). A equipe transforma esse erro de reconstrução em uma pontuação numérica, chamada unfamiliarity, que reflete o quão distante uma molécula está dos padrões químicos que o modelo realmente aprendeu. Crucialmente, essa pontuação é guiada pela própria compreensão de química do modelo, em vez de medidas de similaridade simples e feitas à mão.
Testando a borda do espaço químico
Para avaliar quão bem a unfamiliarity detecta quando um modelo está fora de sua profundidade, os pesquisadores reuniram 33 conjuntos de dados cobrindo diferentes alvos biológicos e propriedades. Eles usaram métodos de agrupamento para dividir cada conjunto em exemplos típicos e outros estruturalmente mais incomuns, imitando a diferença entre moléculas bem estudadas e novas. Ao longo desses benchmarks, moléculas marcadas como fora-da-distribuição consistentemente apresentaram pontuações de unfamiliarity mais altas. Esse efeito não pôde ser explicado por características triviais, como tamanho ou complexidade da molécula. Em vez disso, a unfamiliarity acompanhou de perto o quão distante o núcleo estrutural de uma molécula estava em relação aos compostos de treinamento, confirmando que o modelo estava efetivamente percebendo o quão “fora da tabela” uma molécula era.
Vendo o que a incerteza sozinha pode perder
A equipe então comparou unfamiliarity com várias formas comuns de julgar a confiabilidade da previsão, incluindo a incerteza do modelo e diversas medidas de similaridade química. Tanto a unfamiliarity quanto a incerteza se relacionaram com o desempenho do classificador: quando qualquer uma das métricas era alta, as previsões tendiam a ser menos precisas. Ainda assim, os dois sinais foram em grande parte independentes. A unfamiliarity capturou tanto a distância estrutural quanto o desempenho, enquanto a incerteza sozinha não refletiu bem a estrutura, especialmente quando as moléculas provinham de uma distribuição muito diferente. Em triagens virtuais massivas com mais de um milhão de moléculas comerciais, a unfamiliarity separou nitidamente compostos rotineiros de verdadeiramente novos, ao passo que a incerteza sugeriu pouca diferença entre os dois grupos.
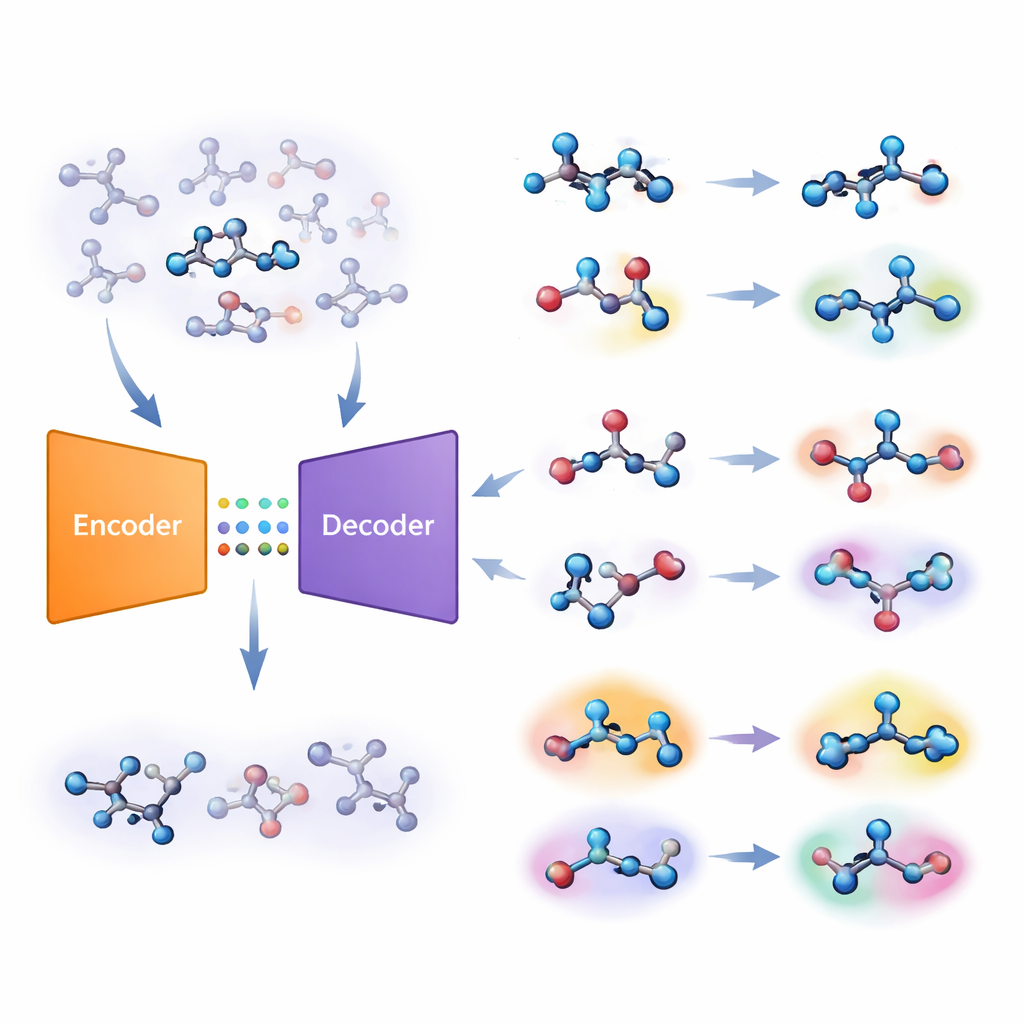
Da tela do computador ao laboratório úmido
Para demonstrar impacto prático, os pesquisadores realizaram uma triagem prospectiva em cerca de 180.000 moléculas adquiríveis, buscando inibidores de duas enzimas relevantes para doenças, PIM1 e CDK1. Eles treinaram seu modelo conjunto em conjuntos de dados existentes e modestos e então ranquearam novos compostos usando três ingredientes ao mesmo tempo: atividade prevista, incerteza do modelo e unfamiliarity. Após comprar e testar apenas 60 moléculas em ensaios bioquímicos, descobriram sete com potência na faixa de micromolar baixa, todas estruturalmente distintas dos compostos de treinamento e dos típicos inibidores de quinase. Estratégias que favoreciam baixa unfamiliarity — mantendo ainda margem para incerteza — tendiam a produzir os melhores hits, sugerindo que atentar para a unfamiliarity pode guiar a exploração rumo a química promissora, embora não completamente alienígena.
O que isso significa para medicamentos futuros
Em termos práticos, a pontuação de unfamiliarity dá aos modelos de aprendizado de máquina para química um senso embutido de quando estão extrapolando além do que conhecem. Ao ligar esse senso à capacidade do modelo de reconstruir moléculas, a abordagem reflete simultaneamente similaridade química e confiabilidade da previsão. O estudo mostra que essa métrica pode revelar deslocamentos de distribuição que métodos padrão perdem, melhorar a priorização em triagens virtuais e ajudar a descobrir nova matéria química em experimentos reais. À medida que caçadores de fármacos se aventuram cada vez mais nas vastas e em grande parte inexploradas regiões do espaço químico, a unfamiliarity oferece uma bússola fundamentada para decidir quais previsões audaciosas valem a pena ser acreditadas — e testadas no laboratório.
Citação: van Tilborg, D., Rossen, L. & Grisoni, F. Molecular deep learning at the edge of chemical space. Nat Mach Intell 8, 575–587 (2026). https://doi.org/10.1038/s42256-026-01216-w
Palavras-chave: aprendizado de máquina molecular, descoberta de fármacos, espaço químico, fora-da-distribuição, triagem virtual