Clear Sky Science · pt
Concentrado plaquetário de nova geração: Alb-PRF superou PRP e H-PRF na promoção da função endotelial e cicatrização de feridas
Por que curativos à base de sangue melhores importam
Para feridas persistentes — como úlceras diabéticas, sítios cirúrgicos ou lesões de cicatrização lenta — simplesmente fechar a pele não é suficiente. O corpo precisa reconstruir rapidamente os vasos sanguíneos microscópicos para levar oxigênio e nutrientes à área danificada. Os médicos já usam produtos à base de sangue feitos com as próprias plaquetas do paciente para acelerar esse processo, mas essas misturas ainda estão sendo aperfeiçoadas. Este estudo apresenta uma nova versão, chamada Alb-PRF, e mostra que ela pode superar produtos anteriores ao ajudar as células vasculares a sobreviver, migrar e reparar danos, especialmente sob estresse inflamatório.
Uma nova abordagem usando seu próprio sangue
O plasma rico em plaquetas tradicional (PRP) é feito centrifugando o sangue do paciente para concentrar plaquetas, que liberam fatores de crescimento que apoiam a cicatrização. No entanto, o PRP requer anticoagulantes e preparação complexa, e seus benefícios podem ser de curta duração. Um produto mais recente, o fibrina rica em plaquetas (PRF), evita anticoagulantes e forma uma malha natural que libera fatores de crescimento de forma lenta. Com base nisso, os pesquisadores desenvolveram o Alb-PRF combinando uma fração rica em fibrina do sangue com albumina tratada por calor do mesmo plasma. Isso cria uma membrana mais estável, em formato de gel, que pode durar mais e potencialmente liberar sinais de cicatrização de forma mais sustentada, tornando-a um candidato atraente para a medicina regenerativa.
Como o novo material foi testado
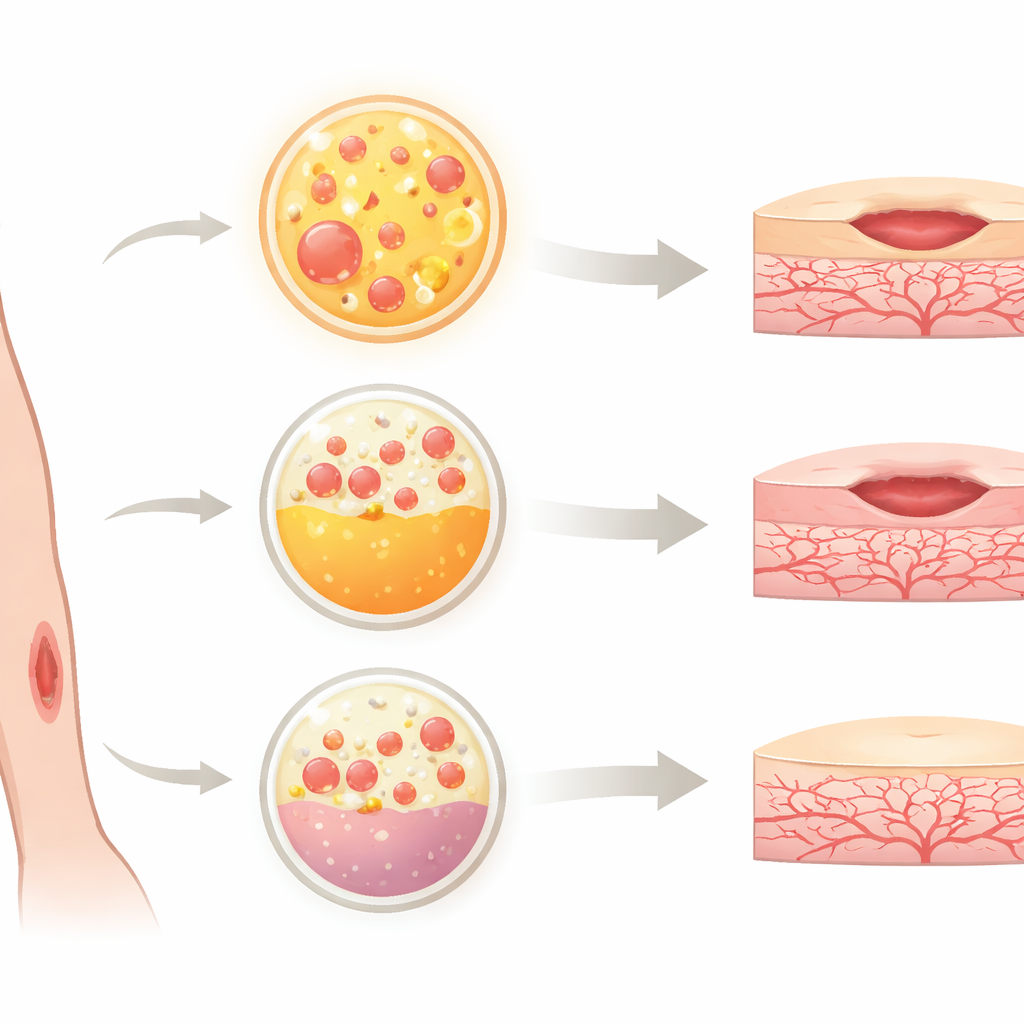
Para comparar o Alb-PRF com PRP e uma forma moderna de PRF conhecida como PRF horizontal (H-PRF), a equipe usou células que revestem os vasos sanguíneos, chamadas de células endoteliais da veia umbilical humana. Essas células são um modelo amplamente usado para estudar o crescimento e a reparação vascular. Os pesquisadores expuseram as células a meio condicionado com cada produto sanguíneo e verificaram várias características-chave: se as células permaneciam vivas, com que velocidade se multiplicavam, como seu citoesqueleto e forma interna mudavam, e quão bem migravam para fechar uma “ferida” artificial numa placa. Também simularam inflamação adicionando componentes bacterianos que normalmente lesionam células vasculares, e então avaliaram qual produto ofereceu a melhor proteção.
Auxiliando o crescimento e o movimento das células vasculares
Todos os três produtos sanguíneos mostraram-se seguros, sem diferenças significativas na morte celular em condições normais. Ainda assim, o Alb-PRF destacou-se pelo forte suporte ao crescimento celular: células endoteliais expostas ao Alb-PRF se multiplicaram mais do que as tratadas com PRP ou H-PRF. Ao microscópio, as células tratadas com Alb-PRF apresentaram formas mais alongadas e filamentos internos mais densos, sinais de que as células estavam ativamente organizando sua estrutura para movimento e reparo. Em ensaios tipo “risco” (scratch), o Alb-PRF levou ao fechamento mais rápido da lacuna, com cobertura quase completa após doze horas, superando claramente os outros dois tratamentos. Esses resultados apontam o Alb-PRF como um gatilho particularmente poderoso para os comportamentos celulares necessários à reconstrução de microvasos.
Protegendo vasos sanguíneos do dano inflamatório
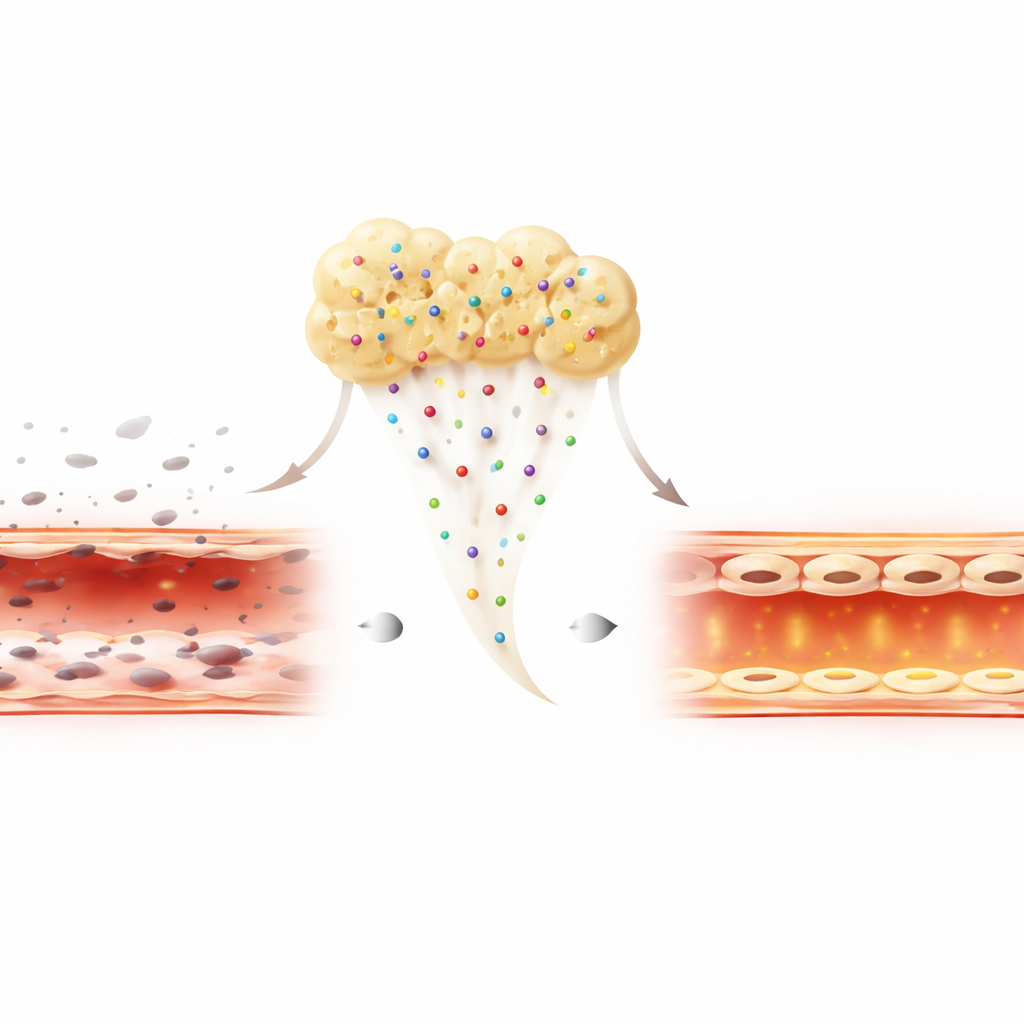
Feridas no mundo real frequentemente existem num ambiente inflamatório e hostil. Para imitar isso, os pesquisadores expuseram as células vasculares a uma toxina bacteriana que normalmente mata células e compromete sua barreira. Sob esse estresse, as três preparações ofereceram alguma proteção, mas H-PRF e especialmente Alb-PRF reduziram fortemente a morte celular em comparação ao PRP. As células tratadas com Alb-PRF não apenas sobreviveram melhor, como também apresentaram níveis mais altos de uma proteína de superfície chave, CD31, que ajuda as células vizinhas a se manterem unidas e a preservar uma parede vascular estreita e resistente a vazamentos. Isso sugere que o Alb-PRF faz mais do que manter as células vivas; ele apoia ativamente a reconstrução de um revestimento saudável e bem selado mesmo na presença de inflamação.
O que isso pode significar para o cuidado de feridas no futuro
Em conjunto, os achados mostram que o Alb-PRF combina a segurança dos tratamentos plaquetários existentes com um suporte mais forte ao crescimento, à migração e à resiliência das células vasculares diante da inflamação. Embora esses testes tenham sido realizados em placas de laboratório e precisem ser confirmados em estudos animais e ensaios clínicos, os resultados sugerem que o Alb-PRF poderia se tornar um “curativo biológico” autólogo de próxima geração. Ao ajudar os vasos a se regenerarem e permanecerem íntegros, pode oferecer aos pacientes cicatrização mais rápida, mais confiável e melhores desfechos em uma variedade de terapias regenerativas.
Citação: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
Palavras-chave: cicatrização de feridas, concentrados plaquetários, angiogênese, medicina regenerativa, células endoteliais