Clear Sky Science · nl
Nieuwe generatie plaatjesconcentraat: Alb-PRF presteerde beter dan PRP en H-PRF bij het bevorderen van endotheliale functie en wondgenezing
Waarom betere bloed-gebaseerde verbanden ertoe doen
Voor hardnekkige wonden—zoals diabetische zweren, operatiewonden of langzaam helende verwondingen—volstaat het niet om alleen de huid te sluiten. Het lichaam moet snel nieuwe kleine bloedvaatjes opbouwen om zuurstof en voedingsstoffen naar het beschadigde gebied te brengen. Artsen gebruiken al bloed-gebaseerde producten gemaakt van de eigen plaatjes van een patiënt om dit proces te versnellen, maar deze mengsels worden nog verfijnd. Deze studie introduceert een nieuwe variant, Alb-PRF, en laat zien dat deze mogelijk beter presteert dan oudere producten bij het helpen van vaatcellen om te overleven, te bewegen en schade te herstellen, vooral onder inflammatoire stress.
Een nieuwe wending in het gebruik van je eigen bloed
Traditioneel plaatjesrijk plasma (PRP) wordt gemaakt door het bloed van een patiënt te centrifugeren om plaatjes te concentreren, die groeifactoren afgeven die genezing ondersteunen. PRP vereist echter anticoagulantia en een complexe bereiding, en de voordelen kunnen van korte duur zijn. Een recenter product, plaatjesrijk fibrine (PRF), voorkomt anticoagulantia en vormt een natuurlijke matrix die groeifactoren langzaam vrijgeeft. Daarop voortbouwend ontwikkelden onderzoekers Alb-PRF door een fibrinerijke fractie van bloed te combineren met hitte-behandeld albumine uit hetzelfde plasma. Dit creëert een stabieler gel-achtig membraan dat langer kan meegaan en mogelijk genezingssignalen meer geleidelijk afgeeft, waardoor het een aantrekkelijke kandidaat is voor regeneratieve geneeskunde.
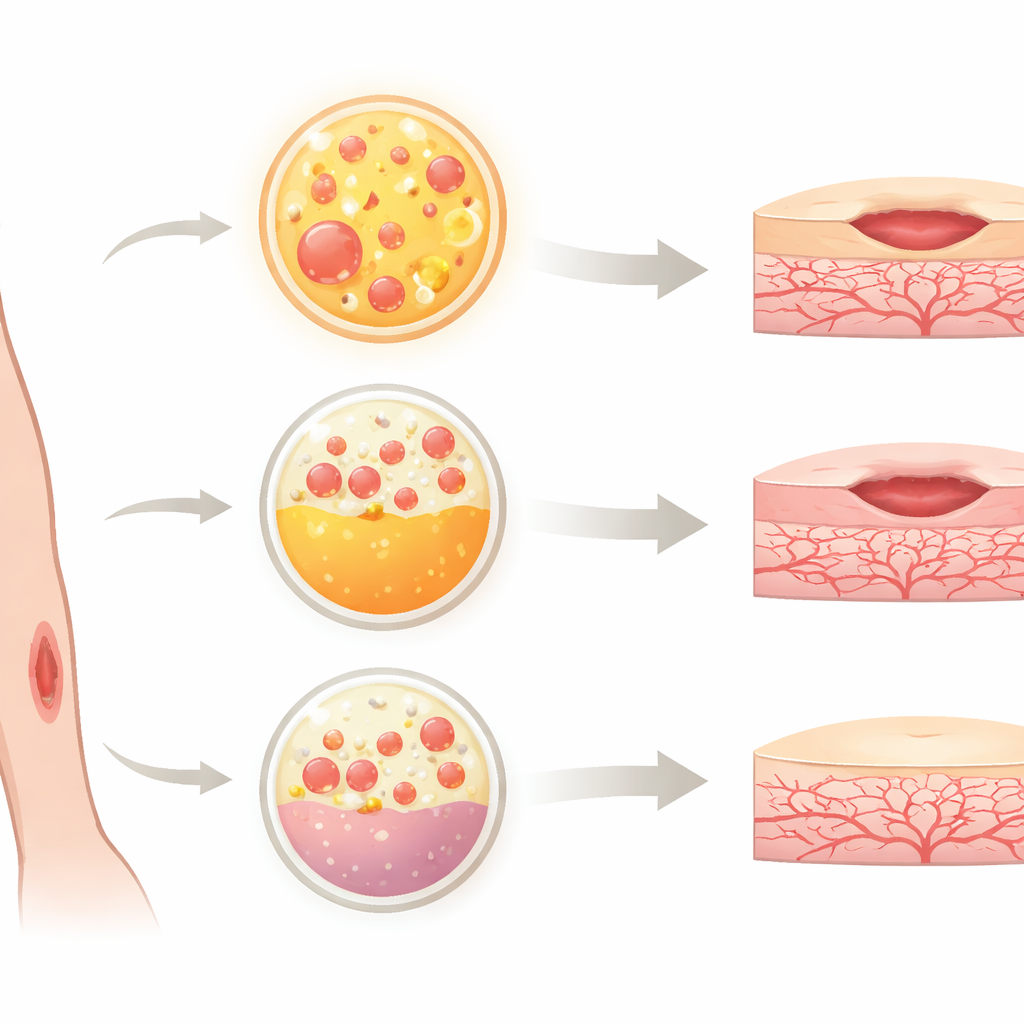
Hoe het nieuwe materiaal werd getest
Om te zien hoe Alb-PRF zich verhoudt tot PRP en een moderne vorm van PRF, bekend als horizontale PRF (H-PRF), gebruikte het team cellen die de bloedvaten bekleden, zogenaamde humane vena umbilicalis endotheelcellen. Deze cellen zijn een veelgebruikt model om vaatgroei en -herstel te bestuderen. De onderzoekers behandelden de cellen met medium geconditioneerd door elk bloedproduct en controleerden verschillende sleutelkenmerken: of de cellen leefden, hoe snel ze zich vermenigvuldigden, hoe hun interne steigersysteem en vorm veranderden, en hoe goed ze migreerden om een kunstmatige “wond” in een schaaltje te sluiten. Ze simuleerden ook ontsteking door bacteriële componenten toe te voegen die normaal vaatcellen beschadigen, en onderzochten welk product de beste bescherming bood.
Vaatcellen helpen groeien en bewegen
Alle drie de bloedproducten bleken veilig, zonder noemenswaardige verschillen in celdood onder normale omstandigheden. Toch viel Alb-PRF op door de sterke ondersteuning van celgroei: endotheelcellen die aan Alb-PRF werden blootgesteld vermenigvuldigden zich meer dan die behandeld met PRP of H-PRF. Onder de microscoop toonden Alb-PRF-behandelde cellen meer uitgerekte vormen en dichtere interne filamenten, tekenen dat de cellen actief hun structuur organiseerden voor beweging en herstel. In krasachtige wondassays leidde Alb-PRF tot de snelste sluiting van de kloof, met bijna volledige dekking na twaalf uur, en overtrof daarmee duidelijk de andere twee behandelingen. Deze resultaten wijzen op Alb-PRF als een bijzonder krachtige prikkel voor het cellulair gedrag dat nodig is om kleine bloedvaten te herbouwen.
Vaatwanden beschermen tegen inflammatoire schade
Wonden in de praktijk bestaan vaak in een ontstoken, vijandige omgeving. Om dit na te bootsen, stelden de onderzoekers de vaatcellen bloot aan een bacteriële toxine die normaal cellen doodt en hun barrière verstoort. Onder deze stress boden alle drie de preparaten enige bescherming, maar H-PRF en vooral Alb-PRF verminderden de celdood sterk vergeleken met PRP. Alb-PRF-behandelde cellen overleefden niet alleen beter, ze vertoonden ook hogere niveaus van een belangrijk oppervlakte-eiwit, CD31, dat buurcellen helpt aan elkaar te hechten en een stevige, lekvrije vaatwand te behouden. Dit suggereert dat Alb-PRF meer doet dan cellen alleen in leven houden; het ondersteunt actief het herstel van een gezonde, goed afgesloten bekleding, zelfs bij aanwezigheid van ontsteking.
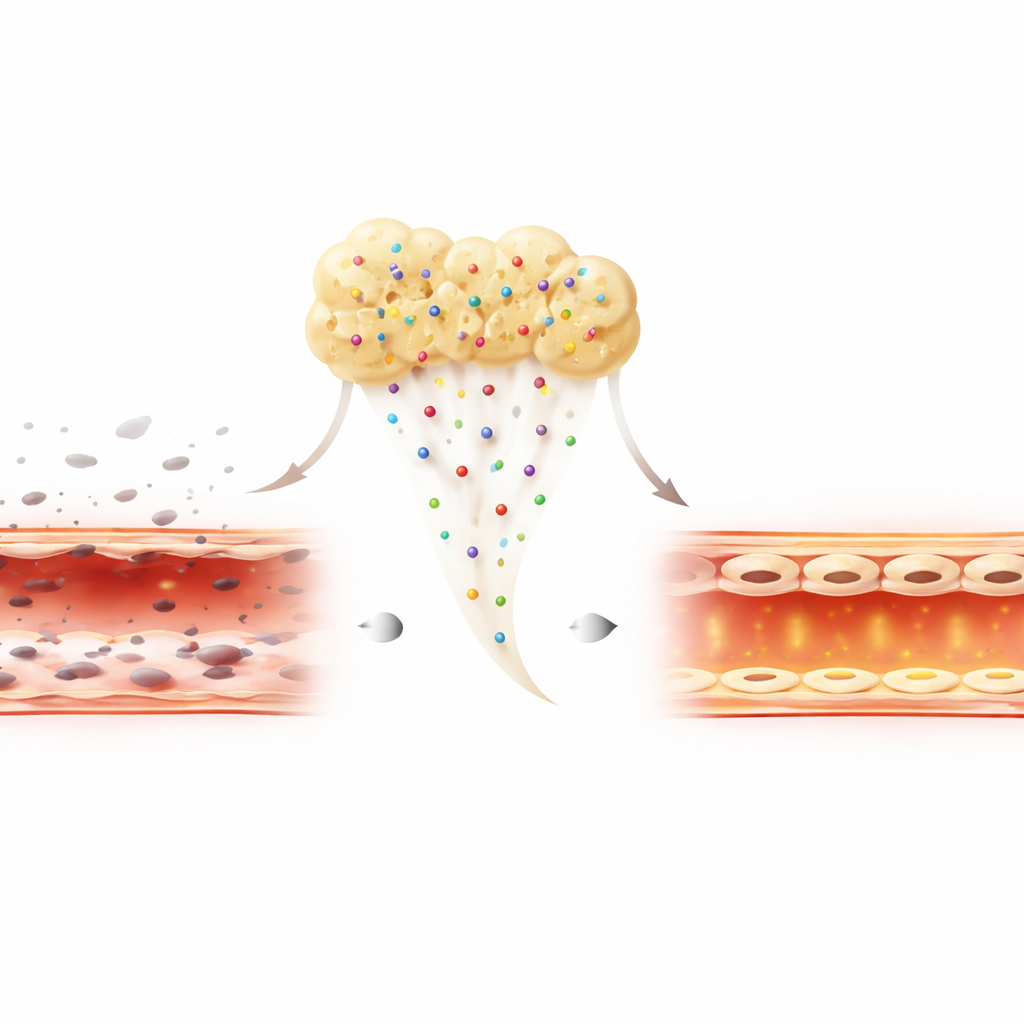
Wat dit kan betekenen voor toekomstige wondzorg
Gezamenlijk tonen de bevindingen aan dat Alb-PRF de veiligheid van bestaande plaatjes-gebaseerde behandelingen combineert met sterkere ondersteuning voor de groei, beweging en veerkracht van vaatcellen bij ontstekingsstress. Hoewel deze tests in laboratoriumschalen zijn uitgevoerd en bevestigd moeten worden in dierstudies en klinische onderzoeken, suggereren de resultaten dat Alb-PRF een volgende generatie autologe “biologische pleister” zou kunnen worden. Door te helpen bij het hergroeien en intact houden van vaten, kan het patiënten snellere, betrouwbaardere wondgenezing en betere uitkomsten bieden in een reeks regeneratieve therapieën.
Bronvermelding: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
Trefwoorden: wondgenezing, plaatjesconcentraten, angiogenese, regeneratieve geneeskunde, endotheelcellen