Clear Sky Science · ar
تركيز الصفائح الدموية الجيل التالي: ألبي-PRF تفوق على PRP وH-PRF في تعزيز وظيفة البطانية وشفاء الجروح
لماذا تهم الضمادات الدموية المحسّنة
بالنسبة للجروح المستعصية — مثل تقرحات السكري، أو مواقع العمليات الجراحية، أو الإصابات بطيئة الشفاء — إن مجرد إغلاق الجلد لا يكفي. يجب على الجسم إعادة بناء الأوعية الدقيقة بسرعة لإيصال الأكسجين والمواد المغذية إلى المنطقة المتضررة. يستخدم الأطباء بالفعل منتجات دموية مصنوعة من صفائح دم المريض نفسها لتسريع هذه العملية، لكن هذه الخلطات ما تزال تخضع للتحسين. تقدم هذه الدراسة نسخة جديدة تُسمى ألبي-PRF، وتُظهر أنها قد تتفوق على المنتجات الأقدم في مساعدة خلايا الأوعية الدموية على البقاء، والتحرك، وإصلاح الضرر، خاصة تحت ضغط الالتهاب.
تطوُّر جديد في استخدام دمك الذاتي
يُصنع البلازما الغنية بالصفائح الدموية التقليدية (PRP) عن طريق طرد دم المريض لتركز الصفائح الدموية، التي تُطلق عوامل نمو تدعم الشفاء. ومع ذلك، يتطلب PRP مضادات التخثر وإعداداً معقّداً، وقد تكون فوائده قصيرة الأمد. المنتج الأحدث، الفيبرين الغني بالصفائح (PRF)، يتجنب مضادات التخثر ويكوّن شبكة طبيعية تُطلق عوامل النمو ببطء. استناداً إلى ذلك، طور الباحثون ألبي-PRF بخلط جزء غني بالفيبرين من الدم مع ألبومين مُعالج بالحرارة من نفس البلازما. ينشئ هذا غشاءً شبيهاً بالهلام أكثر استقراراً يمكن أن يدوم لفترة أطول ويُطلق إشارات الشفاء بصورة أكثر استمرارية، مما يجعله خياراً جاذباً للطب التجديدي.
كيف اختبروا المادة الجديدة
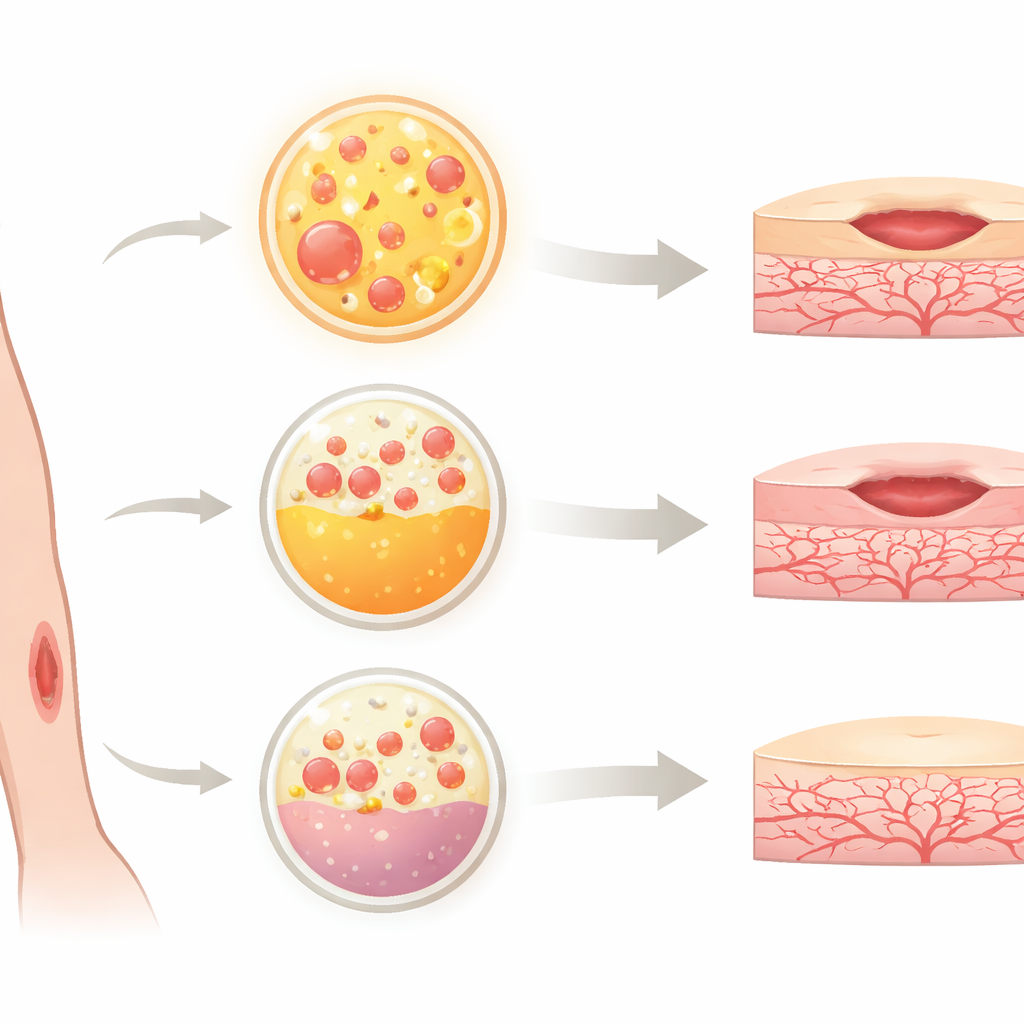
لمقارنة ألبي-PRF مع PRP وشكل حديث من PRF يعرف بـ H-PRF، استخدم الفريق خلايا تبطن الأوعية الدموية تسمى خلايا الوريد الحبل السري البشري البطانية. تُعد هذه الخلايا نموذجا شائعاً لدراسة نمو الأوعية وإصلاحها. عرض الباحثون الخلايا لوسط مُشروط بكل منتج دموي وفحصوا عدة خصائص رئيسية: ما إذا كانت الخلايا تبقى على قيد الحياة، ومدى سرعتها في التكاثر، وكيف تغيّر هيكلها الداخلي وشكلها، ومدى هجرتها لإغلاق "جُرح" اصطناعي في طبق آزرة. كما حاكو الالتهاب بإضافة مكونات بكتيرية التي تضرّ عادة بخلايا الأوعية، ثم راقبوا أي المنتجات قدمت أفضل حماية.
دعم نمو وحركة خلايا الأوعية
أظهرت المنتجات الدموية الثلاثة كلها سلامة الاستخدام، دون فروق ذات دلالة في موت الخلايا تحت الظروف العادية. ومع ذلك، تميّز ألبي-PRF بقوة في دعمه لنمو الخلايا: الخلايا البطانية المعالجة بألبي-PRF تكاثرت أكثر من تلك المعالجة بـ PRP أو H-PRF. تحت المجهر أظهرت الخلايا المعالجة بألبي-PRF أشكالاً أكثر استطالة وخيوطاً داخلية أكثر كثافة، وهي دلائل على أن الخلايا تنظم بنيتها للتحرك والإصلاح. في اختبارات الجروح الشبيهة بالخدش، أدى ألبي-PRF إلى إغلاق الفجوة بأسرع وتيرة، مع تغطية تقترب من الاكتمال بعد اثنتي عشرة ساعة، متفوقاً بوضوح على العلاجين الآخرين. تشير هذه النتائج إلى أن ألبي-PRF يمثل محفزاً قوياً لسلوكيات الخلايا المطلوبة لإعادة بناء الأوعية الدقيقة.
حماية الأوعية من الضرر الالتهابي
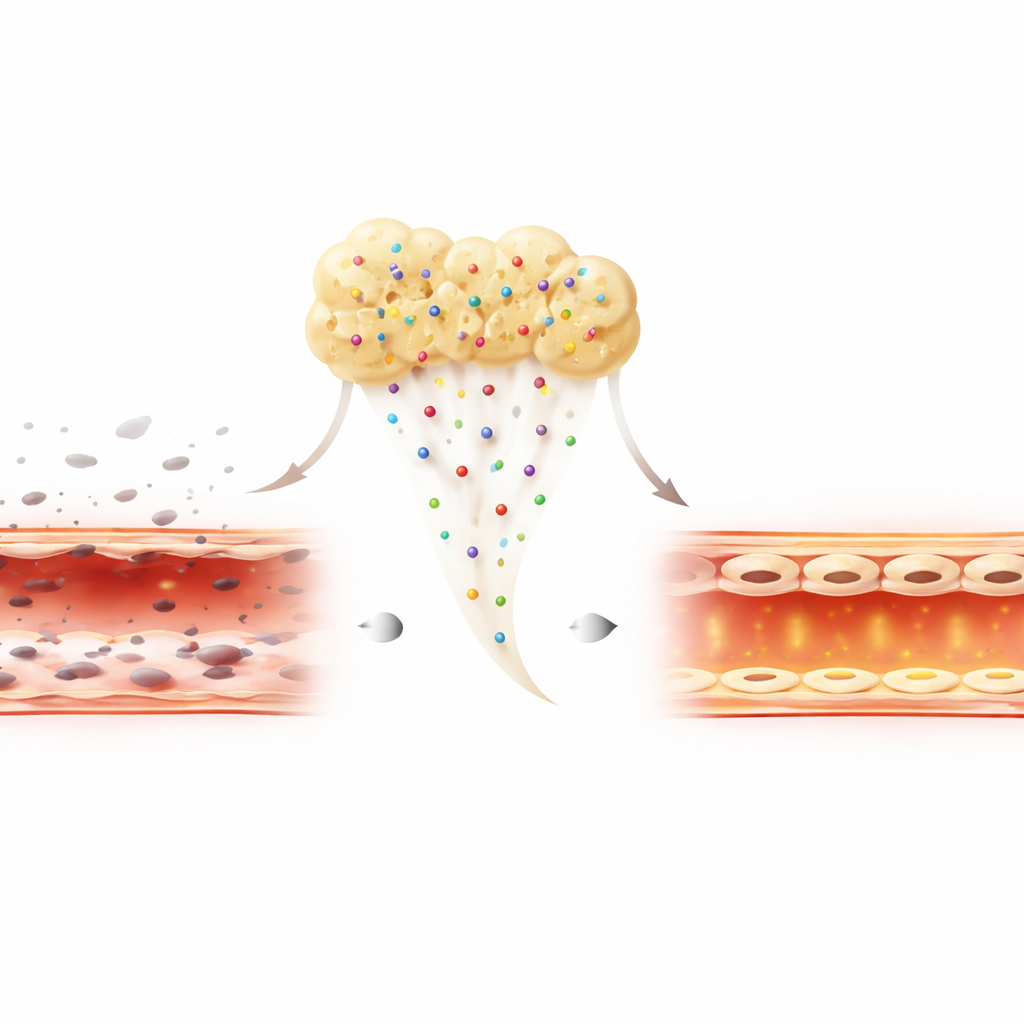
توجد الجروح في العالم الحقيقي غالباً في بيئة ملتهبة ومعادية. لمحاكاة ذلك، عرض الباحثون خلايا الأوعية لسم بكتيري يقتل الخلايا ويعطل حاجزها. تحت هذا الضغط، قدمت التحضيرات الثلاثة بعض الحماية، لكن H-PRF وخاصة ألبي-PRF خففا بشكل حاد من موت الخلايا مقارنة بـ PRP. لم تقتصر فائدة ألبي-PRF على بقاء الخلايا بشكل أفضل فحسب، بل أبدت الخلايا مستويات أعلى من بروتين سطحي رئيسي، CD31، الذي يساعد الخلايا المجاورة على الالتصاق ببعضها والحفاظ على جدار وعائي محكم ومقاوم للتسرب. وهذا يوحي بأن ألبي-PRF يفعل أكثر من إبقاء الخلايا على قيد الحياة؛ إنه يدعم بنشاط إعادة بناء بطانة صحية ومحكمة حتى في وجود الالتهاب.
ماذا قد يعني هذا لرعاية الجروح مستقبلاً
بالتالي، تُظهر النتائج أن ألبي-PRF يجمع بين أمان العلاجات القائمة على الصفائح الدموية ودعماً أقوى لنمو خلايا الأوعية، وحركتها، ومقاومتها أمام الالتهاب. على الرغم من أن هذه الاختبارات أُجريت في أطباق مخبرية وستحتاج إلى تأكيد في دراسات حيوانية وتجارب سريرية، تشير النتائج إلى أن ألبي-PRF قد يصبح "ضمادة بيولوجية" ذاتية الجيل التالي. من خلال مساعدة الأوعية على إعادة النمو والبقاء متماسكة، قد يقدم للمرضى شفاء جروح أسرع وأكثر موثوقية ونتائج محسنة عبر طيف من علاجات التجديد.
الاستشهاد: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
الكلمات المفتاحية: شفاء الجروح, مركَّزات الصفائح الدموية, تكوّن الأوعية الدموية, الطب التجديدي, خلايا بطانية