Clear Sky Science · de
Plättchenkonzentrat der nächsten Generation: Alb-PRF übertraf PRP und H-PRF bei der Förderung der Endothelfunktion und Wundheilung
Warum bessere blutbasierte Verbände wichtig sind
Bei hartnäckigen Wunden – etwa diabetischen Ulzera, Operationswunden oder langsam heilenden Verletzungen – reicht das bloße Verschließen der Haut nicht aus. Der Körper muss rasch winzige Blutgefäße wiederaufbauen, um Sauerstoff und Nährstoffe in das geschädigte Gewebe zu bringen. Ärztinnen und Ärzte verwenden bereits blutbasierte Produkte aus den eigenen Thrombozyten der Patientinnen und Patienten, um diesen Prozess zu beschleunigen, doch diese Mischungen werden weiterhin verfeinert. Diese Studie stellt eine neue Variante namens Alb-PRF vor und zeigt, dass sie ältere Produkte möglicherweise übertrifft, wenn es darum geht, Gefäßzellen beim Überleben, bei der Migration und bei der Reparatur von Schäden zu unterstützen – insbesondere unter entzündlichem Stress.
Eine neue Variante der Nutzung des eigenen Bluts
Traditionelles plättchenreiches Plasma (PRP) entsteht durch Zentrifugation des Bluts, um Thrombozyten zu konzentrieren, die Wachstumsfaktoren freisetzen und die Heilung fördern. PRP erfordert jedoch Antikoagulanzien und eine komplexe Vorbereitung, und seine Wirkung kann nur von kurzer Dauer sein. Ein jüngeres Produkt, plättchenreiches Fibrin (PRF), kommt ohne Antikoagulanzien aus und bildet ein natürliches Netz, das Wachstumsfaktoren langsam freisetzt. Darauf aufbauend entwickelten Forschende Alb-PRF, indem sie einen fibrinreichen Blutanteil mit wärmebehandeltem Albumin aus demselben Plasma kombinierten. Dadurch entsteht eine stabilere, gelartige Membran, die länger bestehen und Heilungssignale nachhaltiger abgeben kann – ein vielversprechender Kandidat für die regenerative Medizin.
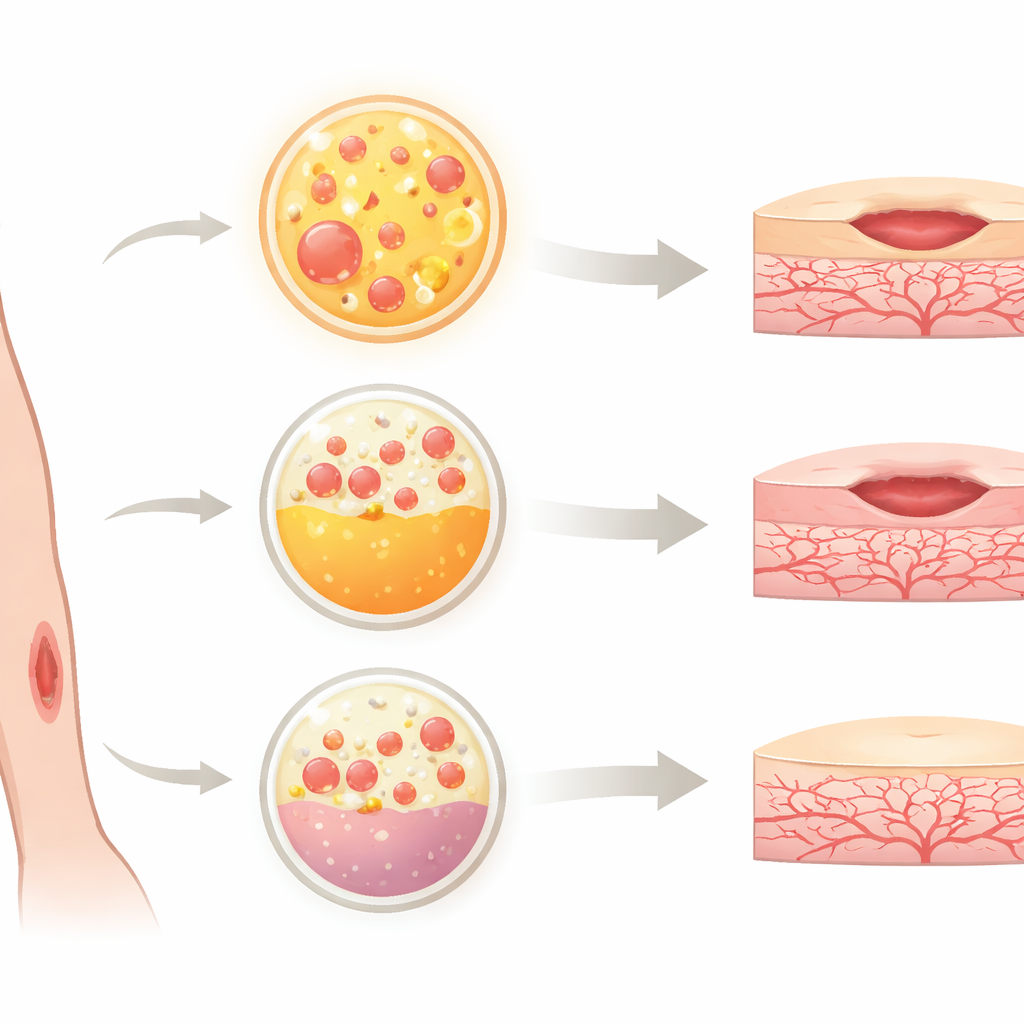
Wie das neue Material getestet wurde
Um zu prüfen, wie Alb-PRF im Vergleich zu PRP und einer modernen Form von PRF, der horizontalen PRF (H-PRF), abschneidet, verwendete das Team Zellen, die Blutgefäße auskleiden, sogenannte humane Nabelschnurvenen-Endothelzellen. Diese Zellen sind ein weit verbreitetes Modell zur Untersuchung von Gefäßwachstum und -reparatur. Die Forschenden setzten die Zellen mit Medien in Kontakt, die mit jedem Blutprodukt konditioniert waren, und untersuchten mehrere Schlüsselfunktionen: ob die Zellen überlebten, wie schnell sie sich teilten, wie sich ihr inneres Gerüst und ihre Form veränderten und wie gut sie migrierten, um eine künstliche „Wunde“ in einer Kultur zu schließen. Zusätzlich simulierten sie Entzündung, indem sie bakterielle Bestandteile hinzufügten, die Gefäßzellen normalerweise schädigen, und prüften, welches Produkt den besten Schutz bot.
Unterstützung von Wachstum und Bewegung der Gefäßzellen
Alle drei Blutprodukte erwiesen sich als sicher, ohne nennenswerte Unterschiede in der Zellsterblichkeit unter normalen Bedingungen. Dennoch hob sich Alb-PRF dadurch ab, dass es das Zellwachstum besonders stark förderte: Endothelzellen, die mit Alb-PRF behandelt wurden, teilten sich stärker als solche, die mit PRP oder H-PRF behandelt wurden. Unter dem Mikroskop zeigten Alb-PRF-behandelte Zellen länglichere Formen und dichtere interne Filamente – Anzeichen dafür, dass die Zellen aktiv ihre Struktur für Bewegung und Reparatur organisieren. In Kratz-Assays zur Wundheilung führte Alb-PRF zur schnellsten Schließung der Lücke, mit nahezu vollständiger Abdeckung nach zwölf Stunden und damit deutlich besser als die beiden anderen Behandlungen. Diese Ergebnisse deuten darauf hin, dass Alb-PRF ein besonders wirkungsvoller Auslöser für die zellulären Verhaltensweisen ist, die zum Wiederaufbau feiner Blutgefäße notwendig sind.
Schutz der Blutgefäße vor entzündlichen Schäden
Reale Wunden befinden sich oft in einer entzündeten, feindlichen Umgebung. Um dies nachzuahmen, setzten die Forschenden die Gefäßzellen einem bakteriellen Toxin aus, das Zellen typischerweise abtötet und ihre Barrierefunktion stört. Unter diesem Stress boten alle drei Präparate einen gewissen Schutz, doch H-PRF und insbesondere Alb-PRF reduzierten die Zellsterblichkeit deutlich stärker im Vergleich zu PRP. Alb-PRF-behandelte Zellen überlebten nicht nur besser, sondern zeigten auch höhere Spiegel eines wichtigen Oberflächenproteins, CD31, das Nachbarzellen aneinander bindet und eine dichte, wenig durchlässige Gefäßwand erhält. Das legt nahe, dass Alb-PRF mehr leistet als nur das Überleben der Zellen zu sichern: Es unterstützt aktiv den Wiederaufbau eines gesunden, gut abgedichteten Endothels, selbst unter entzündlichen Bedingungen.
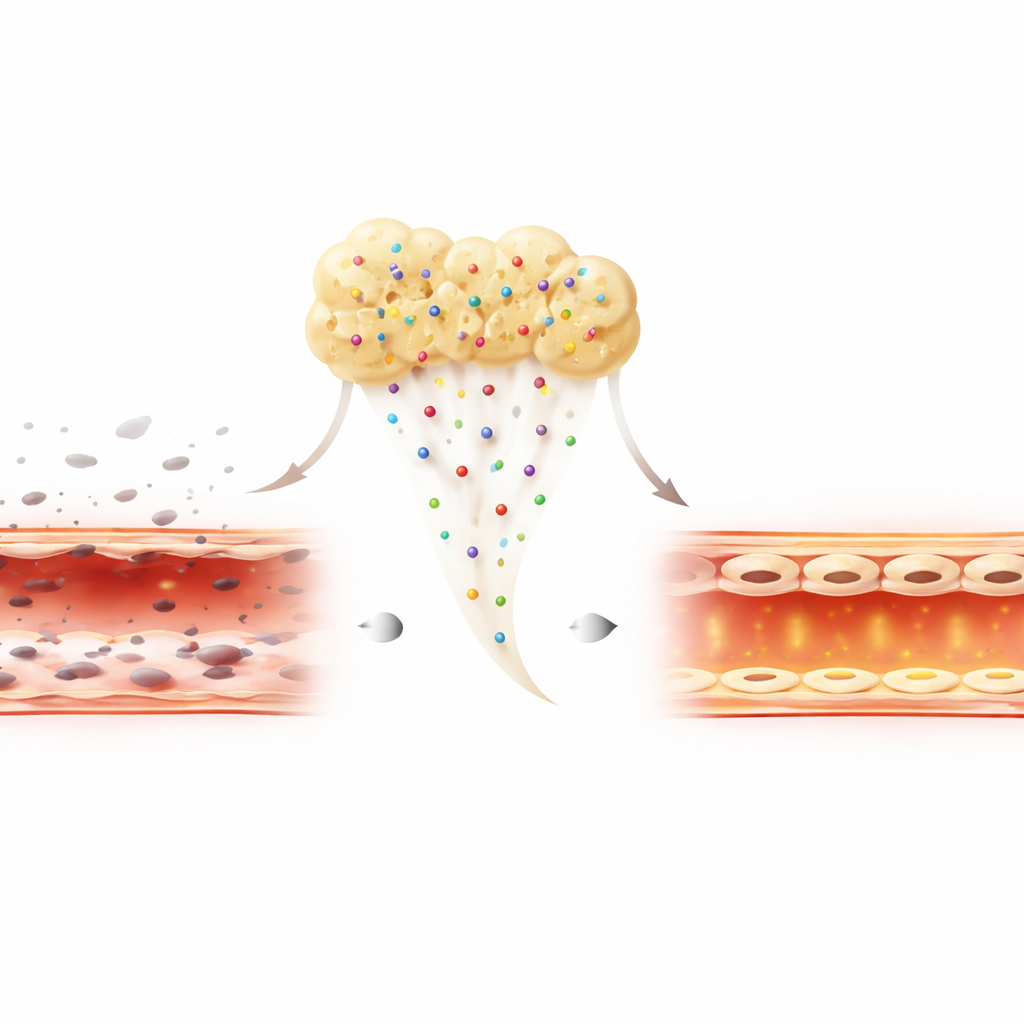
Was das für die zukünftige Wundversorgung bedeuten könnte
Insgesamt zeigen die Befunde, dass Alb-PRF die Sicherheit bestehender plättchenbasierter Behandlungen mit einer stärkeren Unterstützung für Wachstum, Bewegung und Widerstandskraft von Gefäßzellen kombiniert – auch bei Entzündung. Obwohl diese Tests im Labor durchgeführt wurden und in Tierstudien sowie klinischen Prüfungen bestätigt werden müssen, deuten die Ergebnisse darauf hin, dass Alb-PRF zu einem nächsten Schritt autologer „biologischer Verbände“ werden könnte. Indem es das Nachwachsen und die Stabilität der Gefäße fördert, könnte es Patientinnen und Patienten schnellere, verlässlichere Wundheilung und bessere Ergebnisse in einer Reihe regenerativer Therapien bieten.
Zitation: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
Schlüsselwörter: Wundheilung, Plättchenkonzentrate, Angiogenese, regenerative Medizin, Endothelzellen