Clear Sky Science · it
Concentrato piastrinico di nuova generazione: Alb-PRF ha superato PRP e H-PRF nel promuovere la funzione endoteliale e la guarigione delle ferite
Perché contano i cerotti a base di sangue migliori
Per le ferite resistenti—come le ulcere diabetiche, i siti chirurgici o le lesioni a lenta guarigione—chiudere semplicemente la pelle non è sufficiente. Il corpo deve ricostruire rapidamente i piccoli vasi sanguigni per portare ossigeno e nutrienti alla zona danneggiata. I medici utilizzano già prodotti a base di sangue derivati dalle piastrine del paziente per accelerare questo processo, ma queste miscele sono ancora in fase di perfezionamento. Questo studio presenta una nuova versione, chiamata Alb-PRF, e mostra che potrebbe superare i prodotti più datati nell’aiutare le cellule vascolari a sopravvivere, muoversi e riparare i danni, specialmente sotto stress infiammatorio.
Una nuova variante nell’uso del proprio sangue
Il plasma ricco di piastrine tradizionale (PRP) si ottiene centrifugando il sangue del paziente per concentrare le piastrine, che rilasciano fattori di crescita che favoriscono la guarigione. Tuttavia, il PRP richiede anticoagulanti e una preparazione complessa, e i suoi benefici possono essere di breve durata. Un prodotto più recente, il fibrinato ricco di piastrine (PRF), evita gli anticoagulanti e forma una rete naturale che rilascia lentamente i fattori di crescita. Su questa base, i ricercatori hanno sviluppato l’Alb-PRF combinando una frazione ricca di fibrina del sangue con albumina trattata termicamente proveniente dallo stesso plasma. Ciò crea una membrana più stabile e gelatinosa che può durare più a lungo e potenzialmente rilasciare segnali di guarigione in modo più sostenuto, rendendola un candidato interessante per la medicina rigenerativa.
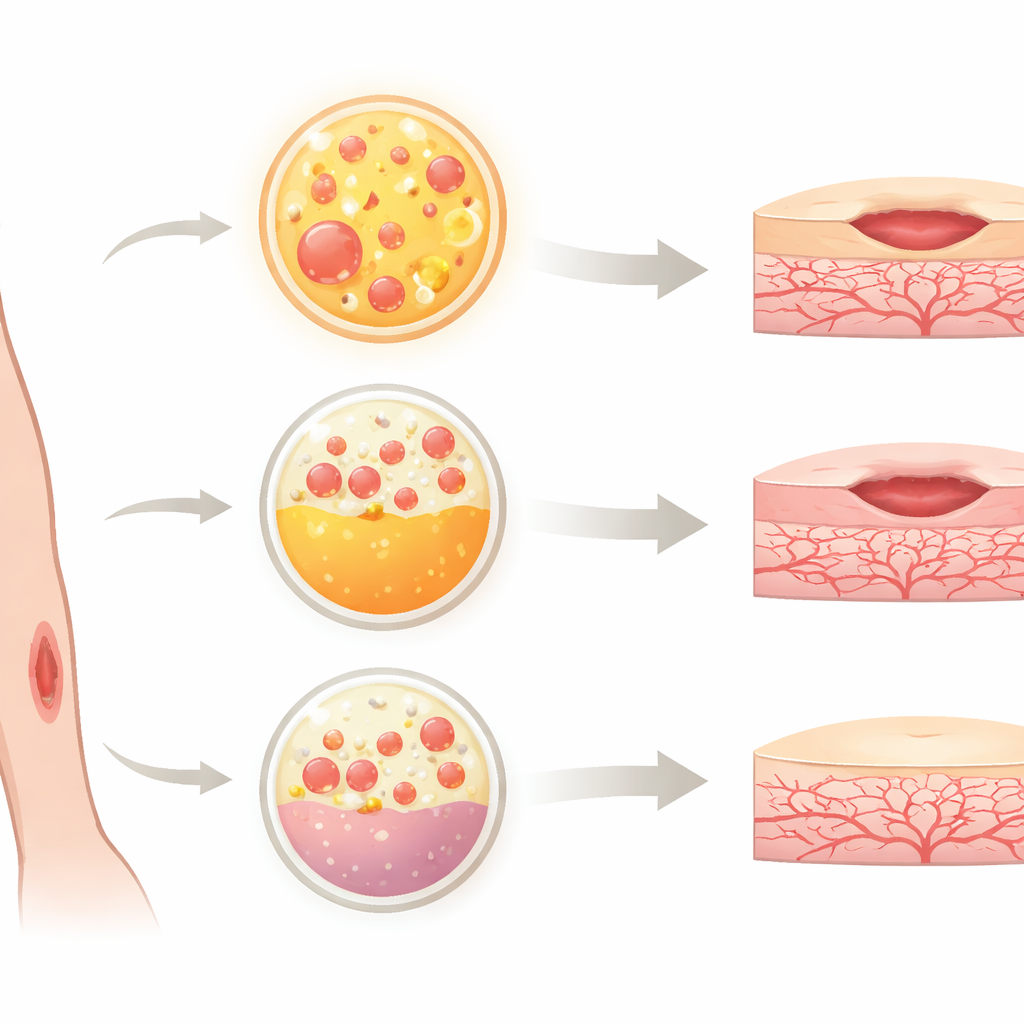
Come è stato testato il nuovo materiale
Per confrontare Alb-PRF con il PRP e una forma moderna di PRF nota come horizontal PRF (H-PRF), il team ha utilizzato cellule che rivestono i vasi sanguigni, chiamate cellule endoteliali della vena ombelicale umana. Queste cellule sono un modello ampiamente usato per studiare la crescita e la riparazione dei vasi. I ricercatori hanno esposto le cellule a terreni condizionati con ciascun prodotto sanguigno e hanno valutato diverse caratteristiche chiave: se le cellule restavano vive, quanto rapidamente si moltiplicavano, come cambiava il loro impalcatura interna e la forma, e quanto bene migravano per chiudere una “ferita” artificiale in coltura. Hanno anche simulato l’infiammazione aggiungendo componenti batteriche che normalmente danneggiano le cellule vascolari, per poi verificare quale prodotto offrisse la protezione migliore.
Favorire la crescita e il movimento delle cellule vascolari
Tutti e tre i prodotti sanguigni si sono dimostrati sicuri, senza differenze significative nella morte cellulare in condizioni normali. Tuttavia Alb-PRF si è distinto per il supporto più marcato alla crescita cellulare: le cellule endoteliali esposte ad Alb-PRF si sono moltiplicate più di quelle trattate con PRP o H-PRF. Al microscopio, le cellule trattate con Alb-PRF presentavano forme più allungate e filamenti interni più densi, segnali che le cellule stavano riorganizzando attivamente la loro struttura per il movimento e la riparazione. Nei saggi di tipo «scratch», Alb-PRF ha portato alla chiusura più rapida del gap, con una copertura quasi completa dopo dodici ore, superando chiaramente gli altri due trattamenti. Questi risultati indicano che Alb-PRF è un potente stimolo per i comportamenti cellulari necessari a ricostruire i piccoli vasi.
Proteggere i vasi dall’oppressione infiammatoria
Le ferite nel mondo reale spesso esistono in un ambiente infiammato e ostile. Per imitare questo, i ricercatori hanno esposto le cellule vascolari a una tossina batterica che normalmente uccide le cellule e compromette la loro barriera. Sotto questo stress, tutte e tre le preparazioni hanno offerto una certa protezione, ma H-PRF e soprattutto Alb-PRF hanno ridotto nettamente la morte cellulare rispetto al PRP. Le cellule trattate con Alb-PRF non solo sono sopravvissute meglio, ma hanno anche mostrato livelli più elevati di una proteina di superficie chiave, CD31, che aiuta le cellule vicine ad aderire e a mantenere una parete vascolare stretta e resistente alle perdite. Ciò suggerisce che Alb-PRF non si limita a tenere in vita le cellule; sostiene attivamente la ricostruzione di un rivestimento sano e ben sigillato anche in presenza di infiammazione.
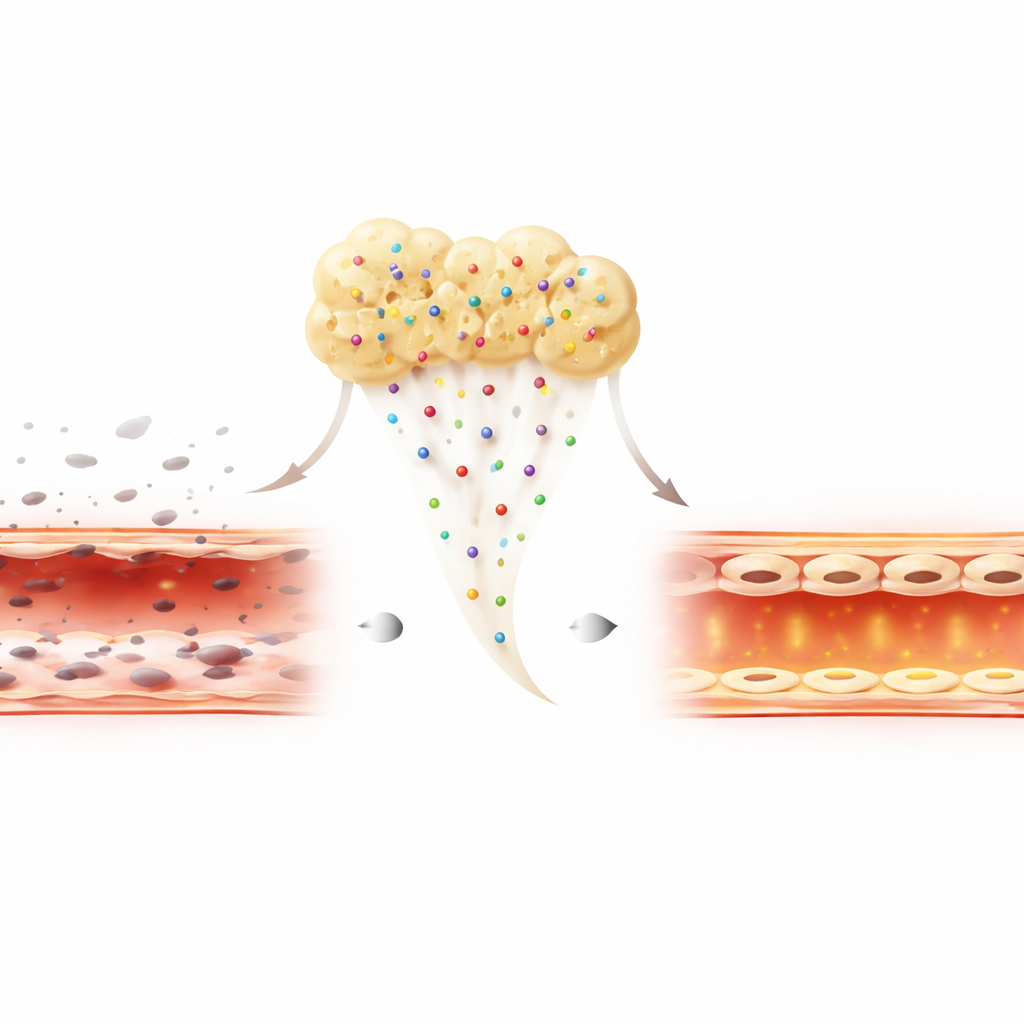
Cosa potrebbe significare per la cura delle ferite in futuro
Nel complesso, i risultati mostrano che Alb-PRF combina la sicurezza dei trattamenti piastrinici esistenti con un supporto più robusto per la crescita, il movimento e la resilienza delle cellule vascolari di fronte all’infiammazione. Sebbene questi test siano stati condotti in provetta e debbano essere confermati in studi su animali e trial clinici, i risultati suggeriscono che Alb-PRF potrebbe diventare un «cerotto biologico» autologo di nuova generazione. Favorendo la ricrescita dei vasi e il loro mantenimento, potrebbe offrire ai pazienti una guarigione delle ferite più rapida e affidabile e migliori risultati in una gamma di terapie rigenerative.
Citazione: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
Parole chiave: guarigione delle ferite, concentrati piastrinici, angiogenesi, medicina rigenerativa, cellule endoteliali