Clear Sky Science · es
Concentrado plaquetario de nueva generación: Alb-PRF superó a PRP y H-PRF en la promoción de la función endotelial y la cicatrización
Por qué importan los apósitos a base de sangre mejorados
Para heridas persistentes—como úlceras diabéticas, sitios quirúrgicos o lesiones de cicatrización lenta—cerrar simplemente la piel no basta. El cuerpo debe reconstruir rápidamente pequeños vasos sanguíneos para llevar oxígeno y nutrientes a la zona dañada. Los médicos ya usan productos a base de sangre preparados a partir de las propias plaquetas del paciente para acelerar este proceso, pero estas mezclas aún se están perfeccionando. Este estudio presenta una nueva versión, llamada Alb-PRF, y muestra que puede superar a productos anteriores al ayudar a las células vasculares a sobrevivir, moverse y reparar el daño, especialmente bajo estrés inflamatorio.
Una nueva variante que utiliza tu propia sangre
El plasma rico en plaquetas (PRP) tradicional se obtiene centrifugando la sangre del paciente para concentrar las plaquetas, que liberan factores de crecimiento que favorecen la curación. Sin embargo, el PRP requiere anticoagulantes y una preparación compleja, y sus beneficios pueden ser de corta duración. Un producto más reciente, el fibrina rica en plaquetas (PRF), evita los anticoagulantes y forma una malla natural que libera factores de crecimiento de forma lenta. A partir de esto, los investigadores desarrollaron Alb-PRF combinando una fracción rica en fibrina de la sangre con albúmina tratada térmicamente procedente del mismo plasma. Esto crea una membrana más estable, similar a un gel, que puede durar más tiempo y potencialmente liberar señales de curación de manera más sostenida, lo que la convierte en un candidato atractivo para la medicina regenerativa.
Cómo se puso a prueba el nuevo material
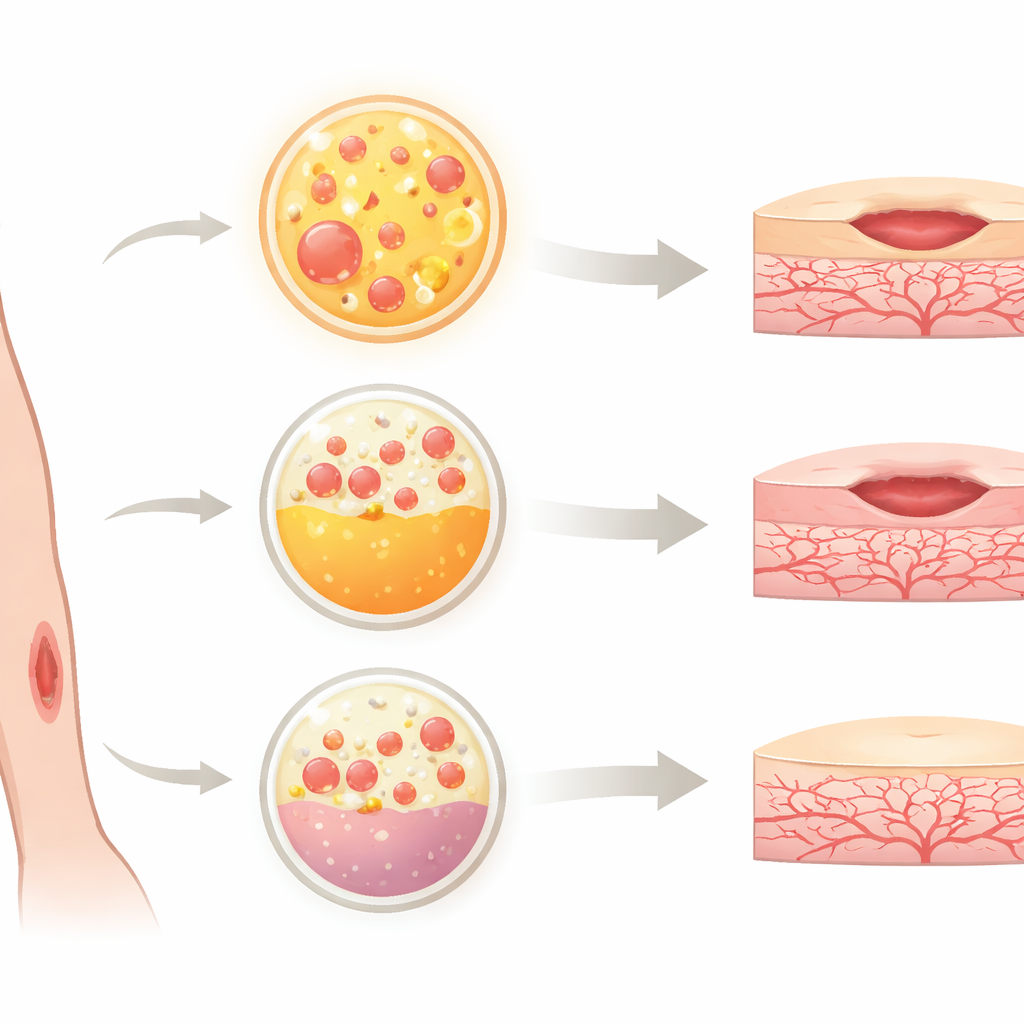
Para comparar Alb-PRF con PRP y con una forma moderna de PRF conocida como PRF horizontal (H-PRF), el equipo usó células que recubren los vasos sanguíneos, las llamadas células endoteliales de la vena umbilical humana. Estas células son un modelo ampliamente utilizado para estudiar el crecimiento y la reparación de vasos. Los investigadores expusieron las células a medios condicionados con cada producto sanguíneo y comprobaron varias características clave: si las células permanecían vivas, la velocidad de proliferación, cómo cambiaba su andamiaje interno y su forma, y qué tan bien migraban para cerrar una “herida” artificial en una placa. También simularon inflamación añadiendo componentes bacterianos que normalmente dañan las células vasculares, y evaluaron qué producto ofrecía la mejor protección.
Favoreciendo el crecimiento y movimiento de las células vasculares
Los tres productos sanguíneos demostraron ser seguros, sin diferencias relevantes en la muerte celular en condiciones normales. Sin embargo, Alb-PRF destacó por el fuerte apoyo al crecimiento celular: las células endoteliales expuestas a Alb-PRF se multiplicaron más que las tratadas con PRP o H-PRF. Al microscopio, las células tratadas con Alb-PRF mostraron formas más alargadas y filamentos internos más densos, signos de que las células estaban organizando activamente su estructura para moverse y reparar. En ensayos tipo “raspado” para simular heridas, Alb-PRF condujo al cierre más rápido de la brecha, con una cobertura casi completa tras doce horas, superando claramente a los otros dos tratamientos. Estos resultados indican que Alb-PRF es un desencadenante particularmente potente de los comportamientos celulares necesarios para reconstruir pequeños vasos sanguíneos.
Protegiendo los vasos sanguíneos del daño inflamatorio
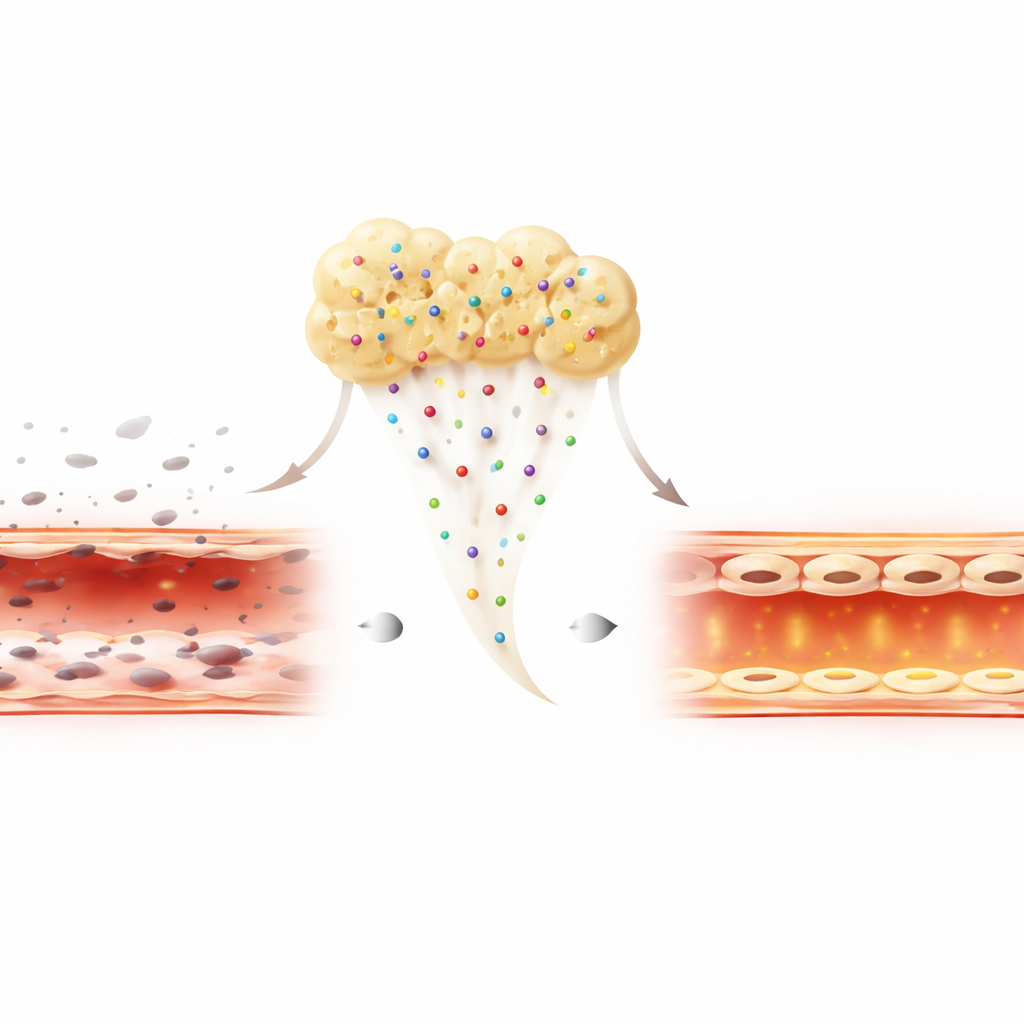
Las heridas en el mundo real a menudo existen en un entorno inflamado y hostil. Para reproducir esto, los investigadores expusieron las células vasculares a una toxina bacteriana que normalmente mata las células y altera su barrera. Bajo este estrés, las tres preparaciones ofrecieron cierta protección, pero H-PRF y especialmente Alb-PRF redujeron drásticamente la muerte celular en comparación con PRP. Las células tratadas con Alb-PRF no solo sobrevivieron mejor, sino que también mostraron niveles más altos de una proteína de superficie clave, CD31, que ayuda a las células vecinas a adherirse y a mantener una pared vascular estrecha y resistente a fugas. Esto sugiere que Alb-PRF hace más que mantener vivas a las células; apoya activamente la reconstrucción de un revestimiento sano y bien sellado incluso cuando hay inflamación.
Qué podría significar esto para el cuidado de heridas en el futuro
En conjunto, los hallazgos muestran que Alb-PRF combina la seguridad de los tratamientos plaquetarios existentes con un apoyo más sólido al crecimiento, movimiento y resistencia de las células vasculares frente a la inflamación. Aunque estas pruebas se realizaron en platos de laboratorio y deberán confirmarse en estudios animales y ensayos clínicos, los resultados sugieren que Alb-PRF podría convertirse en un “apósito biológico” autólogo de nueva generación. Al ayudar a que los vasos se regenere n y se mantengan íntegros, podría ofrecer a los pacientes una cicatrización más rápida y fiable y mejores resultados en una variedad de terapias regenerativas.
Cita: Shen, F., Chai, J., Wei, M. et al. Next-generation platelet concentrate: Alb-PRF outperformed PRP and H-PRF in promoting endothelial function and wound healing. Sci Rep 16, 13934 (2026). https://doi.org/10.1038/s41598-026-44659-2
Palabras clave: cicatrización de heridas, concentrados plaquetarios, angiogénesis, medicina regenerativa, células endoteliales