Clear Sky Science · pt
Modelo de predição precoce de resistência a antibióticos baseado em aprendizado multitarefa usando dados de coorte multiinstitucional
Por que isso importa para os cuidados de saúde do dia a dia
A resistência a antibióticos está silenciosamente transformando infecções antes curáveis em doenças com risco de morte. Médicos muitas vezes precisam escolher antibióticos antes que os testes de laboratório revelem quais drogas funcionarão, um atraso que pode levar vários dias. Este estudo explora como modelos computacionais treinados com registros hospitalares podem dar aos médicos um aviso antecipado sobre quais antibióticos provavelmente falharão, ajudando a proteger os pacientes e a desacelerar a propagação de bactérias resistentes.
Antibióticos sob pressão
A medicina moderna depende fortemente de antibióticos para tudo, desde cirurgias de rotina até cuidados oncológicos. Ainda assim, as bactérias estão evoluindo rapidamente, e novos antibióticos surgem mais devagar do que os antigos perdem eficácia. Na Coreia do Sul, onde este estudo foi realizado, até um terço das prescrições de antibióticos em hospitais é considerado inadequado. Testes de cultura que revelam se um microrganismo é resistente geralmente levam de três a cinco dias, forçando os médicos a tratar no escuro. Os pesquisadores se propuseram a prever a resistência a nove grandes grupos de antibióticos, usando apenas informações disponíveis nas fases iniciais da internação do paciente.
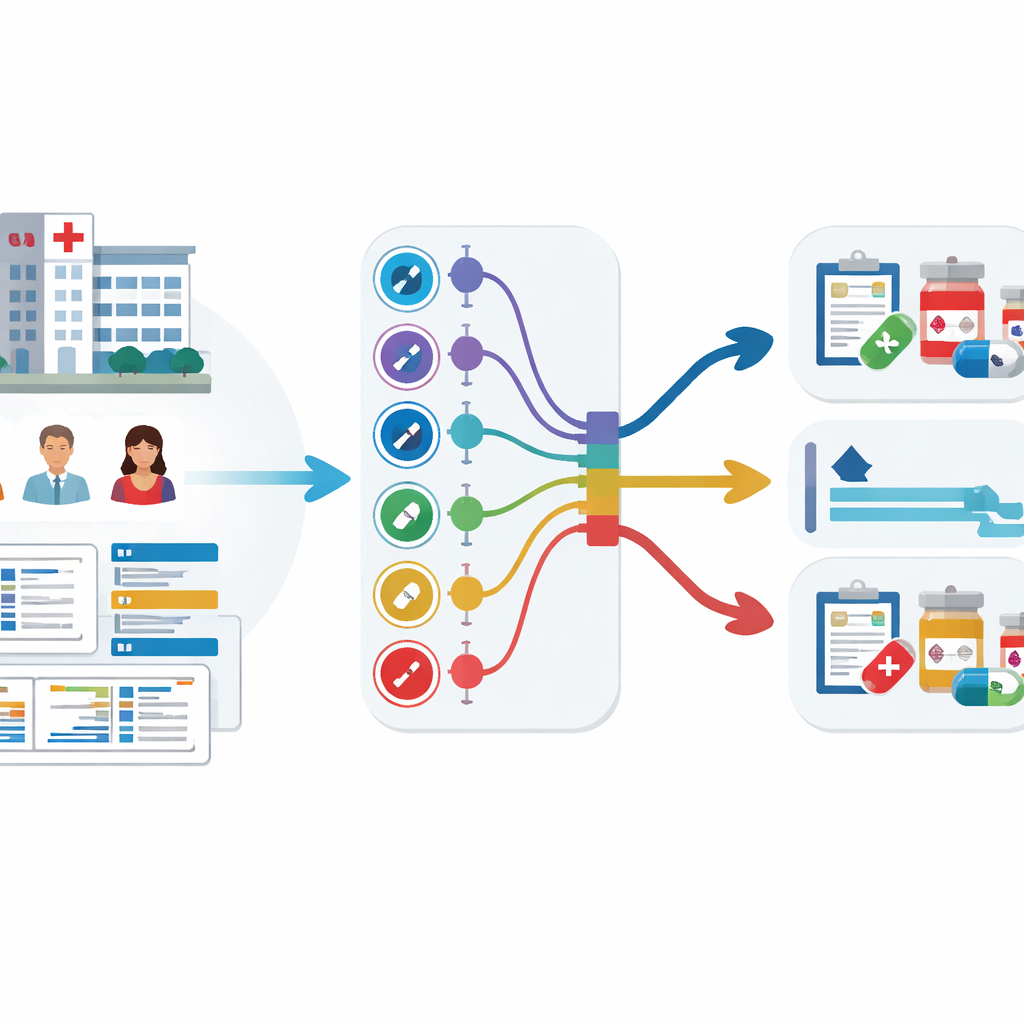
Transformando dados hospitalares em alertas precoces
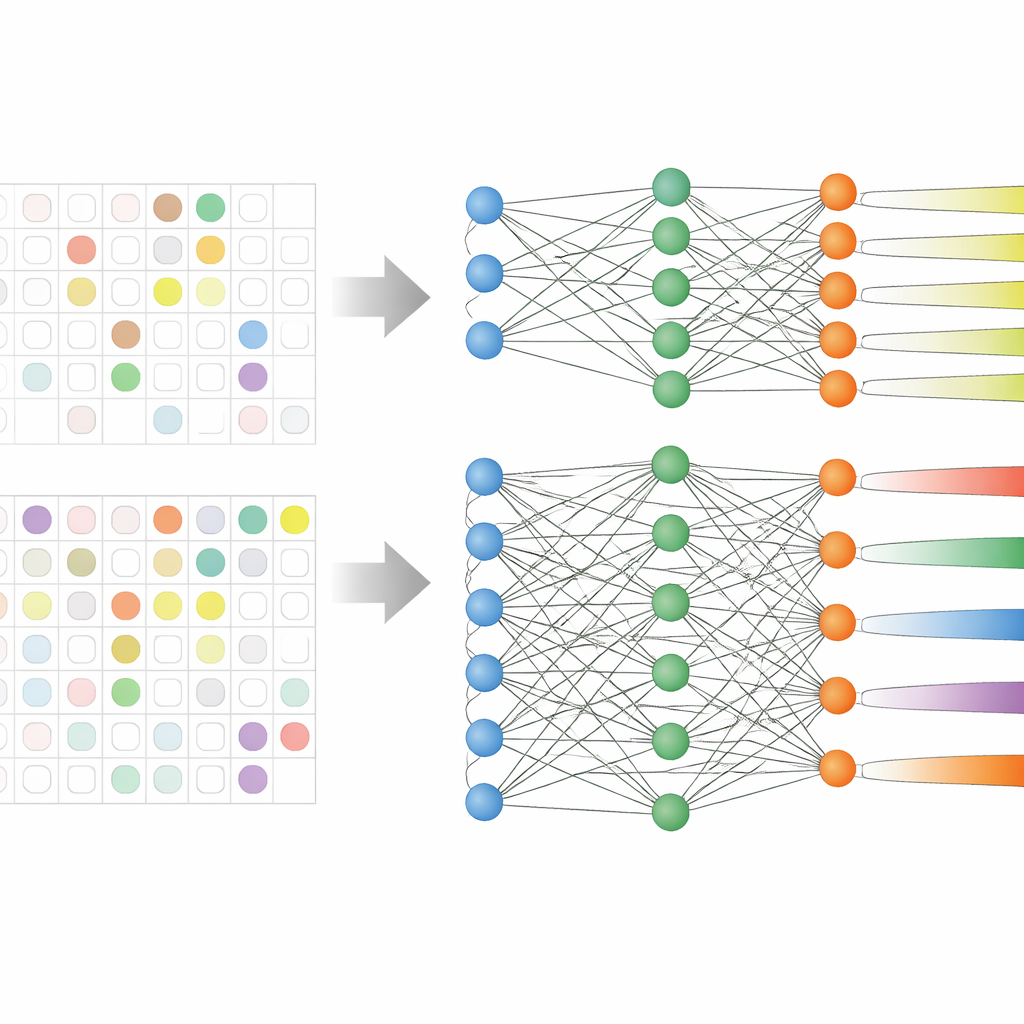
A equipe analisou prontuários eletrônicos de 59.551 pacientes adultos em três grandes hospitais coreanos ao longo de mais de uma década. Esses registros incluíam idade, sinais vitais, tempo de internação, uso prévio de antibióticos e, crucialmente, resultados de culturas anteriores mostrando quais antibióticos já haviam falhado. Em vez de treinar nove modelos separados — um para cada grupo de antibióticos — eles usaram uma estratégia chamada aprendizado multitarefa, que permite a um único modelo aprender várias tarefas de predição relacionadas ao mesmo tempo. Foram testadas duas versões: uma com um núcleo compartilhado que se ramifica em saídas separadas para cada grupo de antibióticos (compartilhamento rígido), e outra em que as tarefas estão ligadas de forma mais frouxa (compartilhamento suave).
Resolvendo o problema de resultados laboratoriais incompletos
Dados hospitalares reais são bagunçados: nem todo paciente é testado contra todo antibiótico. Estudos anteriores frequentemente descartavam esses casos com rótulos parciais, reduzindo seus conjuntos de dados e ignorando padrões que atravessam diferentes drogas. Aqui, os pesquisadores reescreveram a regra de aprendizado do modelo para que ele simplesmente ignore resultados laboratoriais ausentes ao calcular seu erro de treinamento. Isso lhes permitiu manter quase todos os pacientes na análise, mesmo quando alguns resultados de antibióticos estavam ausentes. O modelo de compartilhamento rígido beneficiou-se especialmente dessa abordagem, porque pôde aprender sinais comuns de resistência enquanto ajustava suas predições para cada grupo de drogas.
Quão bem os modelos se saíram?
Quando testados em dados de hospitais que não haviam visto antes, os modelos multitarefa, em geral, superaram métodos mais tradicionais como regressão logística e algoritmos padrão de boosting. Em média, o modelo de compartilhamento rígido mostrou o melhor equilíbrio entre precisão e estabilidade entre as nove classes de antibióticos, sendo particularmente forte para grupos de drogas com os dados mais escassos, como aminoglicosídeos. Uma análise separada que explica quais características impulsionam as predições constatou que a resistência prévia do paciente a um antibiótico foi o fator isolado mais importante, seguida pela resistência ou uso de drogas relacionadas, além de idade e tempo de internação. Análises por subgrupos mostraram que o compartilhamento rígido funcionou melhor quando resultados de cultura anteriores para um determinado antibiótico estavam disponíveis, enquanto o compartilhamento suave foi melhor quando esse histórico estava ausente.
O que isso significa para pacientes e clínicos
O estudo sugere que o uso inteligente de registros hospitalares pode fornecer previsões antecipadas e razoavelmente confiáveis de resistência a antibióticos em várias famílias de drogas importantes. Mesmo ganhos modestos na precisão da predição, aplicados a grande número de pacientes, poderiam ajudar médicos a escolher antibióticos mais estreitos e direcionados mais cedo e a descontinuar drogas de amplo espectro com mais confiança. Isso, por sua vez, pode reduzir complicações, encurtar internações e frear a progressão mais ampla da resistência. Os autores alertam que seu modelo ainda precisa de testes e refinamentos no mundo real, especialmente quando dados de cultura anteriores não estão disponíveis, mas sustentam que o aprendizado multitarefa oferece uma via promissora para usar melhor dados médicos imperfeitos e apoiar um uso mais cuidadoso de antibióticos.
Citação: Kim, Y., Jeong, I., Park, JH. et al. Multi task learning based early prediction model for antibiotic resistance using multi institutional cohort data. Sci Rep 16, 11891 (2026). https://doi.org/10.1038/s41598-026-41185-z
Palavras-chave: resistência a antibióticos, suporte à decisão clínica, prontuários eletrônicos, aprendizado de máquina, aprendizado multitarefa