Clear Sky Science · it
Modello di previsione precoce della resistenza agli antibiotici basato su apprendimento multitask su dati di coorti multi-istituzionali
Perché questo è importante per l'assistenza sanitaria quotidiana
La resistenza agli antibiotici sta silenziosamente trasformando infezioni prima curabili in malattie potenzialmente letali. I medici devono spesso scegliere un antibiotico prima che i test di laboratorio indichino quali farmaci saranno efficaci, un ritardo che può durare diversi giorni. Questo studio esplora come modelli informatici addestrati sui registri ospedalieri possano dare ai clinici un avviso precoce su quali antibiotici sono probabilmente destinati a fallire, aiutando a proteggere i pazienti e a rallentare la diffusione di batteri resistenti.
Antibiotici sotto pressione
La medicina moderna fa ampio affidamento sugli antibiotici, dalla chirurgia di routine alle terapie oncologiche. Eppure i batteri evolvono rapidamente e nuovi antibiotici compaiono più lentamente di quanto quelli vecchi perdano efficacia. In Corea del Sud, dove è stato condotto questo studio, fino a un terzo delle prescrizioni antibiotiche negli ospedali è giudicato inappropriato. I test colturali che rivelano se un germe è resistente richiedono normalmente tre-cinque giorni, costringendo i medici a trattare alla cieca. I ricercatori si sono proposti di prevedere la resistenza a nove principali gruppi di antibiotici, usando solo informazioni disponibili all'inizio del ricovero del paziente.
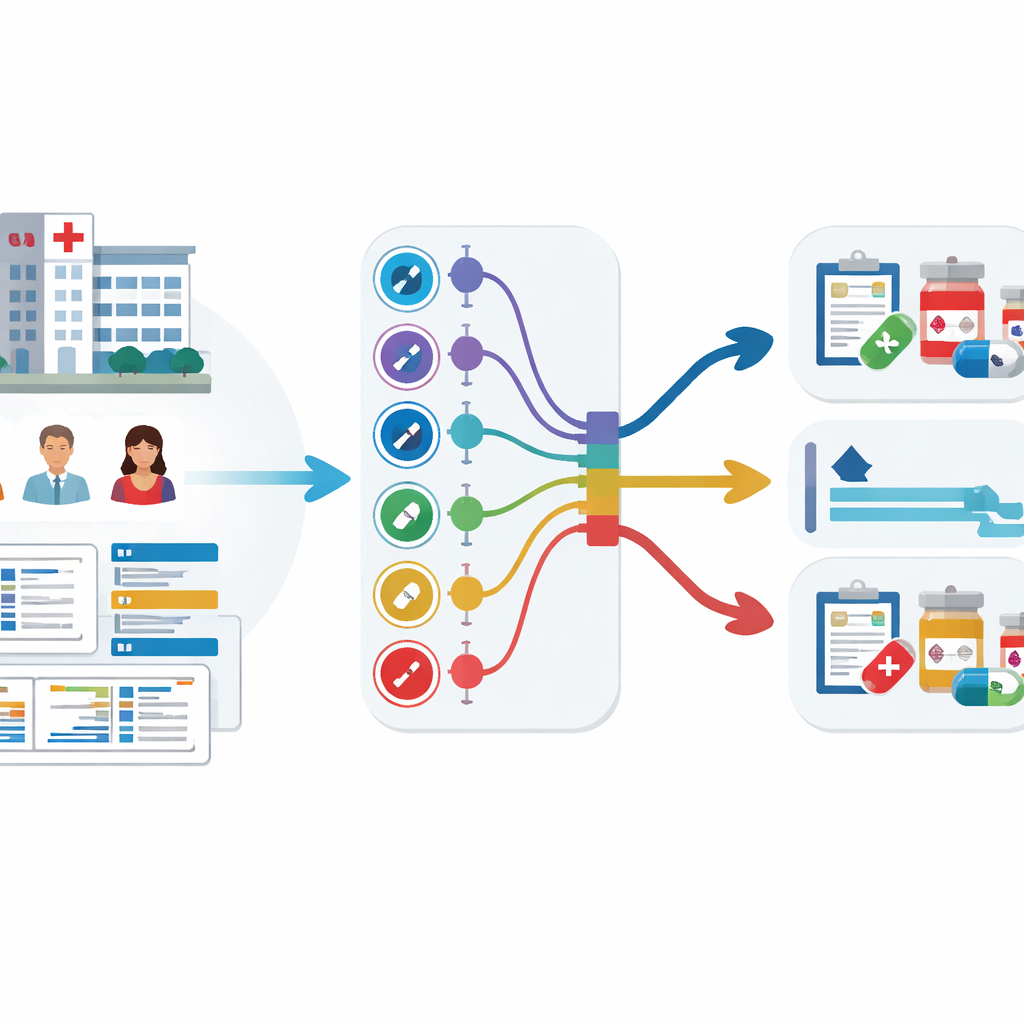
Trasformare i dati ospedalieri in avvisi precoci
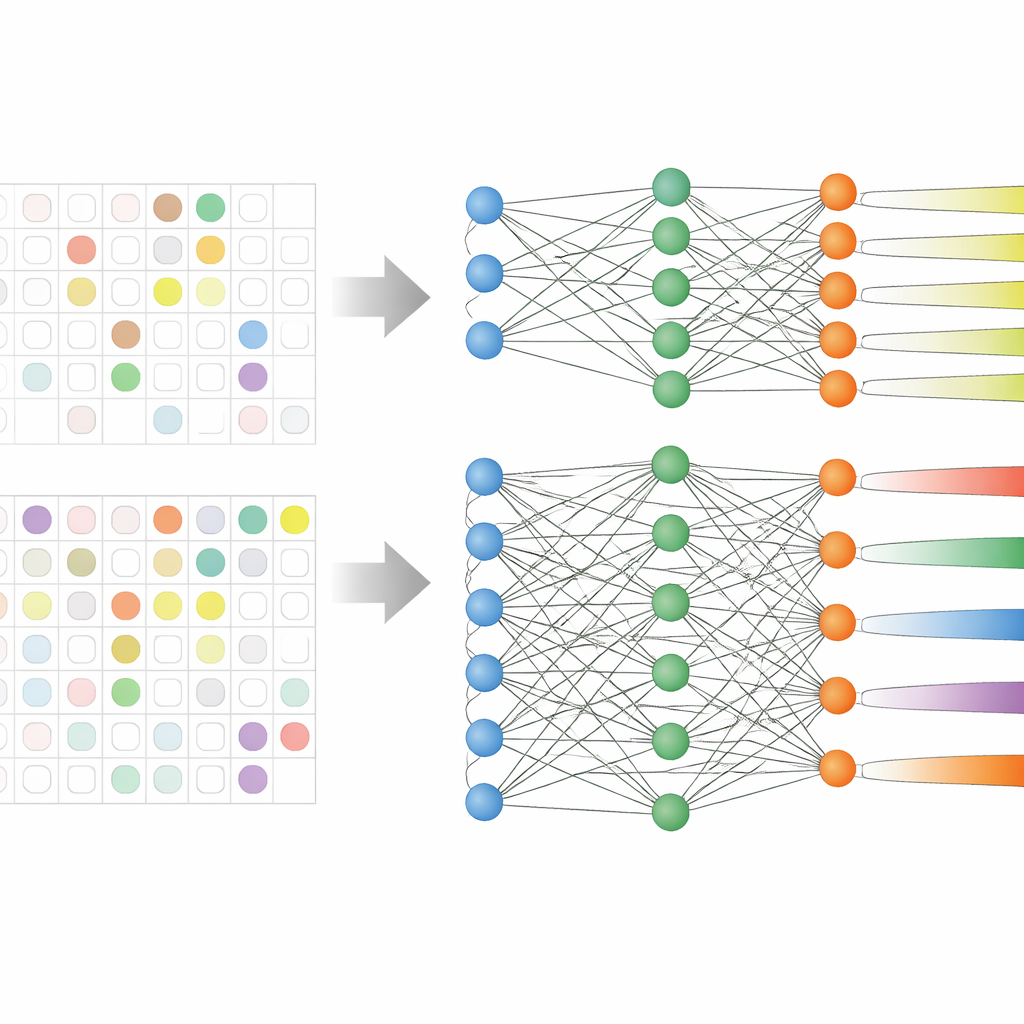
Il team ha analizzato cartelle cliniche elettroniche di 59.551 pazienti adulti in tre grandi ospedali coreani nel corso di più di un decennio. Questi record includevano età, parametri vitali, durata della degenza, uso precedente di antibiotici e, cosa cruciale, risultati di colture precedenti che mostravano quali antibiotici avevano già fallito. Invece di addestrare nove modelli separati — uno per ciascun gruppo di antibiotici — è stata adottata una strategia chiamata apprendimento multitask, che permette a un unico modello di apprendere contemporaneamente diversi compiti di previsione correlati. Sono state testate due versioni: una con un nucleo condiviso che si dirama in uscite separate per ogni gruppo di antibiotici (hard sharing), e una in cui i compiti sono collegati in modo più morbido (soft sharing).
Risolvere il problema dei risultati di laboratorio incompleti
I dati ospedalieri reali sono disordinati: non tutti i pazienti vengono testati contro ogni antibiotico. Studi precedenti spesso scartavano questi casi parzialmente etichettati, riducendo i dataset e ignorando pattern che attraversano diversi farmaci. Qui i ricercatori hanno riscritto la regola di apprendimento del modello in modo che salti semplicemente i risultati di laboratorio mancanti nel calcolo dell'errore di addestramento. Questo ha permesso di mantenere quasi tutti i pazienti nell'analisi, anche quando mancavano alcuni risultati antibiotici. Il modello con hard sharing ha beneficiato in particolare di questa impostazione, perché poteva apprendere segnali comuni di resistenza pur perfezionando le predizioni per ciascun gruppo di farmaci.
Quanto bene hanno funzionato i modelli?
Quando testati su dati provenienti da ospedali non visti durante l'addestramento, i modelli multitask hanno generalmente superato metodi più tradizionali come la regressione logistica e gli algoritmi di boosting standard. In media, il modello con hard sharing ha mostrato il miglior equilibrio tra accuratezza e stabilità attraverso le nove classi di antibiotici, risultando particolarmente efficace per gruppi di farmaci con dati più scarsi, come gli aminoglicosidi. Un'analisi separata che spiega quali caratteristiche guidano le predizioni ha rilevato che la precedente resistenza del paziente a un antibiotico era il singolo fattore più importante, seguita dalla resistenza o dall'uso di farmaci correlati, oltre all'età e alla durata della degenza. Analisi per sottogruppi hanno mostrato che l'hard sharing funzionava meglio quando erano disponibili risultati colturali precedenti per un dato antibiotico, mentre il soft sharing era più efficace quando tale storia mancava.
Cosa significa questo per pazienti e clinici
Lo studio suggerisce che un uso intelligente delle cartelle ospedaliere può fornire previsioni precoci e ragionevolmente affidabili della resistenza agli antibiotici attraverso diverse famiglie di farmaci. Anche miglioramenti modesti nell'accuratezza predittiva, applicati a un grande numero di pazienti, potrebbero aiutare i medici a scegliere più rapidamente antibiotici più mirati e a ridurre con maggiore sicurezza l'uso di farmaci a largo spettro. Ciò potrebbe ridurre le complicanze, accorciare le degenze e rallentare la diffusione della resistenza. Gli autori avvertono che il modello necessita ancora di test e perfezionamenti nel mondo reale, specialmente quando i dati di colture passate non sono disponibili, ma sostengono che l'apprendimento multitask rappresenta una via promettente per sfruttare meglio dati medici imperfetti e sostenere un uso più attento degli antibiotici.
Citazione: Kim, Y., Jeong, I., Park, JH. et al. Multi task learning based early prediction model for antibiotic resistance using multi institutional cohort data. Sci Rep 16, 11891 (2026). https://doi.org/10.1038/s41598-026-41185-z
Parole chiave: resistenza agli antibiotici, supporto decisionale clinico, cartelle cliniche elettroniche, apprendimento automatico, apprendimento multitask