Clear Sky Science · es
Modelo de predicción temprana basado en aprendizaje multitarea para la resistencia a antibióticos usando datos de cohortes multiinstitucionales
Por qué esto importa para la atención sanitaria cotidiana
La resistencia a los antibióticos está convirtiendo silenciosamente infecciones que antes se curaban en enfermedades potencialmente mortales. Los médicos a menudo deben elegir un antibiótico antes de que los análisis de laboratorio indiquen qué fármacos serán eficaces, un retraso que puede durar varios días. Este estudio explora cómo los modelos informáticos entrenados con registros hospitalarios pueden ofrecer a los médicos una alerta temprana sobre qué antibióticos probablemente fracasen, ayudando a proteger a los pacientes y a frenar la propagación de bacterias resistentes.
Antibióticos bajo presión
La medicina moderna depende en gran medida de los antibióticos para todo, desde cirugías rutinarias hasta el tratamiento del cáncer. Sin embargo, las bacterias evolucionan rápidamente y los antibióticos nuevos aparecen más despacio de lo que los antiguos pierden su eficacia. En Corea del Sur, donde se realizó este estudio, hasta un tercio de las prescripciones de antibióticos en hospitales se considera inapropiado. Las pruebas de cultivo que revelan si un germen es resistente suelen tardar de tres a cinco días, obligando a los médicos a tratar a ciegas. Los investigadores se propusieron predecir la resistencia a nueve grupos principales de antibióticos, usando solo la información disponible al inicio de la estancia hospitalaria del paciente.
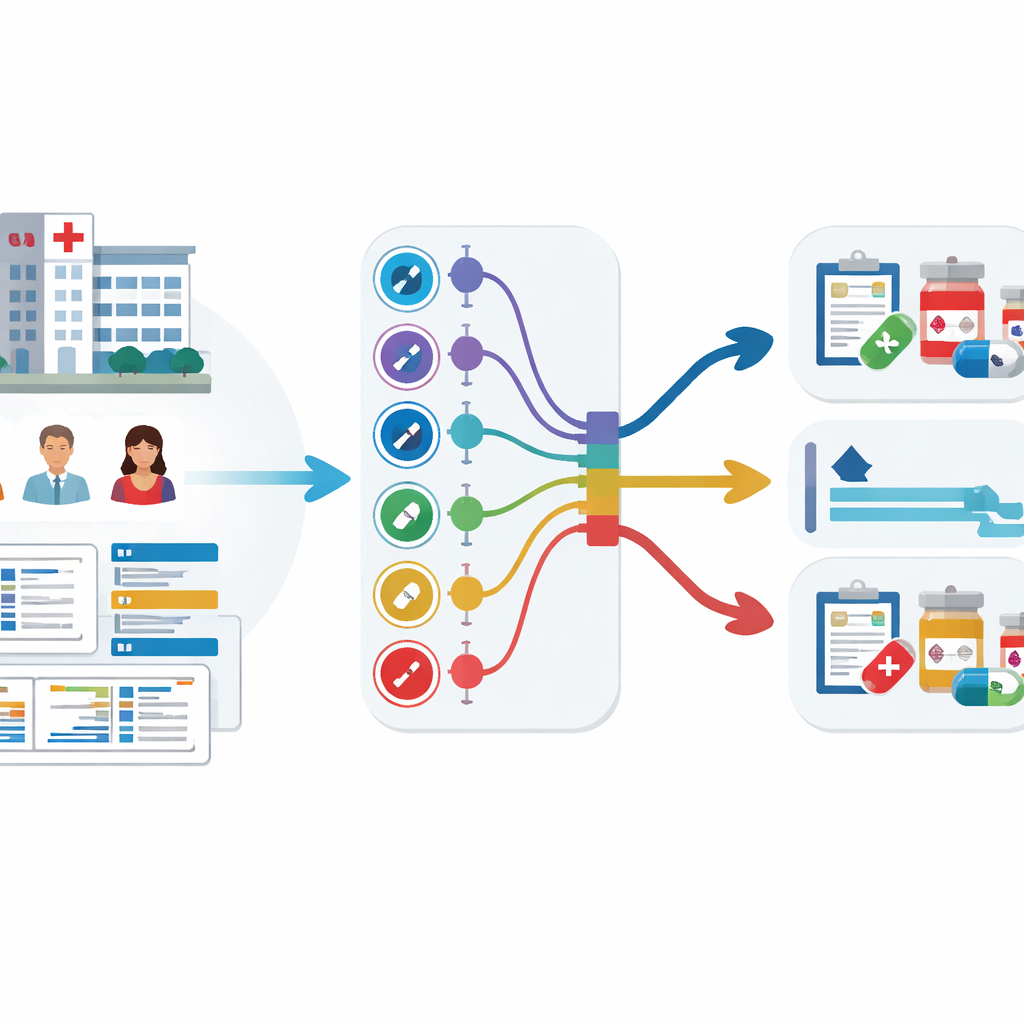
Convertir los datos hospitalarios en alertas tempranas
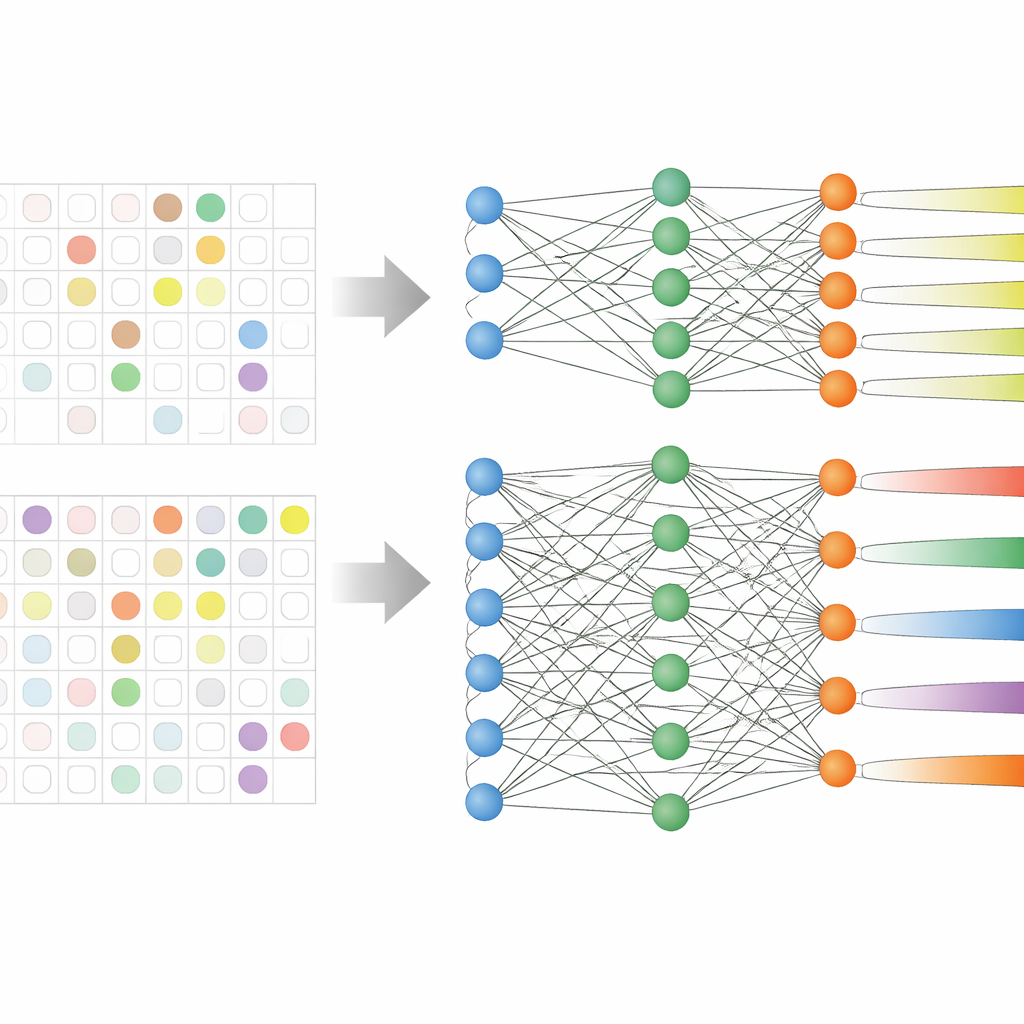
El equipo analizó registros médicos electrónicos de 59.551 pacientes adultos en tres grandes hospitales coreanos durante más de una década. Estos registros incluían edad, signos vitales, tiempo de estancia, uso previo de antibióticos y, crucialmente, resultados de cultivos anteriores que mostraban qué antibióticos ya habían fallado. En lugar de entrenar nueve modelos separados—uno por cada grupo de antibióticos—utilizaron una estrategia llamada aprendizaje multitarea, que permite a un único modelo aprender varias tareas de predicción relacionadas a la vez. Se probaron dos versiones: una con un núcleo compartido que se ramifica en salidas separadas para cada grupo de antibióticos (compartición rígida), y otra en la que las tareas están vinculadas de forma más laxa (compartición flexible).
Resolver el problema de los resultados de laboratorio incompletos
Los datos reales de hospital son desordenados: no a todos los pacientes se les prueba frente a cada antibiótico. Estudios anteriores a menudo descartaban estos casos parcialmente etiquetados, reduciendo sus conjuntos de datos e ignorando patrones que atraviesan diferentes fármacos. Aquí, los investigadores reescribieron la regla de aprendizaje del modelo para que simplemente omita los resultados de laboratorio ausentes al calcular su error de entrenamiento. Esto les permitió mantener casi a todos los pacientes en el análisis, incluso cuando faltaban algunos resultados antibióticos. El modelo de compartición rígida se benefició especialmente de esta configuración, porque pudo aprender señales comunes de resistencia a la vez que afinaba sus predicciones para cada grupo de fármacos.
¿Qué rendimiento alcanzaron los modelos?
Cuando se evaluaron con datos de hospitales que no habían visto antes, los modelos multitarea generalmente superaron a métodos más tradicionales como la regresión logística y algoritmos de boosting estándar. En promedio, el modelo de compartición rígida mostró el mejor equilibrio entre precisión y estabilidad a través de las nueve clases de antibióticos, y fue particularmente fuerte para grupos de fármacos con los datos más escasos, como los aminoglucósidos. Un análisis separado que explica qué características impulsan las predicciones encontró que la resistencia previa del paciente a un antibiótico fue el factor más importante, seguido por la resistencia o el uso de fármacos relacionados, así como la edad y la duración de la estancia. Los análisis por subgrupos mostraron que la compartición rígida funcionó mejor cuando había resultados de cultivo previos para un antibiótico dado, mientras que la compartición flexible fue superior cuando faltaba ese historial.
Qué significa esto para pacientes y clínicos
El estudio sugiere que un uso inteligente de los registros hospitalarios puede ofrecer pronósticos tempranos y razonablemente fiables de la resistencia a antibióticos en varias familias farmacológicas importantes. Incluso pequeñas mejoras en la precisión de la predicción, aplicadas a grandes volúmenes de pacientes, podrían ayudar a los médicos a elegir antibióticos más específicos y estrechos antes y a reducir con más confianza el uso de fármacos de amplio espectro. Esto, a su vez, puede disminuir complicaciones, acortar estancias hospitalarias y frenar el avance general de la resistencia. Los autores advierten que su modelo aún necesita pruebas y refinamiento en el mundo real, especialmente cuando no hay datos de cultivos previos, pero sostienen que el aprendizaje multitarea ofrece una vía prometedora para aprovechar mejor datos médicos imperfectos y apoyar un uso más prudente de los antibióticos.
Cita: Kim, Y., Jeong, I., Park, JH. et al. Multi task learning based early prediction model for antibiotic resistance using multi institutional cohort data. Sci Rep 16, 11891 (2026). https://doi.org/10.1038/s41598-026-41185-z
Palabras clave: resistencia a antibióticos, soporte a la decisión clínica, historiales clínicos electrónicos, aprendizaje automático, aprendizaje multitarea