Clear Sky Science · pt
O papel e o mecanismo regulatório da USP25 na perturbação microcirculatória pancreática na pancreatite aguda grave
Por que os vasos sanguíneos minúsculos do pâncreas importam
A pancreatite aguda grave é um ataque súbito ao pâncreas que pode rapidamente tornar-se uma condição com risco de vida. Nos piores casos, não apenas as células digestivas do órgão morrem, mas os menores vasos sanguíneos que irrigam o pâncreas também entopem e colapsam, privando o tecido de oxigênio. Este estudo faz uma pergunta prática com grandes implicações: quais interruptores moleculares fazem esses microvasos falharem e desligar um deles pode proteger o pâncreas?
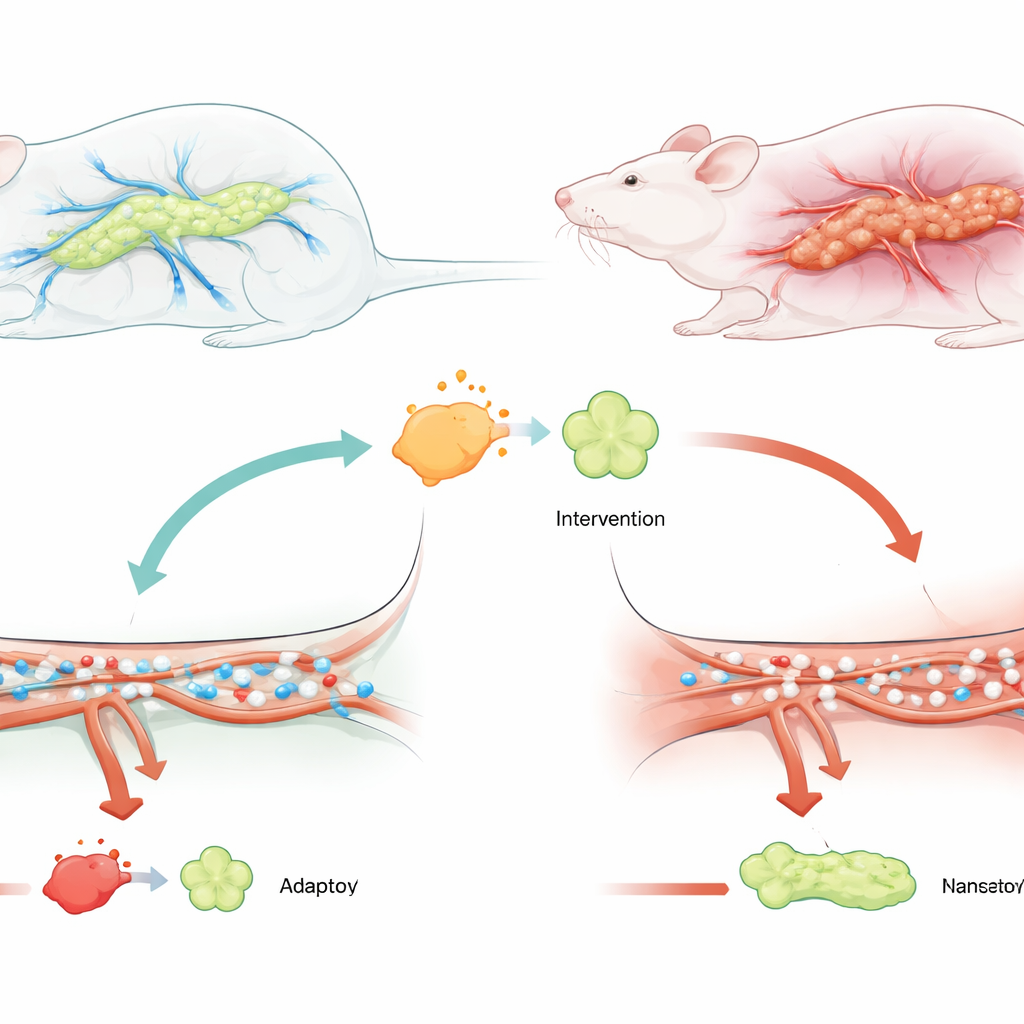
Um olhar mais atento sobre um surto perigoso
Os autores concentraram-se em uma forma grave da doença chamada pancreatite aguda grave, na qual os pacientes frequentemente vão para a unidade de terapia intensiva e enfrentam alto risco de falência de órgãos. Trabalhos anteriores haviam mostrado que a proteína USP25 está aumentada em pessoas e modelos animais com pancreatite e que ela pode alimentar a chama da inflamação. Ao mesmo tempo, outra proteína, TRAF6, é conhecida como um centro chave que retransmite sinais de estresse e perigo dentro de células imunes e do tecido. Como ambas as moléculas estão envolvidas no dano inflamatório, a equipe suspeitou que a USP25 poderia estar agravando problemas de fluxo sanguíneo no pâncreas agindo por meio da TRAF6.
Modelos animais revelam uma parceria prejudicial
Para testar essa ideia, os pesquisadores usaram ratos nos quais a pancreatite grave foi desencadeada pela injeção de um sal biliar no ducto pancreático, um modelo amplamente usado da doença. Alguns ratos receberam um vírus que reduziu os níveis de USP25 no pâncreas antes do surto. Em comparação com os animais não tratados, os ratos com USP25 reduzida apresentaram marcadores sanguíneos de lesão pancreática muito mais baixos, tecido pancreático com aparência mais saudável ao microscópio e muito menos sinais de inchaço, sangramento e morte celular. Importante, as medidas da microcirculação mostraram que os glóbulos vermelhos nos ratos tratados fluíam mais rápido e por mais pequenos vasos, o que significa que os piores bloqueios no fluxo sanguíneo haviam diminuído.
Como o interruptor molecular funciona dentro das células
A equipe então ampliou o foco para as células acinares pancreáticas individuais, as máquinas produtoras de enzimas do órgão. Em células acinares de rato em cultura expostas a um composto que desencadeia pancreatite, os níveis de USP25 dispararam, a sobrevivência celular caiu e mais células morreram. Quando a USP25 foi silenciada, as células tinham maior probabilidade de sobreviver e liberaram menos substâncias inflamatórias. Testes bioquímicos mostraram que a USP25 se liga fisicamente à TRAF6 e a protege de ser marcada para destruição pelo sistema de reciclagem proteica da célula. Como resultado, a TRAF6 se acumula e mantém os sinais inflamatórios ligados. Quando a USP25 foi bloqueada, a TRAF6 ficou mais fortemente marcada para degradação, seus níveis caíram e a sinalização prejudicial se acalmou.
Provando que TRAF6 é o intermediário chave
Para garantir que a TRAF6 fosse o intermediário crucial, os cientistas aumentaram artificialmente os níveis de TRAF6 mesmo enquanto a USP25 estava sendo bloqueada. Em células, esse excesso de TRAF6 eliminou grande parte da proteção conferida pela inibição da USP25: mais células morreram e as substâncias inflamatórias aumentaram novamente. Em ratos, elevar a TRAF6 igualmente minou os benefícios de reduzir a USP25. O fluxo sanguíneo nos microvasos piorou, os marcadores químicos de constrição vascular e estresse oxidativo aumentaram, e o dano ao tecido pancreático se intensificou. Esses experimentos de resgate sustentam uma cadeia de eventos simples: a USP25 preserva a TRAF6, a TRAF6 impulsiona a inflamação, e essa inflamação obstrui a microcirculação pancreática.
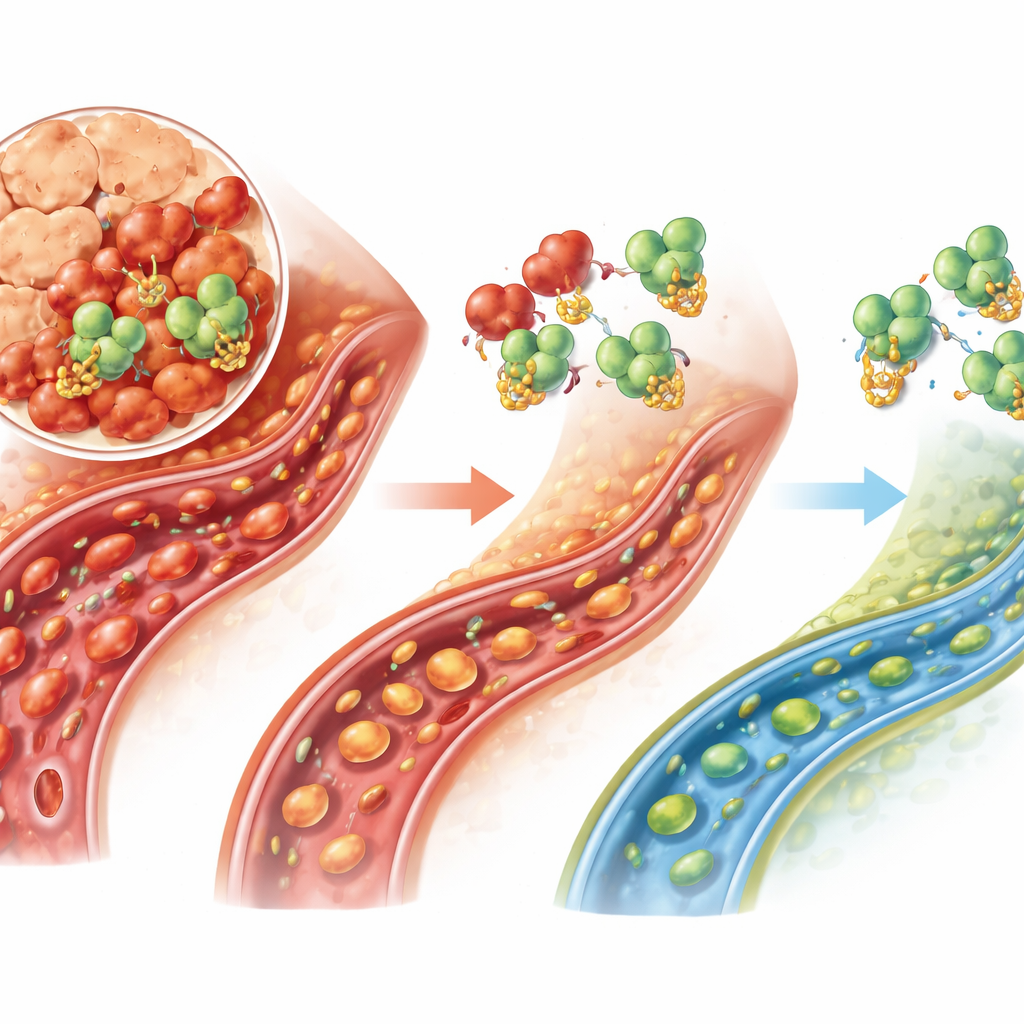
O que isso pode significar para tratamentos futuros
Para pessoas que enfrentam pancreatite aguda grave hoje, o cuidado é em grande parte de suporte — fluidos, nutrição e alívio da dor — porque nenhum medicamento interrompe diretamente a cascata da doença. Este estudo identifica um eixo molecular específico, USP25 atuando via TRAF6, que parece agravar a falha dos pequenos vasos e a morte celular no pâncreas. Embora o trabalho seja pré-clínico e baseado principalmente em um modelo animal e em uma linhagem celular de rato, ele aponta a USP25 como um alvo promissor: bloquear essa enzima poderia permitir ao organismo desmontar a TRAF6, reduzir a inflamação e manter o fluxo sanguíneo pelo pâncreas quando ele estiver mais em risco.
Citação: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
Palavras-chave: pancreatite aguda grave, microcirculação pancreática, USP25, TRAF6, inflamação