Clear Sky Science · de
Die Rolle und der Regulationsmechanismus von USP25 bei der Störung der mikro‑Zirkulation des Pankreas bei schwerer akuter Pankreatitis
Warum winzige Blutgefäße in der Bauchspeicheldrüse wichtig sind
Die schwere akute Pankreatitis ist ein plötzlicher Angriff auf die Bauchspeicheldrüse, der sich rasch lebensbedrohlich entwickeln kann. In den schlimmsten Fällen sterben nicht nur die Verdauungszellen des Organs, sondern auch die kleinsten Blutgefäße, die die Bauchspeicheldrüse versorgen, verstopfen und kollabieren, wodurch das Gewebe von Sauerstoff abgeschnitten wird. Diese Studie stellt eine praxisrelevante Frage mit großen Konsequenzen: Welche molekularen Schalter lassen diese Mikrogefäße versagen, und kann das Abschalten eines davon die Bauchspeicheldrüse schützen?
Ein genauerer Blick auf einen gefährlichen Ausbruch
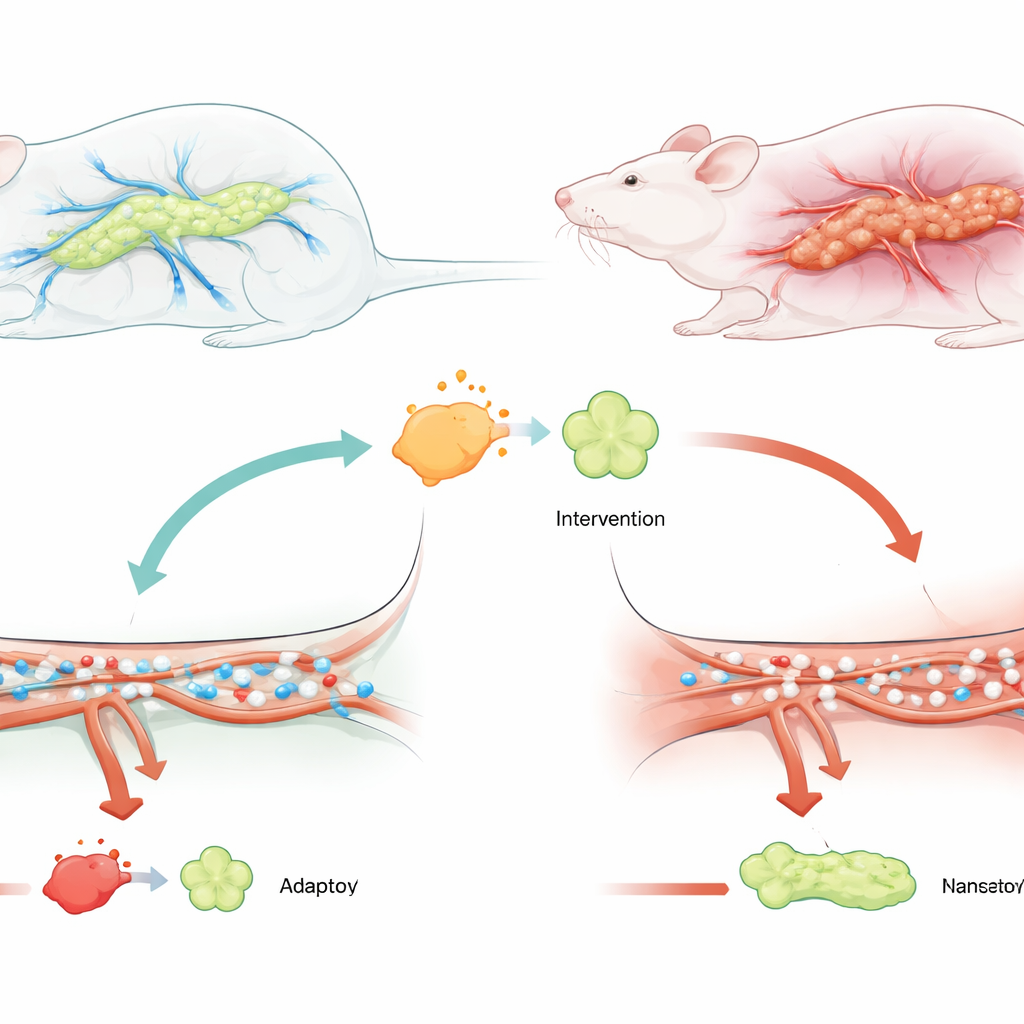
Die Autorinnen und Autoren konzentrierten sich auf eine schwere Form der Erkrankung, die als schwere akute Pankreatitis bezeichnet wird, bei der Patienten häufig auf der Intensivstation landen und ein hohes Risiko für Organversagen haben. Frühere Arbeiten hatten gezeigt, dass das Protein USP25 bei Menschen und Tiermodellen mit Pankreatitis erhöht ist und die Entzündung anheizen kann. Gleichzeitig ist ein anderes Protein, TRAF6, als zentraler Knotenpunkt bekannt, der Stress‑ und Gefahrensignale in Immun‑ und Gewebezellen weiterleitet. Da beide Moleküle an entzündlichen Schäden beteiligt sind, vermutete das Team, dass USP25 die Durchblutungsprobleme im Pankreas über TRAF6 verschlechtern könnte.
Tiermodelle zeigen eine schädliche Partnerschaft
Um diese Idee zu testen, verwendeten die Forschenden Ratten, bei denen eine schwere Pankreatitis durch Injektion eines Gallensalzes in den Pankreasgang ausgelöst wurde — ein weithin genutztes Modell der Erkrankung. Einige Ratten erhielten vor dem Ausbruch ein Virus, das die USP25‑Spiegel im Pankreas senkte. Im Vergleich zu unbehandelten Tieren wiesen Ratten mit reduziertem USP25 deutlich niedrigere Blutmarker für Pankreasschäden, unter dem Mikroskop gesünder aussehendes Pankreasgewebe und weit weniger Anzeichen von Schwellung, Blutungen und Zelltod auf. Wichtig war, dass Messungen der Mikrozirkulation zeigten, dass rote Blutkörperchen in behandelten Ratten schneller und durch mehr winzige Gefäße flossen, was bedeutet, dass die schlimmsten Durchblutungsblockaden sich verminderten.
Wie der molekulare Schalter in Zellen wirkt
Das Team zoomte dann auf einzelne pankreatische Azinuszellen, die enzymproduzierenden Arbeitspferde des Organs. In kultivierten Ratten‑Azinuszellen, die einer pankreatitisauslösenden Verbindung ausgesetzt wurden, stieg USP25 an, die Zellerhaltung nahm ab und mehr Zellen starben. Wenn USP25 ausgeschaltet wurde, überlebten mehr Zellen und es wurden weniger entzündliche Substanzen freigesetzt. Biochemische Tests zeigten, dass USP25 physisch an TRAF6 bindet und es davor schützt, von dem zellulären Proteinfördersystem für den Abbau markiert zu werden. Infolgedessen reichert sich TRAF6 an und hält die Entzündungssignale aktiviert. Wurde USP25 blockiert, wurde TRAF6 stärker für den Abbau markiert, seine Spiegel sanken und die schädliche Signalübertragung beruhigte sich.
Der Nachweis, dass TRAF6 der entscheidende Mittelsmann ist
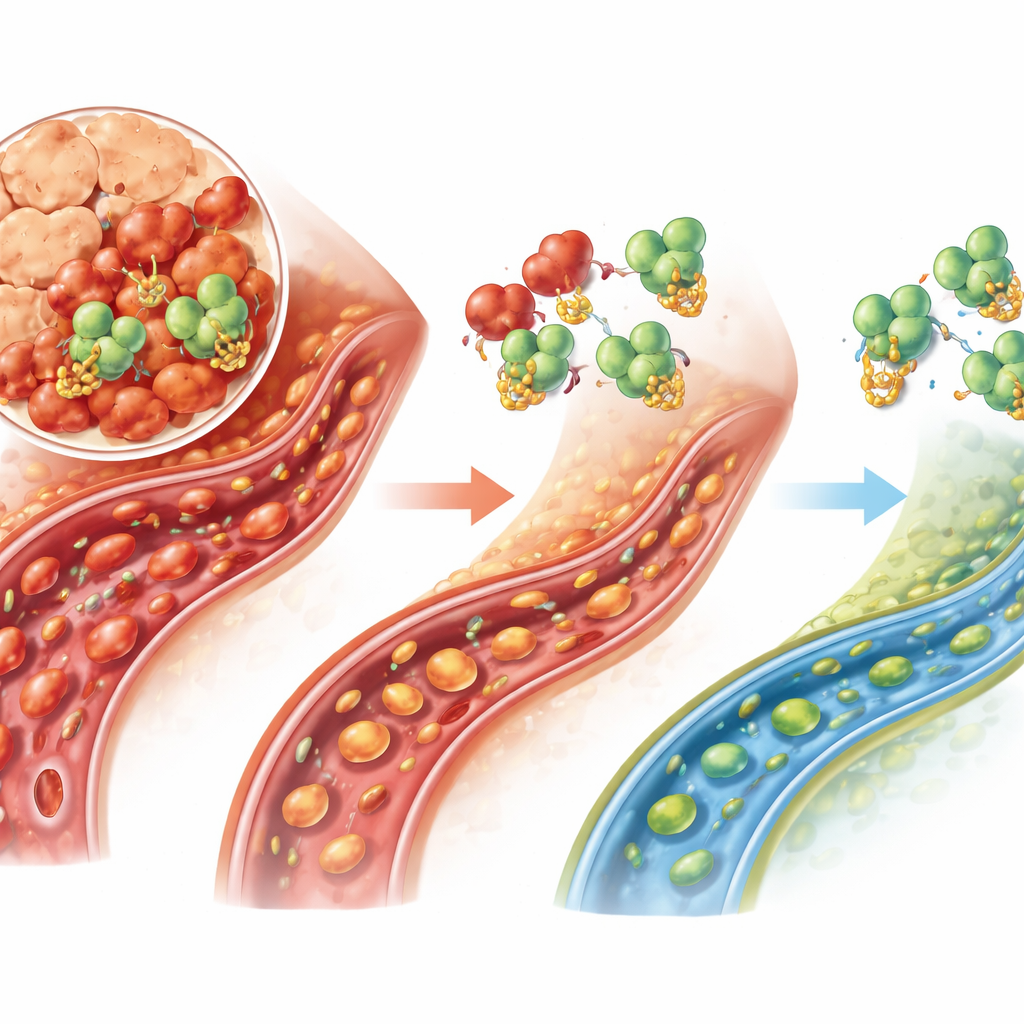
Um sicherzustellen, dass TRAF6 der wesentliche Vermittler ist, erhöhten die Wissenschaftlerinnen und Wissenschaftler künstlich die TRAF6‑Spiegel, während USP25 gleichzeitig blockiert war. In Zellen hob dieses zusätzliche TRAF6 einen Großteil des Schutzes durch die USP25‑Hemmung auf: Mehr Zellen starben und die entzündlichen Substanzen stiegen wieder an. Bei Ratten untergrub die Erhöhung von TRAF6 ebenso die Vorteile der USP25‑Senkung. Der Blutfluss durch Mikrogefäße verschlechterte sich, chemische Marker für Gefäßverengung und oxidativen Stress nahmen zu und die Schädigung des Pankreasgewebes nahm zu. Diese sogenannten Rescue‑Experimente stützen eine einfache Ereigniskette: USP25 bewahrt TRAF6, TRAF6 treibt Entzündung an, und diese Entzündung erstickt die pankreatische Mikrozirkulation.
Was das für künftige Behandlungen bedeuten könnte
Für Menschen mit schwerer akuter Pankreatitis ist die Behandlung heute weitgehend unterstützend — Flüssigkeiten, Ernährung und Schmerzbekämpfung —, weil kein Medikament die Krankheitskaskade direkt stoppt. Diese Studie identifiziert eine spezifische molekulare Achse, USP25 in Verbindung mit TRAF6, die offenbar das Versagen winziger Gefäße und den Zelltod im Pankreas verschlimmert. Obwohl die Arbeit präklinisch ist und hauptsächlich auf einem Tiermodell und einer Rattenzelllinie basiert, weist sie auf USP25 als vielversprechendes Ziel hin: Die Blockade dieses Enzyms könnte dem Körper ermöglichen, TRAF6 abzubauen, die Entzündung zu dämpfen und den Blutfluss durch die Bauchspeicheldrüse in besonders gefährdeten Phasen aufrechtzuerhalten.
Zitation: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
Schlüsselwörter: schwere akute Pankreatitis, pankreatische Mikrozirkulation, USP25, TRAF6, Entzündung