Clear Sky Science · it
Il ruolo e il meccanismo regolatorio di USP25 nel disturbo microcircolatorio pancreatico nella pancreatite acuta grave
Perché i minuscoli vasi sanguigni del pancreas sono importanti
La pancreatite acuta grave è un attacco improvviso al pancreas che può rapidamente diventare pericoloso per la vita. Nei casi più gravi non muoiono soltanto le cellule digestive dell’organo, ma anche i vasi sanguigni più piccoli che lo irrorano si intasano e collassano, privando il tessuto di ossigeno. Questo studio pone una domanda pratica dalle grandi implicazioni: quali interruttori molecolari fanno fallire questi microvasi e spegnere uno di essi può proteggere il pancreas?
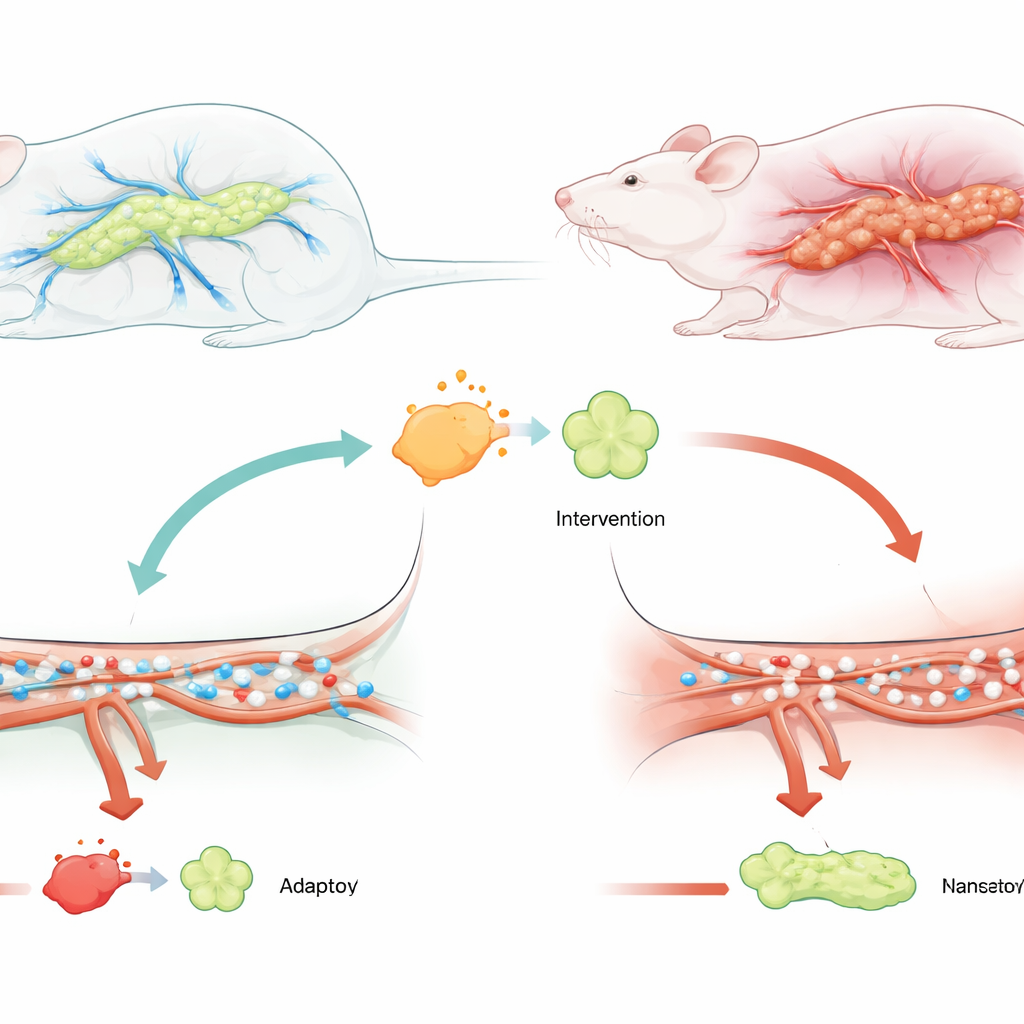
Uno sguardo più ravvicinato a una riacutizzazione pericolosa
Gli autori si sono concentrati su una forma grave della malattia chiamata pancreatite acuta grave, nella quale i pazienti spesso finiscono in terapia intensiva e corrono un alto rischio di insufficienza d’organo. Lavori precedenti avevano mostrato che la proteina USP25 è più elevata nelle persone e nei modelli animali con pancreatite e che può alimentare l’infiammazione. Allo stesso tempo, un’altra proteina, TRAF6, è nota come un nodo chiave che trasmette segnali di stress e di pericolo all’interno delle cellule immunitarie e tessutali. Poiché entrambe le molecole sono coinvolte nel danno infiammatorio, il gruppo ha ipotizzato che USP25 potesse peggiorare i problemi di flusso sanguigno nel pancreas agendo tramite TRAF6.
I modelli animali rivelano una collaborazione dannosa
Per mettere alla prova questa idea, i ricercatori hanno utilizzato ratti in cui la pancreatite grave è stata indotta iniettando un sale biliare nel dotto pancreatico, un modello ampiamente usato della malattia. Alcuni ratti hanno ricevuto un virus che abbassava i livelli di USP25 nel pancreas prima dell’attacco. Rispetto agli animali non trattati, i ratti con USP25 ridotto avevano marcatori ematici di danno pancreatico molto più bassi, tessuto pancreatico dall’aspetto più sano al microscopio e molte meno evidenze di edema, sanguinamento e morte cellulare. Importante, le misurazioni della microcircolazione hanno mostrato che i globuli rossi nei ratti trattati scorrevano più velocemente e attraverso più vasi sottili, il che significa che i peggiori blocchi del flusso sanguigno si erano attenuati.
Come funziona l’interruttore molecolare all’interno delle cellule
Il gruppo ha quindi esaminato più da vicino le singole cellule acinari pancreatiche, le produttrici di enzimi dell’organo. In colture di cellule acinari di ratto esposte a un composto che scatena la pancreatite, i livelli di USP25 sono aumentati, la sopravvivenza cellulare è diminuita e più cellule sono morte. Quando USP25 è stato silenziato, le cellule avevano maggiori probabilità di sopravvivere e rilasciavano meno sostanze infiammatorie. Test biochimici hanno mostrato che USP25 si lega fisicamente a TRAF6 e lo protegge dall’essere contrassegnato per la distruzione dal sistema di riciclo proteico della cellula. Di conseguenza, TRAF6 si accumula e mantiene attivi i segnali infiammatori. Quando USP25 è stato bloccato, TRAF6 è stato più pesantemente etichettato per la degradazione, i suoi livelli sono diminuiti e la segnalazione dannosa si è attenuata.
Dimostrare che TRAF6 è il mediatore cruciale
Per essere sicuri che TRAF6 fosse l’anello intermedio cruciale, gli scienziati hanno aumentato artificialmente i livelli di TRAF6 anche mentre USP25 era bloccato. Nelle cellule, questo TRAF6 in eccesso ha annullato gran parte della protezione conferita dall’inibizione di USP25: più cellule sono morte e le sostanze infiammatorie sono aumentate di nuovo. Nei ratti, l’aumento di TRAF6 ha analogamente compromesso i benefici della riduzione di USP25. Il flusso sanguigno nei microvasi è peggiorato, sono aumentati i marcatori chimici di costrizione vascolare e stress ossidativo e il danno al tessuto pancreatico si è intensificato. Questi esperimenti di “salvataggio” supportano una catena di eventi semplice: USP25 preserva TRAF6, TRAF6 guida l’infiammazione e quell’infiammazione soffoca la microcircolazione pancreatica.
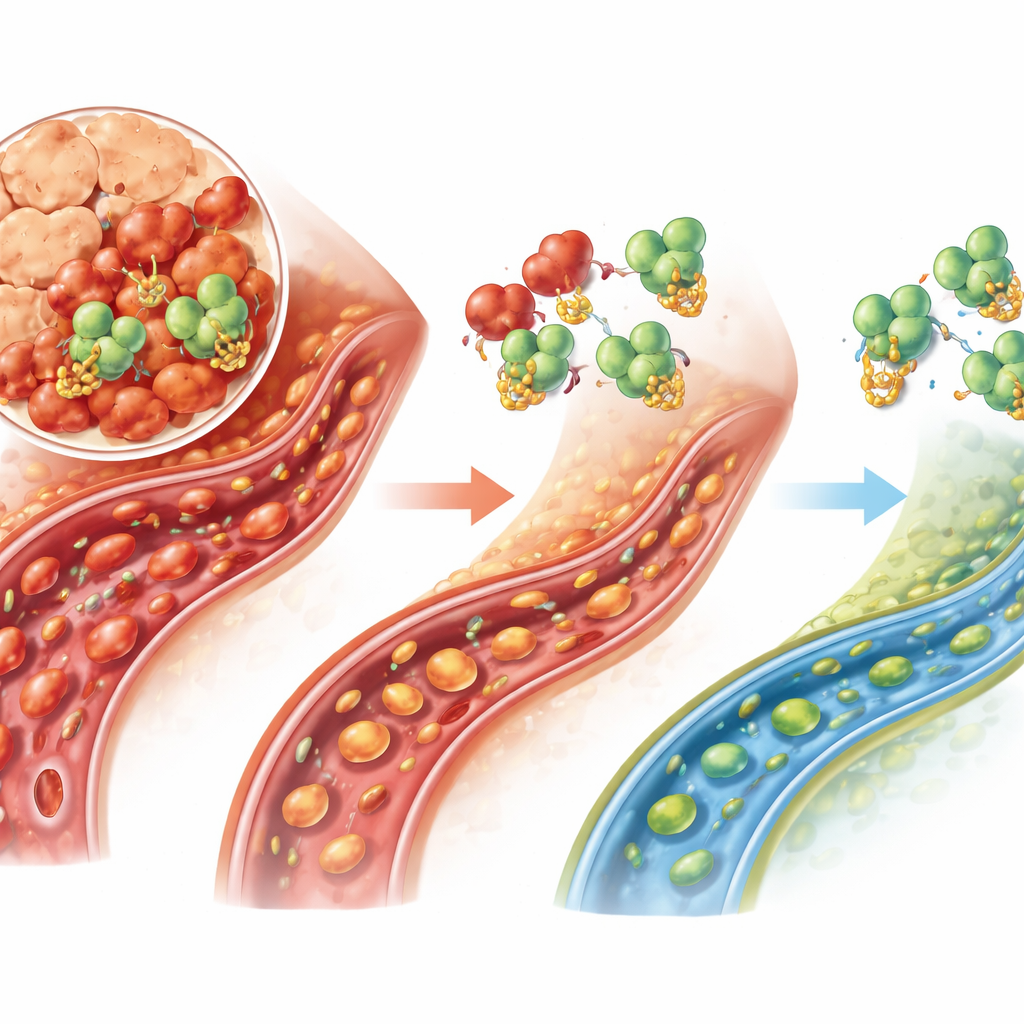
Cosa potrebbe significare per i trattamenti futuri
Per le persone che oggi affrontano la pancreatite acuta grave, le cure sono per lo più di supporto—fluidi, nutrizione e analgesia—perché non esiste un farmaco che interrompa direttamente la cascata della malattia. Questo studio identifica un asse molecolare specifico, USP25 che agisce tramite TRAF6, che sembra peggiorare il fallimento dei microvasi e la morte cellulare nel pancreas. Pur essendo lavoro preclinico e basato principalmente su un modello animale e su una linea cellulare di ratto, indica USP25 come un bersaglio promettente: bloccare questo enzima potrebbe permettere all’organismo di smantellare TRAF6, ridurre l’infiammazione e mantenere il flusso sanguigno attraverso il pancreas quando è più a rischio.
Citazione: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
Parole chiave: pancreatite acuta grave, microcircolazione pancreatica, USP25, TRAF6, infiammazione