Clear Sky Science · es
El papel y el mecanismo regulador de USP25 en la alteración microcirculatoria pancreática en la pancreatitis aguda grave
Por qué importan los vasos sanguíneos diminutos del páncreas
La pancreatitis aguda grave es un ataque repentino al páncreas que puede volverse rápidamente potencialmente mortal. En los peores casos, no solo mueren las células digestivas del órgano, sino que los vasos sanguíneos más pequeños que lo nutren también se obstruyen y colapsan, privando al tejido de oxígeno. Este estudio plantea una pregunta práctica con grandes implicaciones: ¿qué interruptores moleculares hacen que fallen estos microvasos, y puede la desactivación de uno de ellos proteger al páncreas?
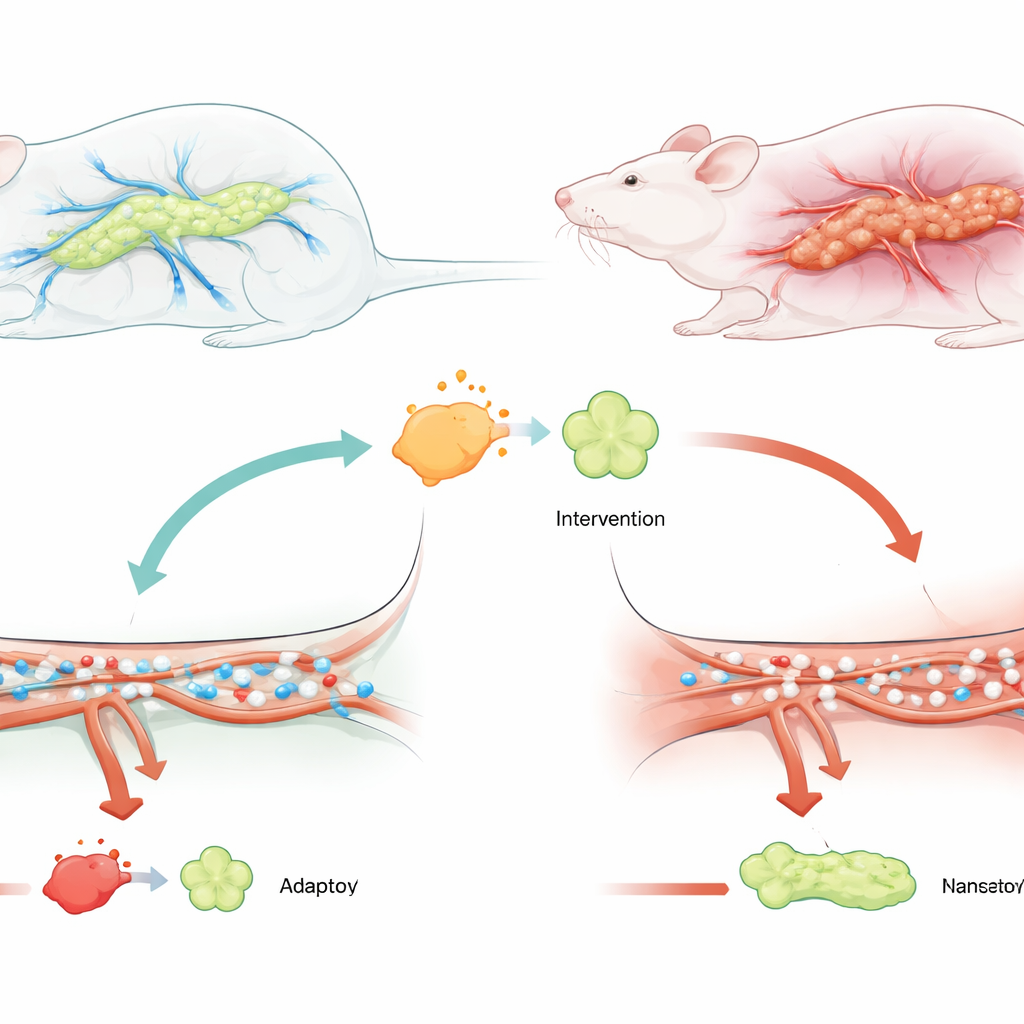
Una mirada más cercana a un brote peligroso
Los autores se centraron en una forma grave de la enfermedad denominada pancreatitis aguda grave, en la que los pacientes a menudo acaban en cuidados intensivos y con alto riesgo de fallo orgánico. Trabajos previos habían mostrado que una proteína llamada USP25 está aumentada en personas y modelos animales con pancreatitis, y que puede avivar la inflamación. Al mismo tiempo, otra proteína, TRAF6, se conoce como un centro clave que retransmite señales de estrés y peligro dentro de células inmunes y tisulares. Dado que ambas moléculas participan en el daño inflamatorio, el equipo sospechó que USP25 podría estar empeorando los problemas de flujo sanguíneo en el páncreas actuando a través de TRAF6.
Modelos animales revelan una asociación perjudicial
Para probar esta idea, los investigadores usaron ratas en las que se desencadenó una pancreatitis grave mediante la inyección de una sal biliar en el conducto pancreático, un modelo ampliamente utilizado de la enfermedad. Algunas ratas recibieron un virus que redujo los niveles de USP25 en el páncreas antes del episodio. En comparación con los animales no tratados, las ratas con USP25 reducido mostraron marcadores sanguíneos de lesión pancreática mucho más bajos, tejido pancreático con mejor aspecto al microscopio y muchas menos señales de hinchazón, sangrado y muerte celular. De forma importante, las mediciones de la microcirculación mostraron que los glóbulos rojos en las ratas tratadas fluían más rápido y por más vasos diminutos, lo que indica que las obstrucciones más severas del flujo sanguíneo se habían aliviado.
Cómo funciona el interruptor molecular dentro de las células
El equipo se centró entonces en las células acinares pancreáticas individuales, las productoras de enzimas del órgano. En células acinares de rata cultivadas expuestas a un compuesto que desencadena pancreatitis, los niveles de USP25 se dispararon, la supervivencia celular cayó y más células murieron. Cuando USP25 fue silenciado, las células tenían más probabilidades de sobrevivir y liberaron menos sustancias inflamatorias. Pruebas bioquímicas mostraron que USP25 se une físicamente a TRAF6 y lo protege de ser marcado para su destrucción por el sistema de reciclaje de proteínas de la célula. Como resultado, TRAF6 se acumula y mantiene activada la señalización inflamatoria. Cuando USP25 fue bloqueado, TRAF6 recibió más marcas de degradación, sus niveles cayeron y la señalización dañina se atenuó.
Demostrando que TRAF6 es el intermediario clave
Para asegurarse de que TRAF6 era el intermediario crucial, los científicos aumentaron artificialmente los niveles de TRAF6 incluso mientras USP25 estaba siendo bloqueado. En las células, este exceso de TRAF6 anuló gran parte de la protección conferida por la inhibición de USP25: más células murieron y las sustancias inflamatorias volvieron a aumentar. En las ratas, el aumento de TRAF6 también minó los beneficios de reducir USP25. El flujo sanguíneo en los microvasos empeoró, aumentaron los marcadores químicos de constricción vascular y estrés oxidativo, y el daño al tejido pancreático se intensificó. Estos experimentos de rescate respaldan una cadena de eventos sencilla: USP25 preserva TRAF6, TRAF6 impulsa la inflamación y esa inflamación asfixia la microcirculación pancreática.
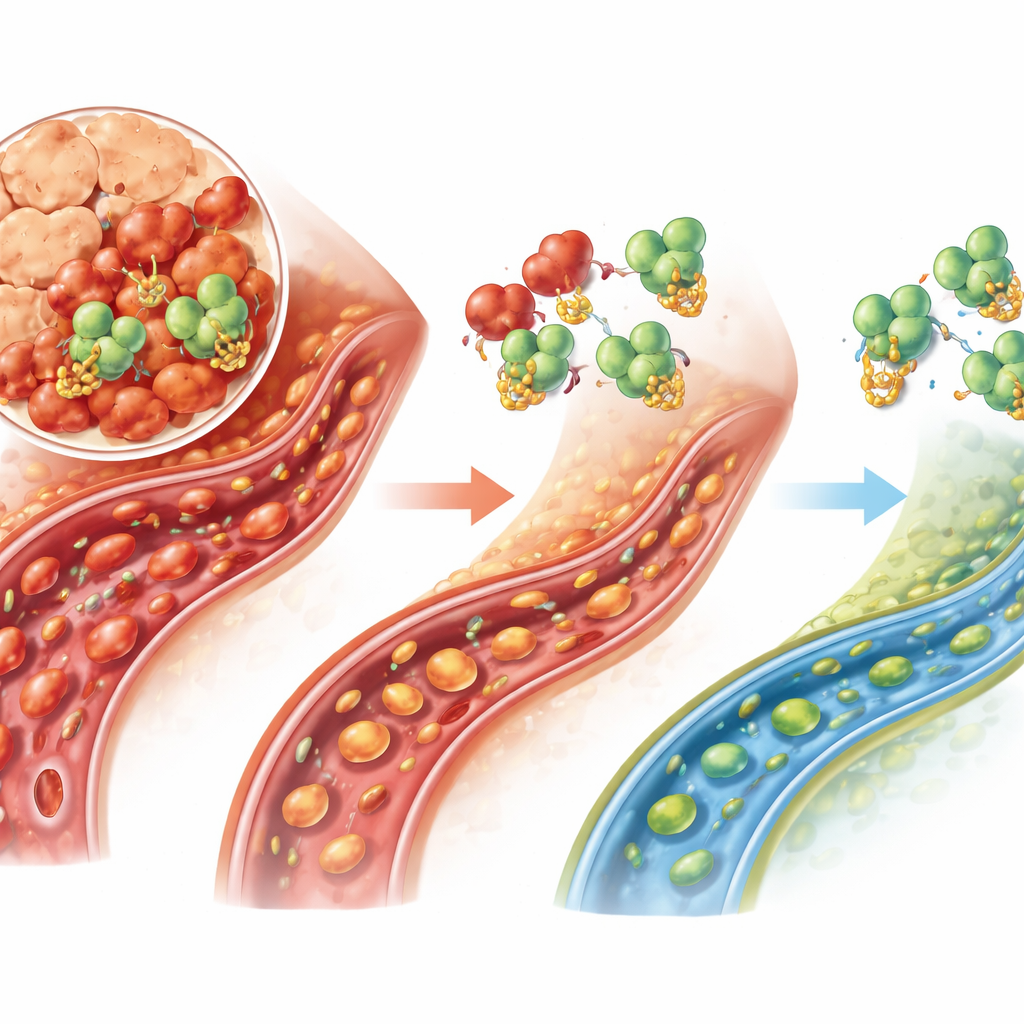
Qué podría significar esto para tratamientos futuros
Para las personas que hoy enfrentan una pancreatitis aguda grave, la atención es sobre todo de soporte —líquidos, nutrición y alivio del dolor— porque no existe ningún fármaco que detenga directamente la cascada de la enfermedad. Este estudio identifica un eje molecular específico, USP25 actuando a través de TRAF6, que parece empeorar la falla de los vasos diminutos y la muerte celular en el páncreas. Si bien el trabajo es preclínico y se basa principalmente en un modelo animal y en una línea celular de rata, apunta a USP25 como un objetivo prometedor: bloquear esta enzima podría permitir que el organismo elimine TRAF6, reduzca la inflamación y mantenga el flujo sanguíneo en el páncreas cuando más está en riesgo.
Cita: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
Palabras clave: pancreatitis aguda grave, microcirculación pancreática, USP25, TRAF6, inflamación