Clear Sky Science · nl
De rol en het regulatiemechanisme van USP25 bij pancreatische microcirculatoire stoornissen bij ernstige acute pancreatitis
Waarom de kleine bloedvaten in de alvleesklier ertoe doen
Ernstige acute pancreatitis is een plotselinge aanval op de alvleesklier die snel levensbedreigend kan worden. In de zwaarste gevallen gaan niet alleen de spijsverteringscellen in het orgaan dood, maar raken ook de allerkleinste bloedvaten die de alvleesklier van bloed voorzien verstopt of ingezakt, waardoor het weefsel verstoken raakt van zuurstof. Deze studie stelt een praktische vraag met grote implicaties: welke moleculaire schakelaars laten deze microvaten falen, en kan het uitschakelen van één daarvan de alvleesklier beschermen?
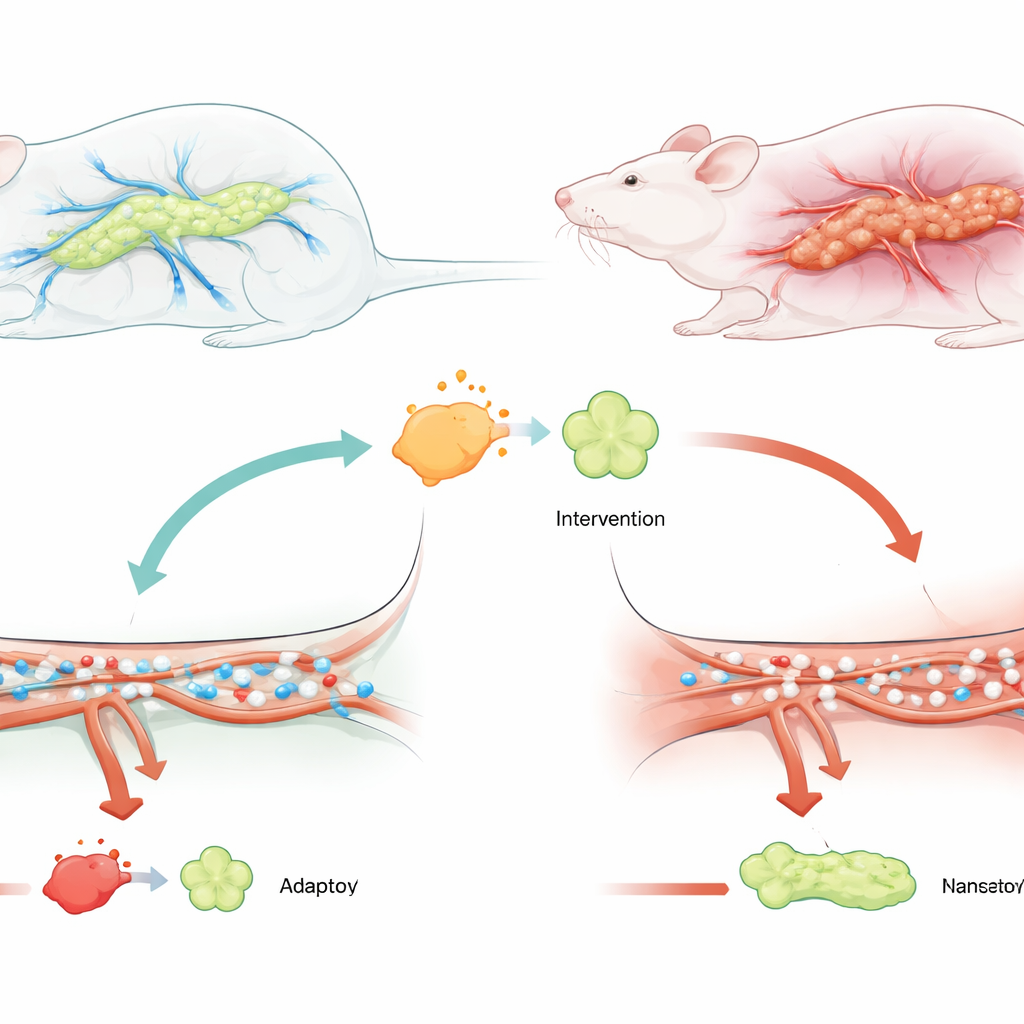
Een nadere blik op een gevaarlijke uitbarsting
De auteurs concentreerden zich op een ernstige vorm van de ziekte die ernstige acute pancreatitis heet, waarbij patiënten vaak op de intensive care belanden en een groot risico lopen op orgaanfalen. Eerdere studies toonden aan dat het eiwit USP25 verhoogd is bij mensen en diermodellen met pancreatitis, en dat het ontsteking kan aanwakkeren. Tegelijkertijd is een ander eiwit, TRAF6, bekend als een belangrijk knooppunt dat stress- en alarmsignalen binnen immuun- en weefselcellen doorgeeft. Omdat beide moleculen betrokken zijn bij inflammatoire schade, vermoedden de onderzoekers dat USP25 de problemen met de bloedstroom in de alvleesklier mogelijk verergert door via TRAF6 te werken.
Diermodellen onthullen een schadelijke samenwerking
Om dit idee te testen, gebruikten de onderzoekers ratten waarbij ernstige pancreatitis werd opgewekt door een galzout in het pancratische kanaal te injecteren, een veelgebruikt model voor de ziekte. Sommige ratten kregen vooraf een virus toegediend dat de USP25-niveaus in de alvleesklier verlaagde. Vergeleken met onbehandelde dieren hadden ratten met verlaagd USP25 veel lagere bloedwaarden van pancreatische schade, gezonder ogend pancreatisch weefsel onder de microscoop en veel minder tekenen van zwelling, bloedingen en celdood. Belangrijk is dat metingen van de microcirculatie lieten zien dat rode bloedcellen bij behandelde ratten sneller stroomden en door meer kleine vaten gingen, wat aangeeft dat de ergste blokkades in de bloedstroom waren verminderd.
Hoe de moleculaire schakel binnen cellen werkt
Het team zoomde vervolgens in op individuele pancreatische acinaire cellen, de enzymproducerende werkpaarden van het orgaan. In gekweekte rat-acinaire cellen die werden blootgesteld aan een pancreatitis-uitlokkende verbinding, steeg USP25 sterk, daalde het celoverleven en gingen meer cellen dood. Wanneer USP25 werd stilgelegd, overleefden cellen vaker en gaven ze minder ontstekingsstoffen af. Biochemische tests lieten zien dat USP25 fysiek bindt aan TRAF6 en het beschermt tegen markering voor afbraak via het cellulaire eiwitrecyclingsysteem. Daardoor hoopt TRAF6 zich op en blijft de ontstekingssignalering actief. Wanneer USP25 werd geblokkeerd, raakte TRAF6 zwaarder gemarkeerd voor afbraak, daalden de niveaus en verminderde de schadelijke signalering.
Aantonen dat TRAF6 de sleutelschakel is
Om zeker te weten dat TRAF6 de cruciale tussenpersoon was, verhoogden de wetenschappers kunstmatig de TRAF6-niveaus, zelfs terwijl USP25 werd geblokkeerd. In cellen wiste die extra TRAF6 een groot deel van de bescherming die door USP25-remming werd geboden: meer cellen stierven en ontstekingsfactoren stegen weer. Bij ratten ondermijnde het verhogen van TRAF6 eveneens de voordelen van het verlagen van USP25. De bloedstroom door microvaten verslechterde, chemische markers van vaatvernauwing en oxidatieve stress namen toe en de schade aan pancreatisch weefsel verergerde. Deze rescue-experimenten ondersteunen een eenvoudige keten van gebeurtenissen: USP25 behoudt TRAF6, TRAF6 drijft ontsteking aan, en die ontsteking verstikt de pancreatische microcirculatie.
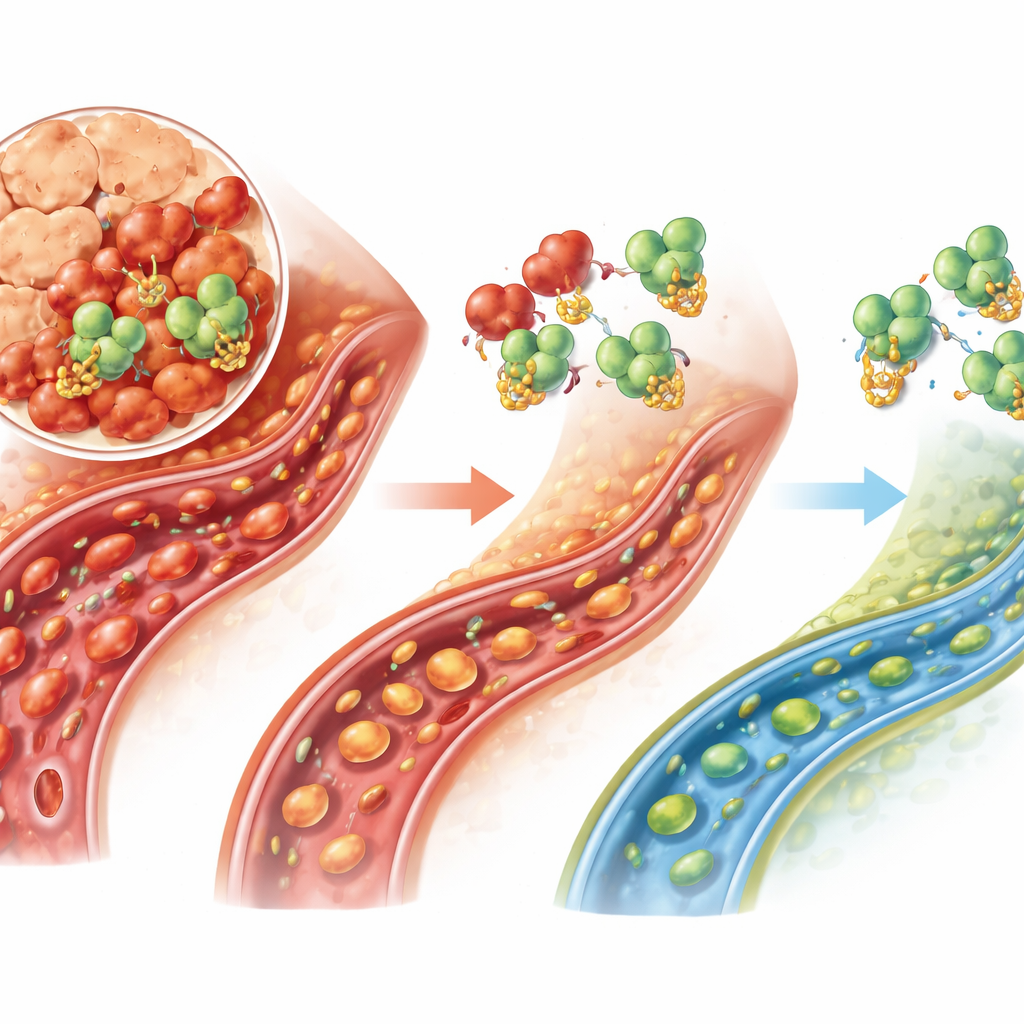
Wat dit kan betekenen voor toekomstige behandelingen
Voor mensen die vandaag de dag geconfronteerd worden met ernstige acute pancreatitis is de zorg grotendeels ondersteunend—vloeistoffen, voeding en pijnbestrijding—omdat geen enkel geneesmiddel de ziektecascade direct stopt. Deze studie identificeert een specifiek moleculair as, USP25 werkend via TRAF6, dat lijkt bij te dragen aan falen van kleine vaten en celdood in de alvleesklier. Hoewel het werk preklinisch is en hoofdzakelijk gebaseerd op één diermodel en een ratten-cellijn, wijst het op USP25 als een veelbelovend doelwit: het blokkeren van dit enzym zou het lichaam in staat kunnen stellen TRAF6 af te breken, de ontsteking te verminderen en de bloeddoorstroming door de alvleesklier te behouden wanneer die het meest kwetsbaar is.
Bronvermelding: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
Trefwoorden: ernstige acute pancreatitis, pancreatische microcirculatie, USP25, TRAF6, ontsteking