Clear Sky Science · ja
重症急性膵炎における膵臓微小循環障害に対するUSP25の役割と制御機構
膵臓の微小血管が重要な理由
重症急性膵炎は膵臓への急襲であり、急速に生命を脅かす状態に進行することがあります。最悪の場合、消化酵素を産生する細胞が壊死するだけでなく、膵臓に酸素を供給するごく細い血管が詰まり崩壊し、組織が虚血に陥ります。本研究は実用的で影響の大きい問いを立てています:どの分子スイッチがこれらの微小血管の機能不全を引き起こし、そのうちの一つを止めることで膵臓を保護できるか、という点です。
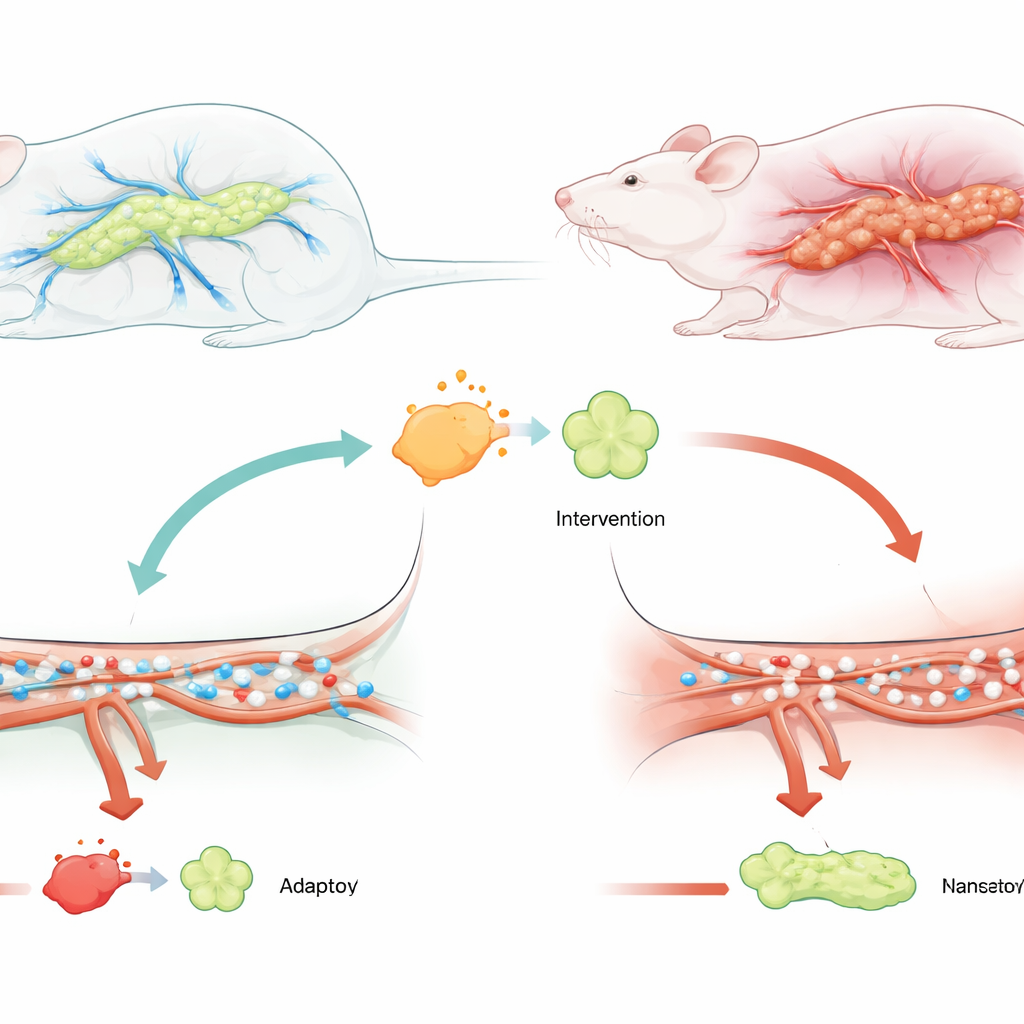
危険な急性増悪を詳しく見る
著者らは、患者が集中治療を要し臓器不全のリスクが高い重症急性膵炎に着目しました。先行研究は、USP25というタンパク質が膵炎患者や疾患モデルで上昇し、炎症を増幅する可能性があることを示していました。同時に、TRAF6は免疫細胞や組織細胞内でストレスや危険信号を中継する重要なハブとして知られています。両分子が炎症性損傷に関与することから、研究チームはUSP25がTRAF6を介して膵臓の血流障害を悪化させているのではないかと推測しました。
動物モデルが示す有害な連携
この仮説を検証するため、研究者らは膵管に胆汁塩を注入して重症膵炎を誘導するラットモデルを用いました。実験では攻撃前に膵臓でUSP25レベルを低下させるウイルスを投与したラットも含めました。未処置群と比べて、USP25が低下したラットは膵損傷の血中マーカーが著しく低く、組織像も良好で、腫脹・出血・細胞死の兆候が大幅に減少しました。重要なことに、微小循環の測定では、処置群の赤血球はより速く、より多くの微小血管を通って流れており、深刻な血流閉塞が緩和されていることが示されました。
細胞内で分子スイッチが働く仕組み
研究チームは次に、膵臓の酵素産生を担う腺房細胞に着目しました。培養したラット腺房細胞に膵炎誘発化合物を与えると、USP25の発現が急上昇し、細胞生存率が低下して細胞死が増加しました。USP25をサイレンシングすると、細胞は生存しやすくなり、炎症性物質の放出も減少しました。生化学的解析では、USP25がTRAF6に物理的に結合し、細胞のタンパク質分解システムによる分解マーキングからTRAF6を保護していることが示されました。その結果、TRAF6は蓄積して炎症シグナルを持続させます。USP25を阻害すると、TRAF6は分解のためのタグを受けやすくなりレベルが低下し、有害なシグナルは沈静化しました。
TRAF6が鍵となる仲介者であることの立証
TRAF6が重要な仲介役であることを確かめるため、研究者らはUSP25を阻害した状況でもTRAF6のレベルを人工的に増強しました。細胞実験では、この余剰のTRAF6がUSP25抑制による保護効果の多くを消し去り、細胞死が増え炎症性物質が再び上昇しました。ラットでもTRAF6を高めるとUSP25低下の利点が損なわれました。微小血管の血流は悪化し、血管収縮や酸化ストレスの化学マーカーが増加し、膵組織損傷が強まりました。これらのリスキュー実験は単純な事象連鎖を支持します:USP25はTRAF6を保持し、TRAF6は炎症を推進し、その炎症が膵臓の微小循環を絞扼する、という流れです。
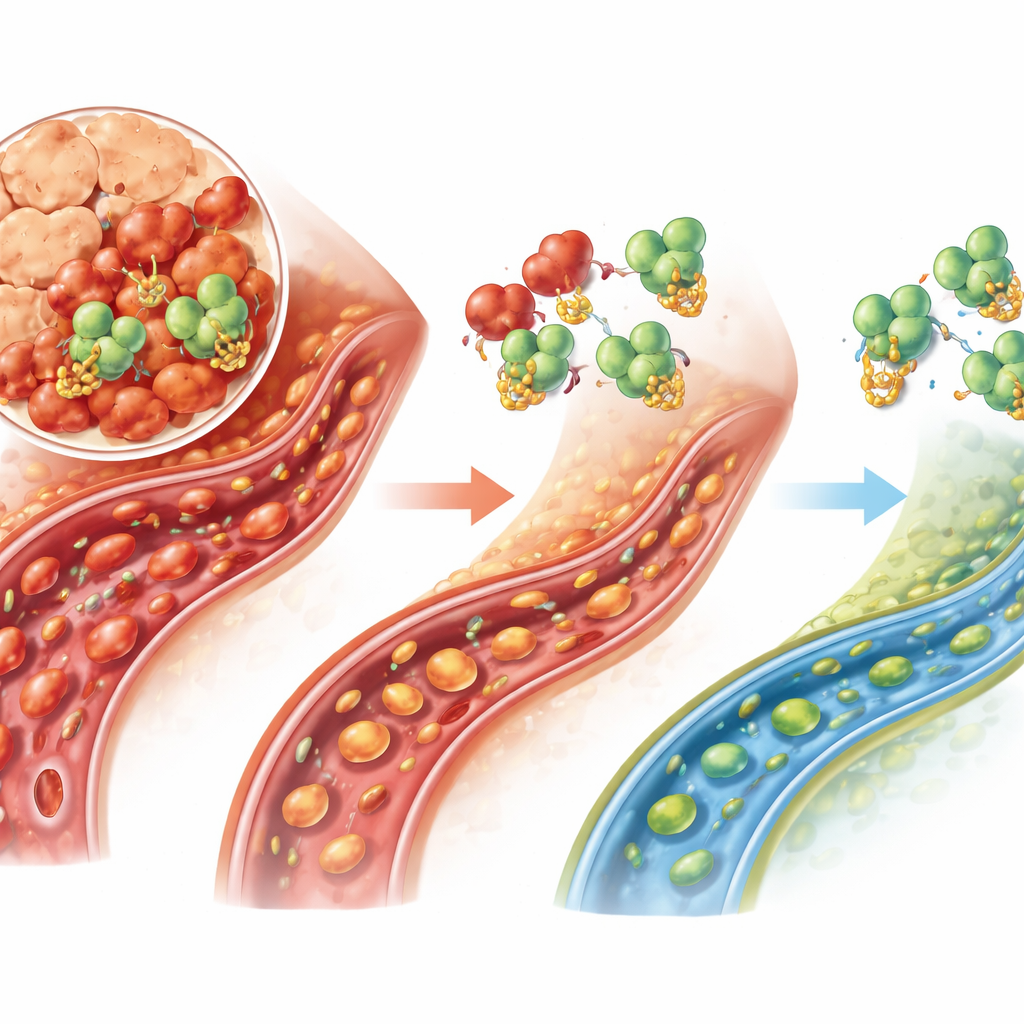
将来の治療に向けた意義
現在、重症急性膵炎患者に対する治療は主に対症療法—輸液、栄養、鎮痛—にとどまり、疾患カスケードを直接止める薬はありません。本研究は、微小血管の破綻や細胞死を悪化させる明確な分子経路、すなわちUSP25がTRAF6を介して働く軸を同定しました。本研究は前臨床段階であり、主に一つの動物モデルとラット細胞株に基づく点は限界ですが、USP25を標的とすることによりTRAF6を解体し、炎症を和らげ、最も危険な時期に膵臓への血流を維持できる可能性が示唆されます。
引用: Zhang, Q., Zhang, X. & Shan, F. The role and regulatory mechanism of USP25 in pancreatic microcirculatory disturbance in severe acute pancreatitis. Sci Rep 16, 11570 (2026). https://doi.org/10.1038/s41598-026-39295-9
キーワード: 重症急性膵炎, 膵臓微小循環, USP25, TRAF6, 炎症