Clear Sky Science · pt
As cascatas de sinalização moldam subpopulações funcionais de astrócitos corticais em camundongos machos selvagens e no modelo de Alzheimer APP/PS1dE9
Auxiliares Ocultos no Cérebro
A doença de Alzheimer costuma ser descrita como uma história sobre neurônios doentes e aglomerados pegajosos de proteína chamados placas. Mas os neurônios não trabalham sozinhos. Eles são cercados por células de suporte em forma de estrela, os astrócitos, que silenciosamente mantêm os circuitos cerebrais funcionando. Este estudo mostra que mesmo entre essas células “auxiliares” existem equipes distintas com tarefas diferentes, e que seus sistemas internos de comunicação podem influenciar tanto o acúmulo de placas quanto o comportamento em um modelo murino da doença de Alzheimer.
Equipes Diferentes de Células de Suporte
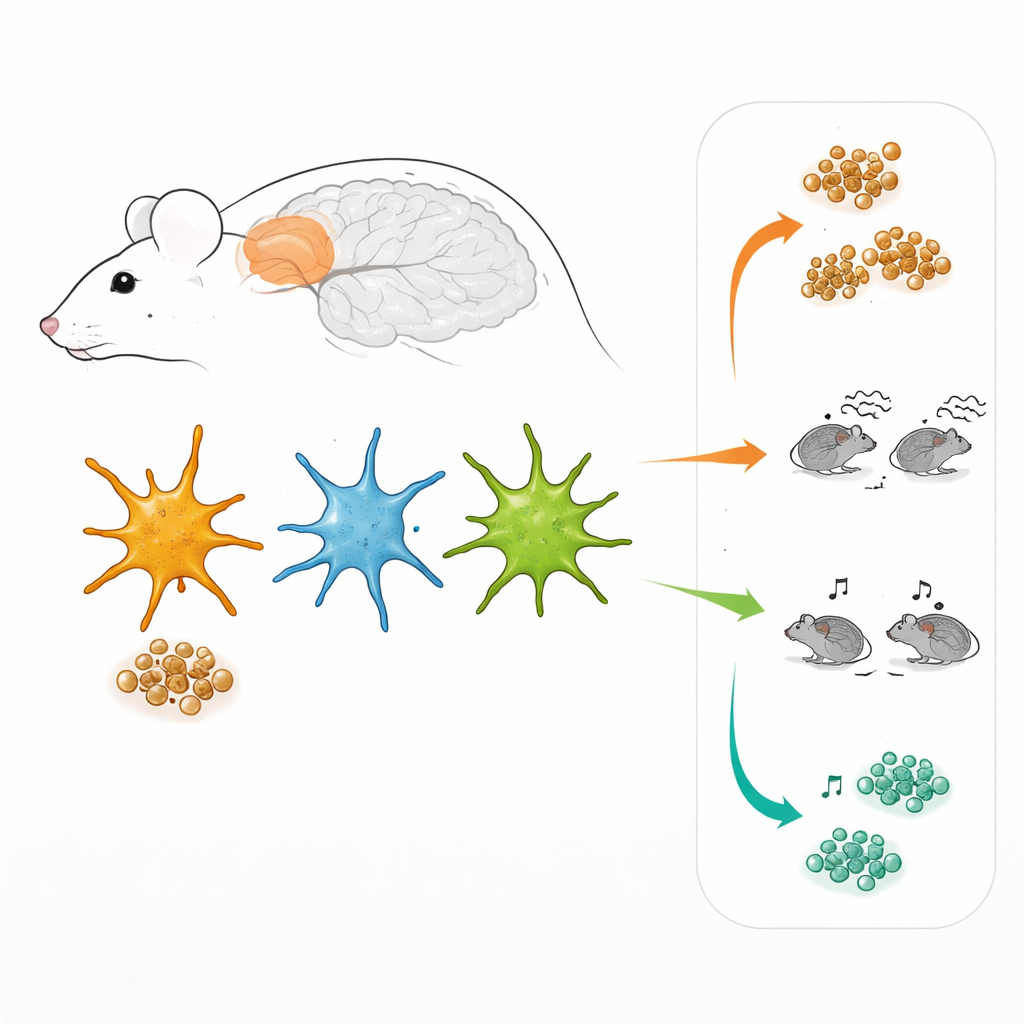
Os astrócitos não são um grupo uniforme. Trabalhando no córtex pré-frontal, uma região cerebral envolvida na tomada de decisão e no comportamento social, os pesquisadores usaram vírus especialmente projetados para fazer os astrócitos brilharem quando duas principais vias internas de sinalização estavam ativas. Uma via é controlada por um fator chamado STAT3, a outra por NF-kB. Em tecido cerebral vivo, isso permitiu “marcar” três subgrupos de astrócitos: aqueles que usam principalmente a via STAT3, os que usam principalmente a via NF-kB e os que usam ambas ao mesmo tempo. Surpreendentemente, esses três grupos estavam presentes não apenas em camundongos com fenótipo semelhante ao Alzheimer, mas também em camundongos saudáveis, e estavam espalhados por todo o córtex em vez de concentrados em uma camada específica ou ao redor das placas.
Não Apenas uma Reação às Placas
Como as placas proteicas na doença de Alzheimer afetam fortemente as células cerebrais próximas, poderia se esperar que esses subgrupos de astrócitos aparecessem principalmente ao redor desses depósitos. Em vez disso, os níveis de atividade de STAT3 e NF-kB nos astrócitos não dependiam de quão próximas as células estavam das placas nem do tamanho das placas. Os mesmos três tipos de astrócitos já estavam presentes em camundongos mais jovens antes de muitas placas se formarem, e em camundongos normais que nunca desenvolvem acúmulo de amiloide. Isso sugere que as diferentes equipes de astrócitos surgem a partir de propriedades intrínsecas, “programadas”, das células, com a doença então modificando o que cada equipe faz em vez de criar tipos inteiramente novos.
Formas Distintas e Tarefas de Manutenção
As três equipes de astrócitos diferiam não apenas em sua sinalização, mas também em sua forma, composição molecular e tarefas cotidianas. As células dominadas pela via NF-kB tendiam a cobrir um território maior no tecido e mostravam maior atividade de compartimentos de reciclagem interna que degradam proteínas. Os astrócitos dominados por STAT3, em contraste, eram menores, mas apresentavam canais de membrana mais ativos chamados hemicanais, que controlam a passagem de pequenas moléculas entre a célula e seu entorno. Medições da atividade gênica em células selecionadas confirmaram que cada grupo ativava um conjunto diferente de genes, especialmente aqueles envolvidos em inflamação e no manejo e remoção de proteínas. Nos camundongos com fenótipo semelhante ao Alzheimer, essas diferenças moleculares foram amplificadas, com algumas vias em células ricas em STAT3 mostrando sinais claros de estresse.
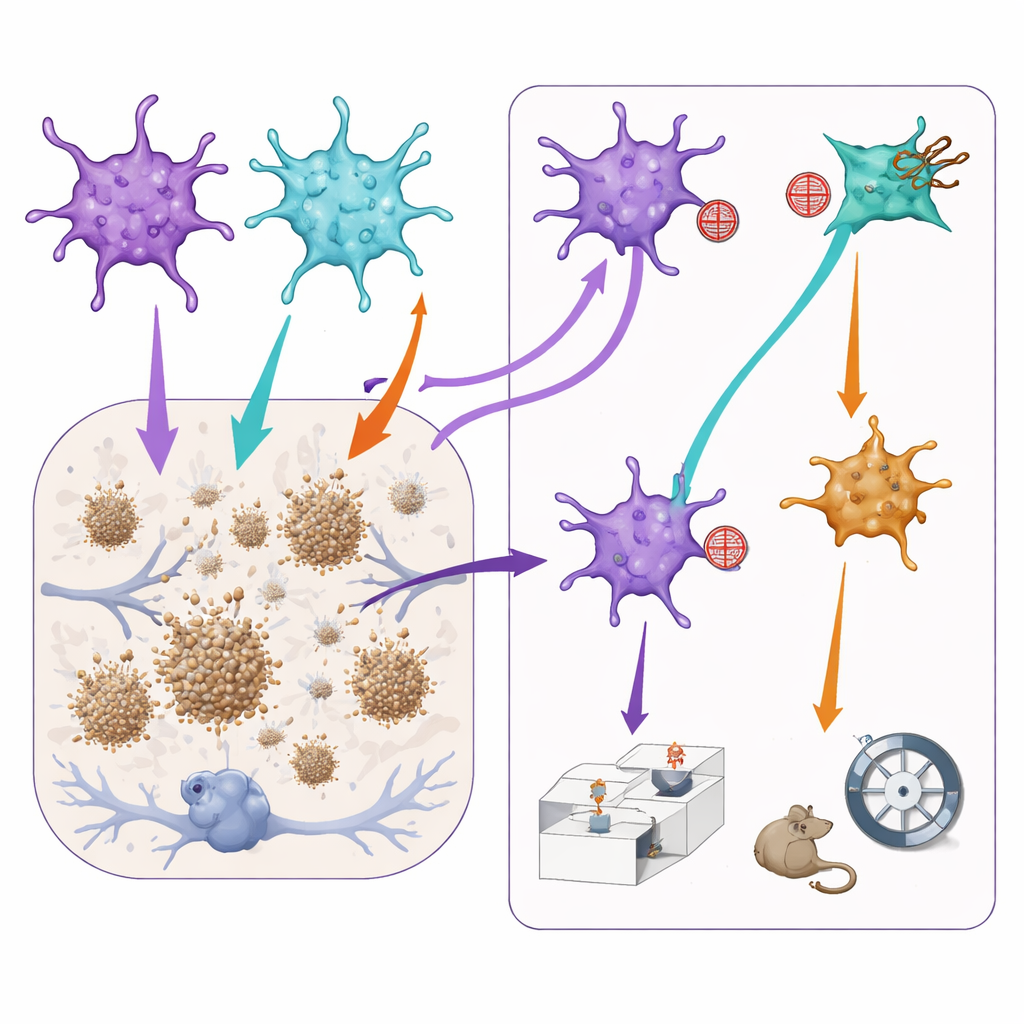
Ajustar a Sinalização dos Astrócitos Muda Placas e Comportamento
Para testar como esses subgrupos afetam características da doença, a equipe então usou ferramentas virais adicionais para atenuar suavemente a sinalização de STAT3 ou NF-kB apenas nos astrócitos onde essas vias já estavam ativas. Em camundongos com fenótipo semelhante ao Alzheimer, bloquear a via STAT3 levou a placas de amiloide menores no córtex pré-frontal, sugerindo que astrócitos dominados por STAT3 podem, direta ou indiretamente, favorecer o crescimento das placas. No entanto, essa mesma manipulação piorou aspectos da memória social: os camundongos tiveram mais dificuldade em distinguir um camundongo familiar de um novo. Por outro lado, reduzir a sinalização de NF-kB pareceu aliviar ligeiramente comportamentos semelhantes à ansiedade, mas também reduziu o interesse e a memória social normais. Importante, realizar as mesmas manipulações em camundongos saudáveis teve pouco efeito, indicando que essas equipes de astrócitos se tornam especialmente influentes em um cérebro doente.
O Que Isso Significa para a Doença de Alzheimer
Este trabalho pinta um quadro mais nuançado das células de suporte do cérebro na doença de Alzheimer. Em vez de responderem de forma uniforme, os astrócitos se dividem em grupos funcionais distintos definidos por suas cascatas internas de sinalização. Esses grupos diferem em tamanho, capacidade de limpar proteínas e na forma como se comunicam com células vizinhas, e contribuem de maneira diferente para o crescimento de placas e para comportamentos relacionados à ansiedade e interação social. Para terapias futuras, isso sugere que ligar ou desligar amplamente os astrócitos pode ser uma abordagem grosseira demais. Em vez disso, direcionar cuidadosamente rotas de sinalização específicas em subpopulações selecionadas de astrócitos poderá, um dia, ajudar a ajustar o equilíbrio entre proteger os circuitos cerebrais, limitar o acúmulo prejudicial de proteínas e preservar o comportamento normal.
Citação: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Palavras-chave: astrócitos, doença de Alzheimer, sinalização cerebral, neuroinflamação, clareamento de proteínas