Clear Sky Science · pl
Kaskady sygnalizacyjne kształtują funkcjonalne subpopulacje astrocytów korowych u samców myszy typu dzikiego i w modelu choroby Alzheimera APP/PS1dE9
Ukryci pomocnicy w mózgu
Chorobę Alzheimera często przedstawia się jako historię o chorych neuronach i lepkich skupiskach białkowych zwanych płytkami. Neurony jednak nie działają w izolacji. Otaczają je gwiaździste komórki wspomagające — astrocyty — które dyskretnie utrzymują funkcjonowanie obwodów mózgowych. Badanie to pokazuje, że nawet wśród tych „pomocniczych” komórek istnieją odrębne zespoły z różnymi zadaniami, a ich wewnętrzne systemy komunikacji mogą wpływać zarówno na narastanie płytek, jak i na zachowanie w modelu myszy choroby Alzheimera.
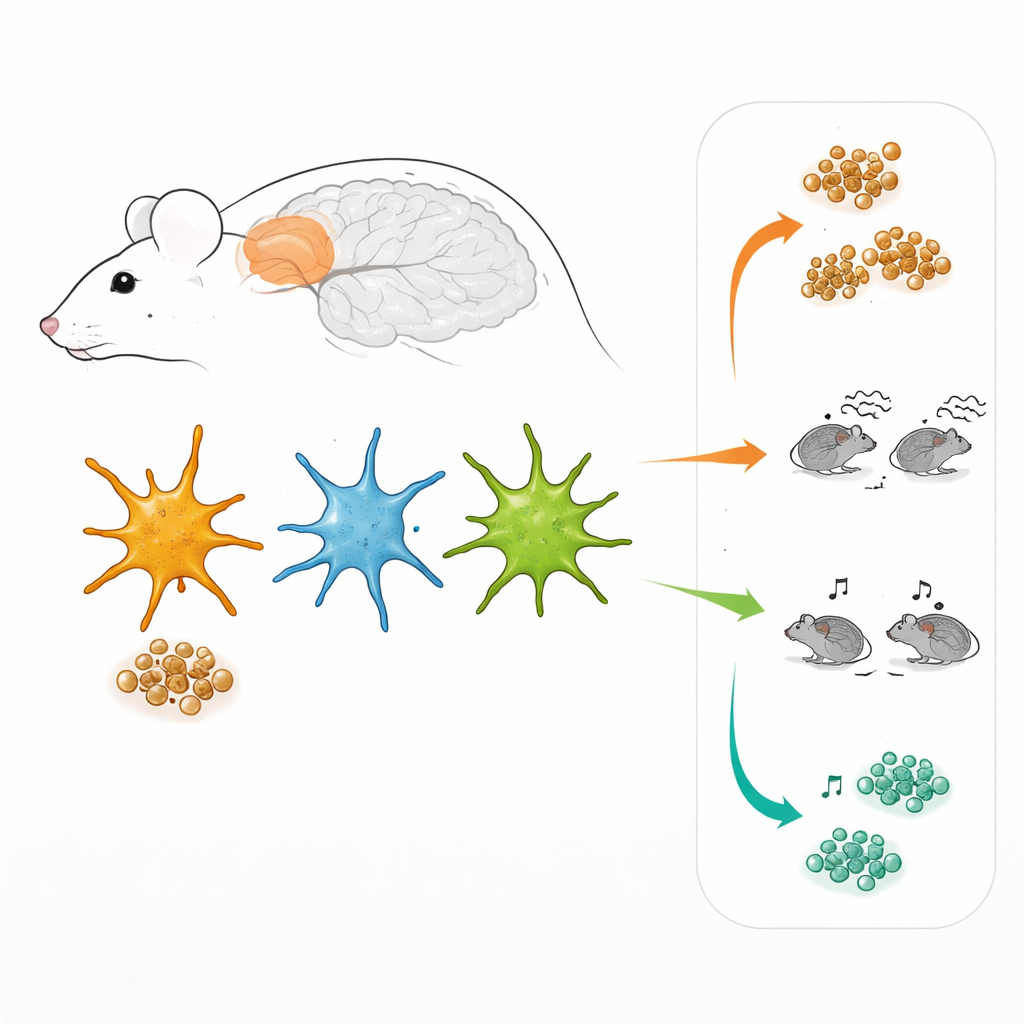
Różne zespoły komórek wspomagających
Astrocyty nie są jednorodną masą. Pracując w korze przedczołowej — obszarze mózgu zaangażowanym w podejmowanie decyzji i zachowania społeczne — badacze użyli specjalnie zaprojektowanych wirusów, aby sprawić, że astrocyty zaświecą się, gdy aktywne są dwie główne ścieżki wewnątrzkomórkowej sygnalizacji. Jedna trasa jest kontrolowana przez czynnik STAT3, druga przez NF-kB. W żywej tkance mózgowej pozwoliło to „otagować” trzy podgrupy astrocytów: te głównie używające szlaku STAT3, te głównie używające NF-kB oraz te korzystające z obu jednocześnie. Co zaskakujące, trzy te grupy występowały nie tylko u myszy przypominających Alzheimera, ale także u zdrowych myszy, i były rozproszone po całej korze, a nie skupione w konkretnej warstwie czy wokół płytek.
Nie tylko reakcja na płytki
Ponieważ płytki białkowe w chorobie Alzheimera silnie wpływają na pobliskie komórki mózgowe, można by oczekiwać, że podgrupy astrocytów pojawiają się głównie wokół tych złogów. Tymczasem poziomy aktywności STAT3 i NF-kB w astrocytach nie zależały od tego, jak blisko komórki znajdowały się względem płytek ani od wielkości płytek. Te same trzy typy astrocytów występowały już u młodszych myszy, zanim powstało wiele płytek, oraz u normalnych myszy, które nigdy nie rozwijają nagromadzeń amyloidu. Sugeruje to, że różne zespoły astrocytów wynikają z wrodzonych, „twardo zaprogramowanych” właściwości komórek, a choroba raczej modyfikuje funkcje poszczególnych zespołów niż tworzy całkowicie nowe typy.
Odrębne kształty i prace porządkowe
Trzy zespoły astrocytów różniły się nie tylko sygnalizacją, lecz także kształtem, składem molekularnym i codziennymi obowiązkami. Komórki z przewagą szlaku NF-kB miały tendencję do zajmowania większego terytorium w tkance i wykazywały silniejszą aktywność wewnętrznych kompartmentów recyklingowych, które rozkładają białka. Astrocyty z dominacją STAT3 były z kolei mniejsze, ale miały bardziej aktywne „bramy” błonowe zwane hemichannelami, które kontrolują przepływ małych cząsteczek między komórką a jej otoczeniem. Pomiary aktywności genów w posortowanych komórkach potwierdziły, że każda grupa włączała inny zestaw genów, szczególnie tych związanych z zapaleniem oraz z obsługą i usuwaniem białek. U myszy przypominających Alzheimera różnice molekularne były wzmocnione, a niektóre szlaki w komórkach bogatych w STAT3 wykazywały wyraźne oznaki stresu.
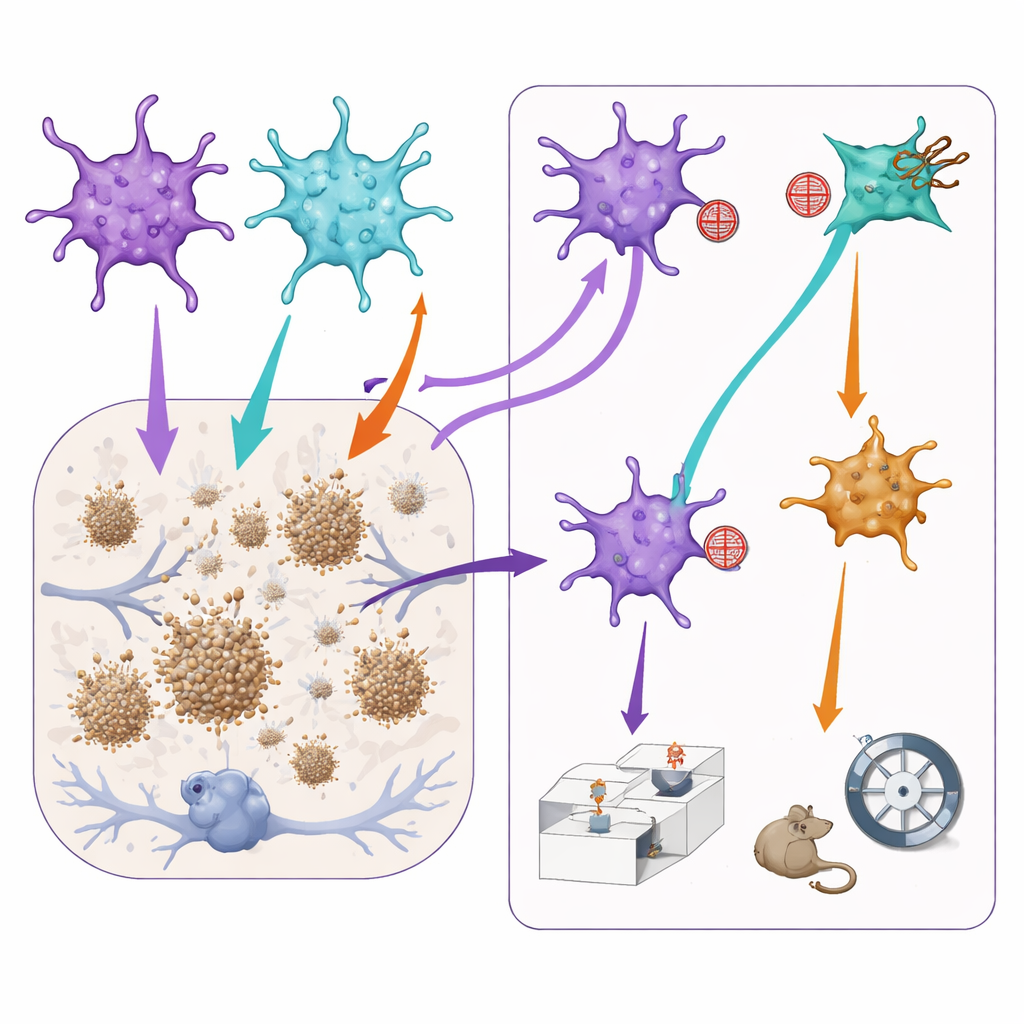
Dostrajanie sygnałów astrocytów zmienia płytki i zachowanie
Aby sprawdzić, jak te podgrupy wpływają na cechy choroby, zespół wykorzystał dodatkowe narzędzia wirusowe, by delikatnie stłumić albo sygnalizację STAT3, albo NF-kB jedynie w tych astrocytach, gdzie te ścieżki były już aktywne. U myszy przypominających Alzheimera zablokowanie szlaku STAT3 prowadziło do mniejszych płytek amyloidowych w korze przedczołowej, co sugeruje, że astrocyty z przewagą STAT3 mogą bezpośrednio lub pośrednio sprzyjać wzrostowi płytek. Jednak ta sama manipulacja pogorszyła aspekty pamięci społecznej: myszy miały większe trudności z rozróżnieniem znajomej myszy od nowej. Natomiast zmniejszenie sygnalizacji NF-kB wydawało się nieco łagodzić zachowania lękowe, ale jednocześnie obniżało normalne zainteresowanie społeczne i pamięć. Co ważne, wykonanie tych samych manipulacji u zdrowych myszy miało niewielki efekt, co wskazuje, że te zespoły astrocytów stają się szczególnie wpływowe w mózgu dotkniętym chorobą.
Co to oznacza dla choroby Alzheimera
Ta praca kreśli bardziej subtelny obraz komórek wspomagających mózg w chorobie Alzheimera. Zamiast reagować jednolicie, astrocyty dzielą się na wyraźne funkcjonalne grupy definiowane przez ich wewnętrzne kaskady sygnalizacyjne. Grupy te różnią się rozmiarem, zdolnościami do oczyszczania białek oraz sposobem komunikacji z sąsiednimi komórkami, i różnie przyczyniają się do wzrostu płytek oraz do zachowań związanych z lękiem i interakcjami społecznymi. Dla przyszłych terapii sugeruje to, że szerokie „włączanie” lub „wyłączanie” astrocytów może być zbyt grubym narzędziem. Zamiast tego precyzyjne celowanie w konkretne szlaki sygnalizacyjne w wybranych subpopulacjach astrocytów mogłoby w przyszłości pomóc lepiej wyważyć ochronę obwodów mózgowych, ograniczanie szkodliwego nagromadzenia białek i zachowanie normalnego zachowania.
Cytowanie: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Słowa kluczowe: astrocyty, choroba Alzheimera, sygnalizacja mózgowa, neurozapalenie, oczyszczanie białek