Clear Sky Science · de
Signalübertragungs-Kaskaden formen funktionelle Unterpopulationen kortikaler Astrozyten bei männlichen Wildtyp-Mäusen und dem Alzheimer-Modell APP/PS1dE9
Verborgene Helfer im Gehirn
Die Alzheimer-Krankheit wird häufig als eine Geschichte kranker Neuronen und klebriger Proteinablagerungen, so genannter Plaques, erzählt. Doch Neuronen arbeiten nicht allein. Sie sind umgeben von sternförmigen Stützzellen, den Astrozyten, die stillschweigend die Funktion von Gehirnschaltkreisen aufrechterhalten. Diese Studie zeigt, dass selbst unter diesen „Helfer“-Zellen unterschiedliche Teams mit verschiedenen Aufgaben existieren und dass ihre inneren Kommunikationswege sowohl die Plaquebildung als auch das Verhalten in einem Mausmodell der Alzheimer-Krankheit beeinflussen können.
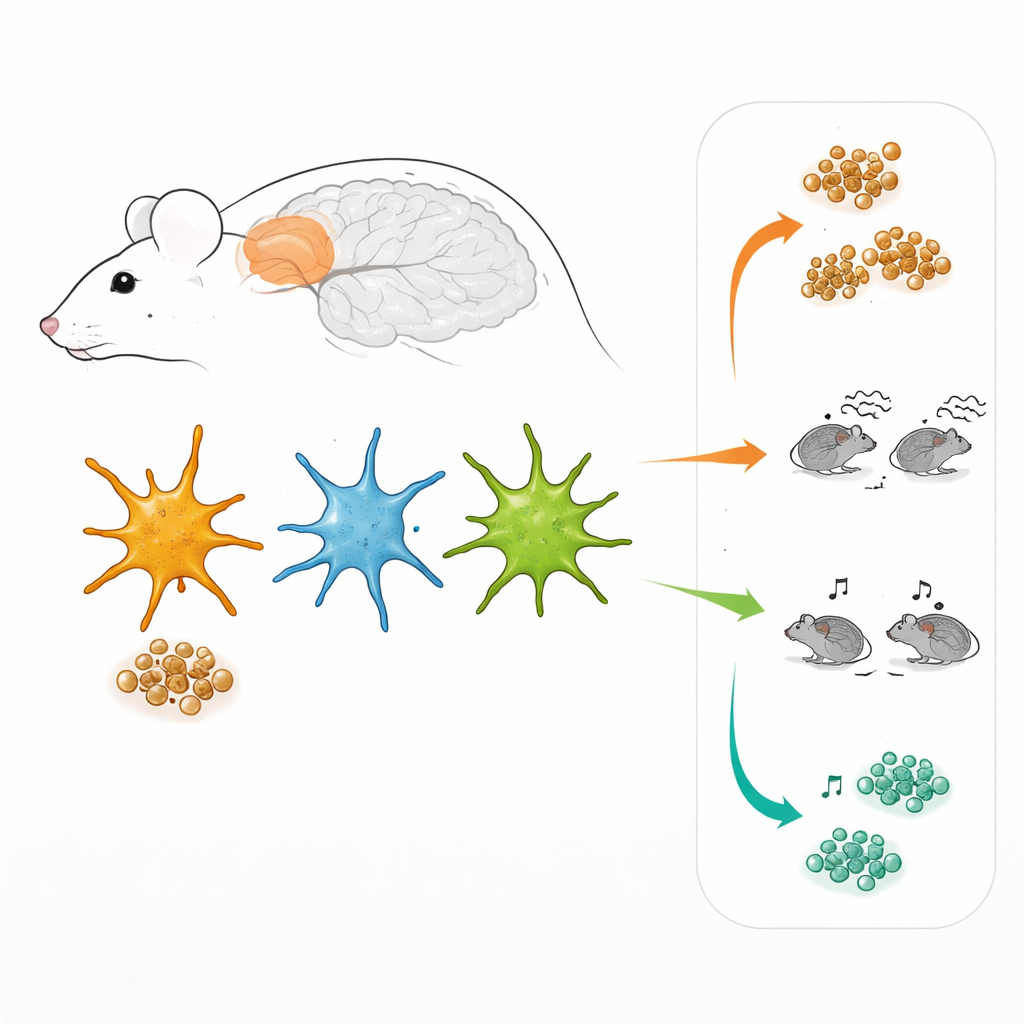
Verschiedene Teams von Stützzellen
Astrozyten sind keine einheitliche Masse. Arbeiten im präfrontalen Kortex, einer Hirnregion, die an Entscheidungsfindung und sozialem Verhalten beteiligt ist, nutzten die Forschenden speziell entwickelte Viren, um Astrozyten zum Leuchten zu bringen, wenn zwei große interne Signalkaskaden aktiv waren. Eine Route wird durch den Faktor STAT3 gesteuert, die andere durch NF-kB. In lebendem Hirngewebe ermöglichte dies, drei Untergruppen von Astrozyten zu „markieren“: solche, die vorwiegend den STAT3-Weg nutzen, solche, die vorwiegend den NF-kB-Weg nutzen, und solche, die beide gleichzeitig nutzen. Überraschenderweise fanden sich diese drei Gruppen nicht nur bei Alzheimer-ähnlichen Mäusen, sondern auch bei gesunden Tieren, und sie waren über den Kortex verteilt, statt in einer bestimmten Schicht oder um Plaques herum zu konzentrieren.
Nicht nur eine Reaktion auf Plaques
Da Proteinplaques bei Alzheimer die umliegenden Gehirnzellen stark beeinflussen, könnte man erwarten, dass diese Astrozyten-Untergruppen vornehmlich in der Nähe solcher Ablagerungen auftreten. Stattdessen hingen die Aktivitätsniveaus von STAT3 und NF-kB in Astrozyten nicht davon ab, wie nahe die Zellen an Plaques lagen oder wie groß die Plaques waren. Dieselben drei Astrozytentypen waren bereits in jüngeren Mäusen vorhanden, bevor zahlreiche Plaques entstanden, und in normalen Mäusen, die nie Amyloidablagerungen entwickeln. Das deutet darauf hin, dass die verschiedenen Astrozyten-Teams aus angelegten, „fest verdrahteten“ Eigenschaften der Zellen entstehen, wobei die Krankheit später eher die Funktion jedes Teams verändert, statt völlig neue Zelltypen zu schaffen.
Unterschiedliche Formen und Hausarbeiten
Die drei Astrozyten-Teams unterschieden sich nicht nur in ihrer Signalgebung, sondern auch in ihrer Gestalt, molekularen Zusammensetzung und ihren alltäglichen Aufgaben. Zellen, die vom NF-kB-Weg dominiert wurden, deckten tendenziell ein größeres Gebiet im Gewebe ab und zeigten stärkere Aktivität interner Recycling-Kompartimente, die Proteine abbauen. STAT3-dominierte Astrozyten waren dagegen kleiner, verfügten aber über aktivere Membrantore, so genannte Hemikanäle, die den Durchtritt kleiner Moleküle zwischen der Zelle und ihrer Umgebung steuern. Messungen der Genaktivität in sortierten Zellen bestätigten, dass jede Gruppe einen anderen Gen-Satz hochregulierte, insbesondere solche, die an Entzündungsprozessen sowie am Umgang mit und dem Abbau von Proteinen beteiligt sind. In den Alzheimer-ähnlichen Mäusen wurden diese molekularen Unterschiede verstärkt, wobei einige Wege in STAT3-reichen Zellen klare Stresszeichen zeigten.
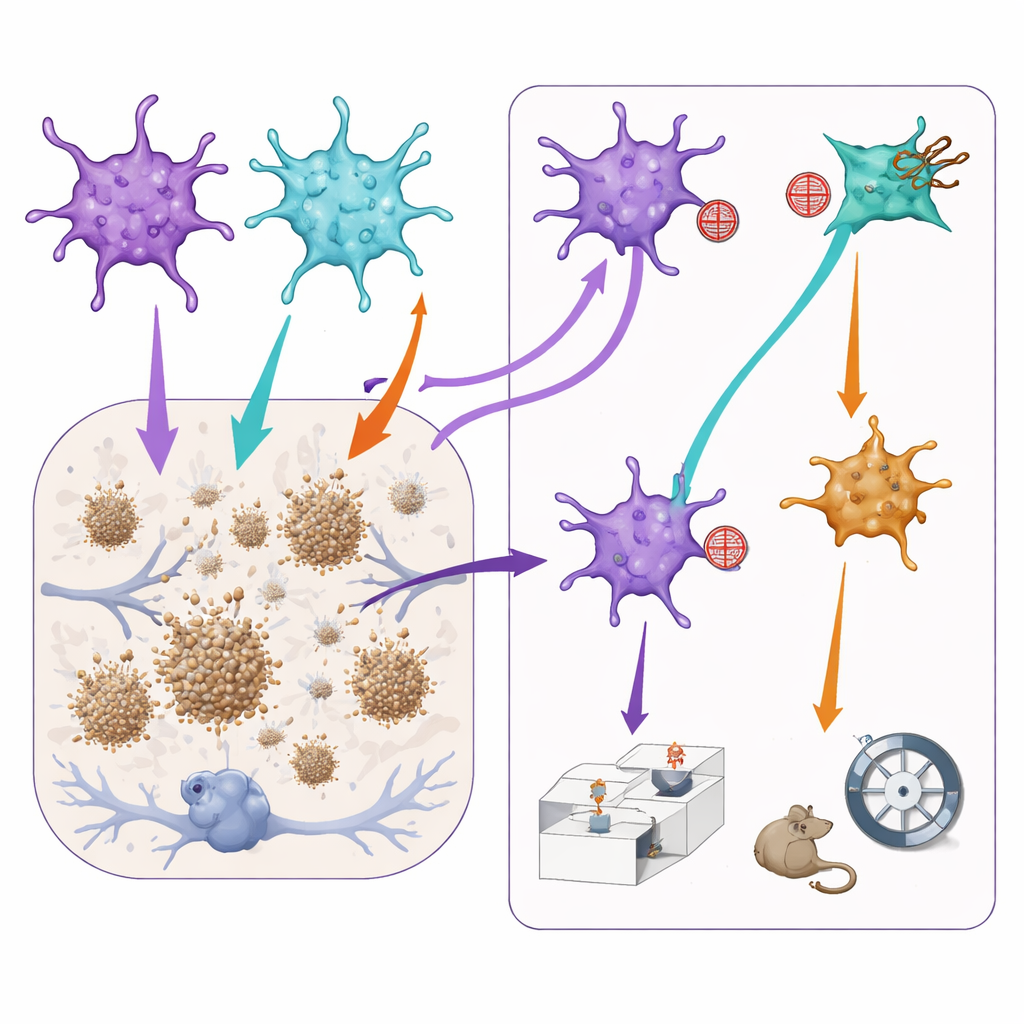
Das Einstellen von Astrozyten-Signalen verändert Plaques und Verhalten
Um zu testen, wie diese Untergruppen Krankheitsmerkmale beeinflussen, verwendete das Team zusätzliche virale Werkzeuge, um entweder den STAT3- oder den NF-kB-Signalweg nur in den Astrozyten abzuschwächen, in denen diese Wege bereits aktiv waren. Bei den Alzheimer-ähnlichen Mäusen führte die Blockade des STAT3-Wegs zu kleineren Amyloidplaques im präfrontalen Kortex, was nahelegt, dass STAT3-dominierte Astrozyten direkt oder indirekt das Plaquewachstum fördern könnten. Allerdings verschlechterte dieselbe Intervention Aspekte des sozialen Gedächtnisses: Die Mäuse hatten mehr Schwierigkeiten, ein vertrautes Tier von einem neuen zu unterscheiden. Umgekehrt schien die Reduktion der NF-kB-Signalgebung leicht angstähnliches Verhalten zu lindern, reduzierte aber auch das normale soziale Interesse und Gedächtnis. Wichtig ist, dass dieselben Manipulationen bei gesunden Mäusen kaum Effekte zeigten, was darauf hindeutet, dass diese Astrozyten-Teams im kranken Gehirn besonders einflussreich werden.
Was das für die Alzheimer-Krankheit bedeutet
Diese Arbeit zeichnet ein nuancierteres Bild der Stützzellen im Gehirn bei Alzheimer. Statt einheitlich zu reagieren, fallen Astrozyten in funktionell unterschiedliche Gruppen, definiert durch ihre internen Signalkaskaden. Diese Gruppen unterscheiden sich in Größe, Fähigkeit zur Proteinsäuberung und in der Kommunikation mit Nachbarzellen und tragen unterschiedlich zum Plaquewachstum sowie zu Verhaltensmerkmalen wie Angst und sozialer Interaktion bei. Für künftige Therapien deutet dies darauf hin, dass ein pauschales „Auf“- oder „Ab“-Regeln der Astrozyten zu grob sein könnte. Stattdessen könnte das gezielte Ansprechen spezifischer Signalwege in ausgewählten Astrozyten-Unterpopulationen eines Tages helfen, das Gleichgewicht zwischen Schutz von Schaltkreisen, Begrenzung schädlicher Proteinablagerungen und Erhalt normalen Verhaltens fein abzustimmen.
Zitation: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Schlüsselwörter: Astrozyten, Alzheimer-Krankheit, Gehirnsignalübertragung, Neuroinflammation, Proteinbeseitigung