Clear Sky Science · nl
Signaalcascade vormen functionele subpopulaties van corticale astrocyten in mannelijke wildtypemuizen en het APP/PS1dE9-Alzheimermodel
Verborgen helpers in de hersenen
De ziekte van Alzheimer wordt vaak verteld als een verhaal over zieke neuronen en kleverige eiwitklonten, plaques genoemd. Maar neuronen werken niet alleen. Ze worden omgeven door stervormige ondersteunende cellen, astrocyten, die stilletjes de hersencircuits draaiende houden. Deze studie toont aan dat zelfs onder deze “hulpcellen” verschillende teams met uiteenlopende taken bestaan, en dat hun interne communicatiesystemen zowel de ophoping van plaques als gedrag in een muismodel van Alzheimer kunnen beïnvloeden.
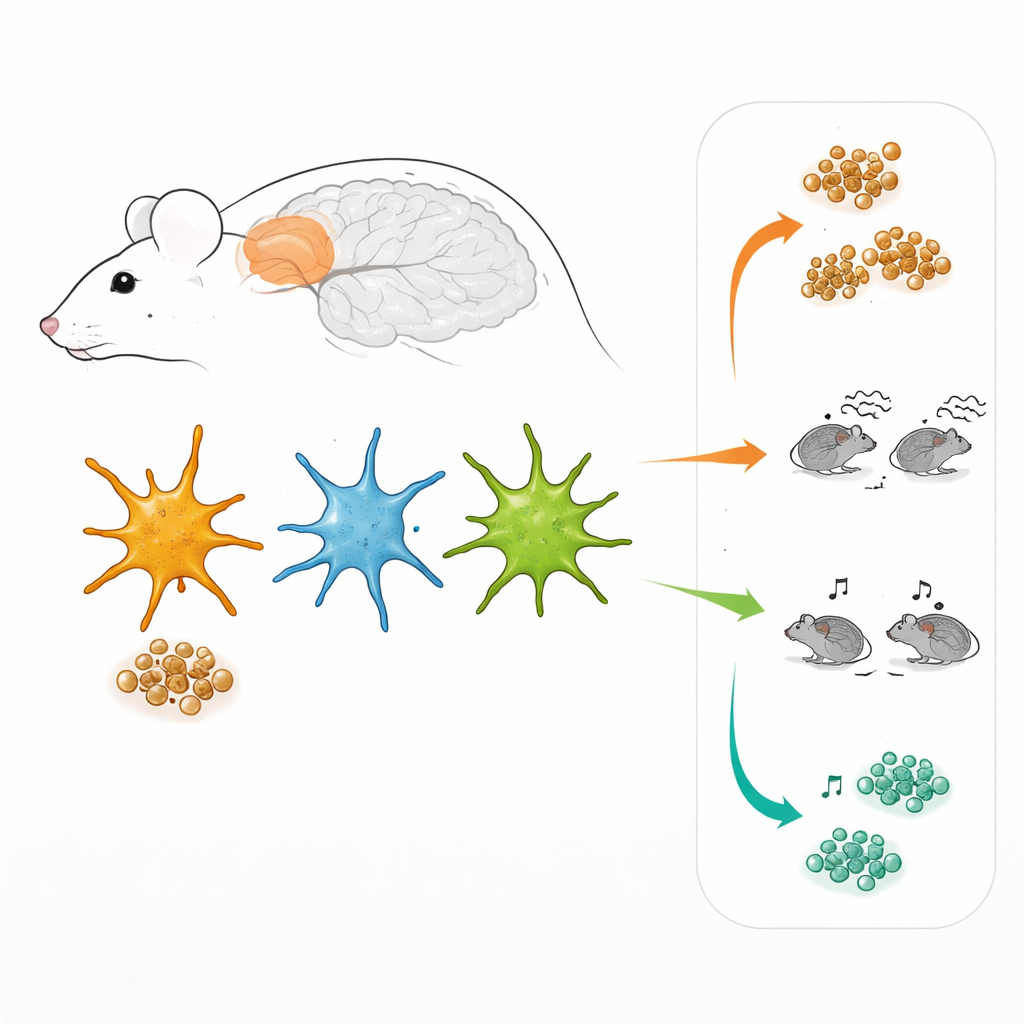
Verschillende teams van ondersteunende cellen
Astrocyten vormen geen uniforme massa. Werkend in de prefrontale cortex, een hersengebied dat betrokken is bij besluitvorming en sociaal gedrag, gebruikten de onderzoekerSpeciaal ontworpen virussen om astrocyten te laten oplichten wanneer twee belangrijke interne signaalroutes actief waren. De ene route wordt gereguleerd door een factor genaamd STAT3, de andere door NF-kB. In levend hersenweefsel stelde dit hen in staat drie subgroepen astrocyten te “taggen”: die voornamelijk de STAT3-route gebruiken, die voornamelijk de NF-kB-route gebruiken, en die beide tegelijk gebruiken. Verrassend genoeg waren deze drie groepen niet alleen aanwezig in Alzheimerachtige muizen maar ook in gezonde muizen, en ze waren verspreid door de cortex in plaats van gegroepeerd in een specifieke laag of rondom plaques.
Niet alleen een reactie op plaques
Aangezien eiwitplaques bij de ziekte van Alzheimer sterke effecten hebben op nabijgelegen hersencellen, zou je verwachten dat deze astrocytesubgroepen hoofdzakelijk rond die afzettingen verschijnen. In plaats daarvan bleken de niveaus van STAT3- en NF-kB-activiteit in astrocyten niet afhankelijk van hoe dicht de cellen bij plaques stonden of hoe groot die plaques waren. Dezelfde drie astrocytetyperen waren al aanwezig in jongere muizen voordat veel plaques waren gevormd, en in normale muizen die nooit amyloïde ophoping ontwikkelen. Dit suggereert dat de verschillende astrocyteteams voortkomen uit ingebouwde, “hard‑wired” eigenschappen van de cellen, waarbij de ziekte vervolgens verandert wat elk team doet in plaats van geheel nieuwe types te creëren.
Verschillende vormen en huishoudelijke taken
De drie astrocyteteams verschilden niet alleen in hun signaalvoer, maar ook in hun vorm, moleculaire samenstelling en dagelijkse klusjes. Cellen die gedomineerd werden door de NF-kB-route dekten doorgaans een groter territorium in het weefsel en toonden sterkere activiteit van interne recyclingscompartimenten die eiwitten afbreken. STAT3-gedomineerde astrocyten waren daarentegen kleiner maar hadden meer actieve membraanpoorten, hemichannels genoemd, die de doorgang van kleine moleculen tussen de cel en haar omgeving regelen. Metingen van genactiviteit uit gefractioneerde cellen bevestigden dat elke groep een verschillend genprogramma activeerde, vooral genen die betrokken zijn bij ontsteking en bij het omgaan met en opruimen van eiwitten. In de Alzheimerachtige muizen werden deze moleculaire verschillen versterkt, waarbij sommige routes in STAT3-rijke cellen duidelijke tekenen van stress vertoonden.
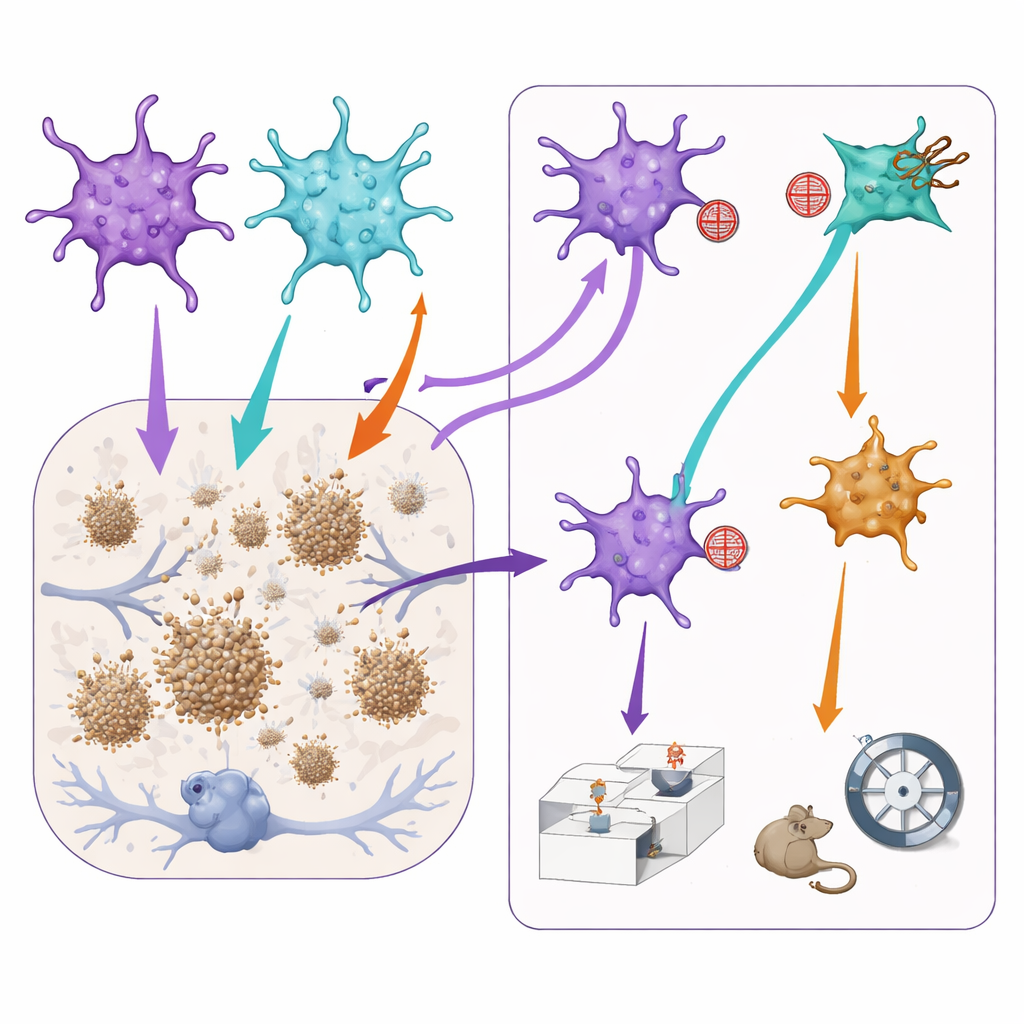
Het afstemmen van astrocytaire signalen verandert plaques en gedrag
Om te testen hoe deze subgroepen ziektekenmerken beïnvloeden, gebruikte het team vervolgens aanvullende virale hulpmiddelen om ofwel de STAT3- ofwel de NF-kB-signaalroute zachtjes te dempen, alleen in astrocyten waar die routes al actief waren. In Alzheimerachtige muizen leidde het blokkeren van de STAT3-route tot kleinere amyloïde plaques in de prefrontale cortex, wat suggereert dat STAT3-gedomineerde astrocyten mogelijk, direct of indirect, de groei van plaques bevorderen. Dezezelfde ingreep verergerde echter aspecten van sociaal geheugen: de muizen hadden meer moeite om een bekend exemplaar te onderscheiden van een nieuw exemplaar. Omgekeerd leek het verminderen van NF-kB-signaalgeving angstachtig gedrag licht te verlichten, maar verminderde het ook normale sociale interesse en geheugen. Belangrijk is dat dezelfde manipulaties in gezonde muizen weinig effect hadden, wat aangeeft dat deze astrocyteteams vooral invloedrijk worden in een ziek brein.
Wat dit betekent voor de ziekte van Alzheimer
Dit werk schetst een genuanceerder beeld van de ondersteunende cellen in de hersenen bij de ziekte van Alzheimer. In plaats van uniform te reageren, vallen astrocyten uiteen in onderscheiden functionele groepen die worden gedefinieerd door hun interne signaalcascades. Deze groepen verschillen in omvang, eiwitopruimingscapaciteit en in hoe ze communiceren met naburige cellen, en ze dragen verschillend bij aan plaquegroei en aan gedrag gerelateerd aan angst en sociale interactie. Voor toekomstige therapieën suggereert dit dat het in grote lijnen ‘op-’ of ‘afzetten’ van astrocyten te grofmazig kan zijn. In plaats daarvan kan het gericht moduleren van specifieke signaalroutes in geselecteerde astrocytesubpopulaties mogelijk ooit helpen het evenwicht te verfijnen tussen het beschermen van hersencircuits, het beperken van schadelijke eiwitophoping en het behouden van normaal gedrag.
Bronvermelding: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Trefwoorden: astrocyten, Ziekte van Alzheimer, hersen-signaaltransductie, neuro-inflammatie, eiwitopruiming