Clear Sky Science · it
Le cascate di segnalazione plasmano sottopopolazioni funzionali di astrociti corticali in topi maschi wild-type e nel modello di Alzheimer APP/PS1dE9
Aiutanti nascosti nel cervello
La malattia di Alzheimer viene spesso raccontata come la storia di neuroni malati e di ammassi proteici appiccicosi chiamati placche. Ma i neuroni non lavorano da soli. Sono circondati da cellule di supporto a forma di stella, gli astrociti, che silenziosamente mantengono in funzione i circuiti cerebrali. Questo studio mostra che anche tra queste cellule “aiutanti” esistono squadre distinte con compiti diversi, e che i loro sistemi di comunicazione interni possono influenzare sia l’accumulo di placche sia il comportamento in un modello murino della malattia di Alzheimer.
Squadre diverse di cellule di supporto
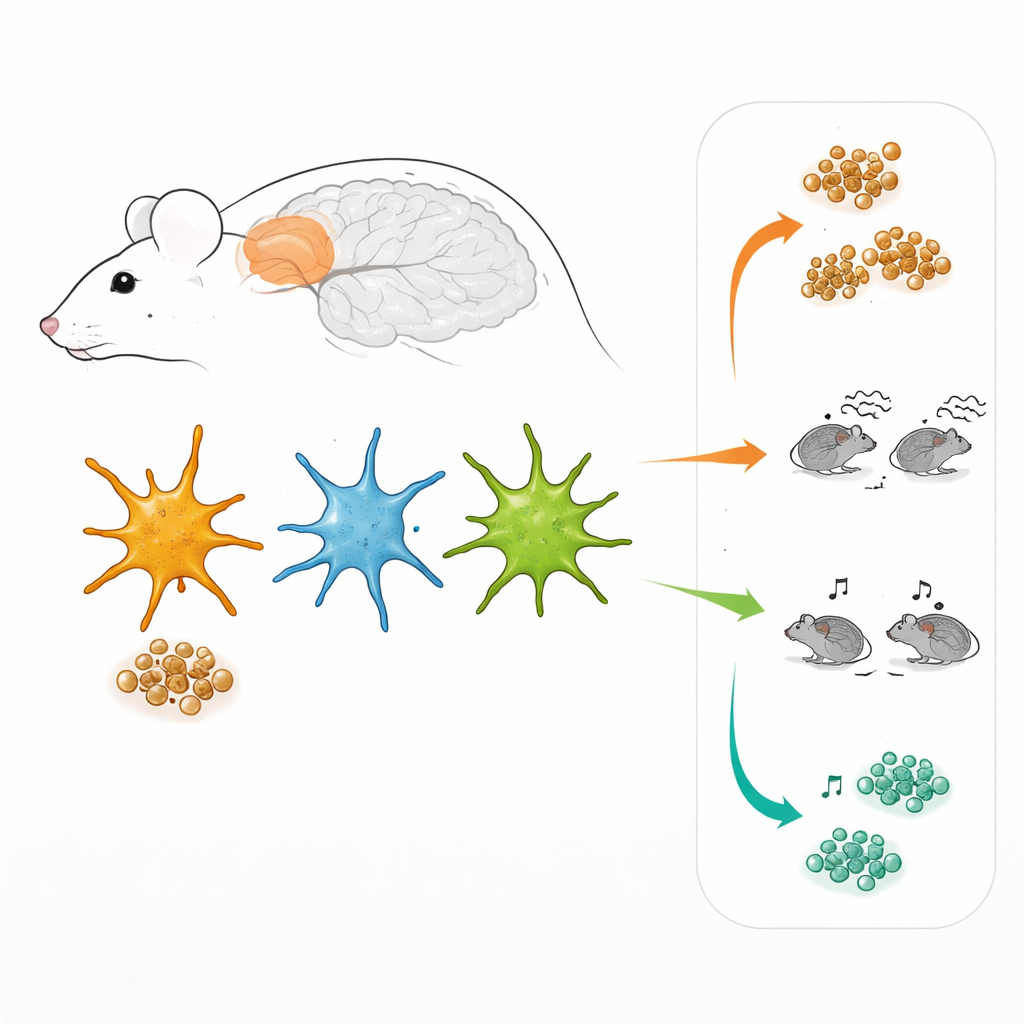
Gli astrociti non sono un gruppo uniforme. Lavorando nella corteccia prefrontale, una regione cerebrale coinvolta nel processo decisionale e nel comportamento sociale, i ricercatori hanno usato virus appositamente progettati per far “illuminare” gli astrociti quando erano attive due principali vie di segnalazione interne. Una via è controllata da un fattore chiamato STAT3, l’altra da NF-kB. Nei tessuti cerebrali vivi ciò ha permesso di “marcare” tre sottogruppi di astrociti: quelli che utilizzano principalmente la via STAT3, quelli che prediligono la via NF-kB e quelli che usano entrambe contemporaneamente. Sorprendentemente, questi tre gruppi erano presenti non solo nei topi con fenotipo simile all’Alzheimer ma anche nei topi sani, e risultavano distribuiti in tutta la corteccia piuttosto che raggruppati in uno strato particolare o intorno alle placche.
Non solo una reazione alle placche
Poiché le placche proteiche nella malattia di Alzheimer influenzano fortemente le cellule cerebrali vicine, si potrebbe pensare che questi sottogruppi di astrociti compaiano principalmente attorno a quei depositi. Invece, i livelli di attività di STAT3 e NF-kB negli astrociti non dipendevano da quanto le cellule fossero vicine alle placche né dalle dimensioni delle placche stesse. Gli stessi tre tipi di astrociti erano già presenti in topi più giovani, prima che molte placche si fossero formate, e in topi normali che non sviluppano accumuli di amiloide. Ciò suggerisce che le diverse “squadre” di astrociti derivano da proprietà intrinseche e “preimpostate” delle cellule, con la malattia che poi modifica ciò che ciascuna squadra fa piuttosto che creare tipi completamente nuovi.
Forme distinte e compiti di manutenzione
Le tre squadre di astrociti differivano non solo nella segnalazione, ma anche nella forma, nel profilo molecolare e nei compiti quotidiani. Le cellule dominate dalla via NF-kB tendevano a occupare un territorio più ampio nel tessuto e mostravano un’attività più intensa dei compartimenti di riciclo intracellulari che degradano le proteine. Gli astrociti dominati da STAT3, al contrario, erano più piccoli ma presentavano canali di membrana più attivi, detti emicanali, che regolano il passaggio di piccole molecole tra la cellula e l’ambiente circostante. Misurazioni dell’attività genica su cellule separate hanno confermato che ogni gruppo attivava un diverso insieme di geni, soprattutto quelli coinvolti nell’infiammazione e nella gestione e rimozione delle proteine. Nei topi simili all’Alzheimer queste differenze molecolari risultavano amplificate, con alcune vie nelle cellule ricche di STAT3 che mostravano chiari segni di stress.
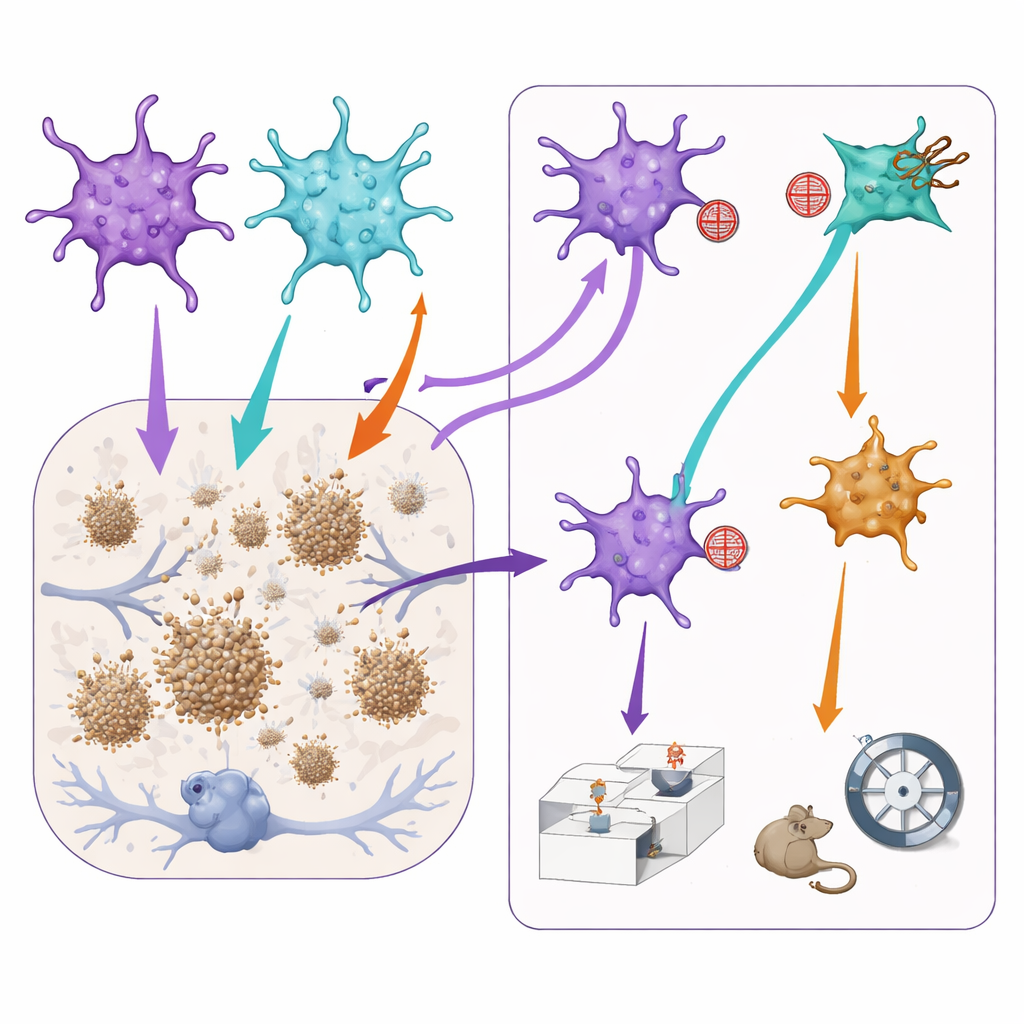
Modulare la segnalazione degli astrociti cambia placche e comportamento
Per verificare come questi sottogruppi influenzino i tratti della malattia, il gruppo ha poi usato ulteriori strumenti virali per attenuare delicatamente la segnalazione di STAT3 o di NF-kB solo negli astrociti in cui quelle vie erano già attive. Nei topi con fenotipo Alzheimer, bloccare la via STAT3 ha portato a placche amiloidi più piccole nella corteccia prefrontale, suggerendo che gli astrociti dominati da STAT3 possano, direttamente o indirettamente, favorire la crescita delle placche. Tuttavia, questa stessa manipolazione ha peggiorato alcuni aspetti della memoria sociale: i topi hanno avuto più difficoltà a distinguere un topo familiare da uno nuovo. Al contrario, ridurre la segnalazione NF-kB pareva alleviare lievemente comportamenti simili all’ansia ma riduceva anche l’interesse sociale e la memoria normali. È importante sottolineare che effettuare le stesse manipolazioni in topi sani ha avuto scarso effetto, indicando che queste «squadre» di astrociti diventano particolarmente influenti in un cervello malato.
Cosa significa per la malattia di Alzheimer
Questo lavoro dipinge un quadro più sfumato delle cellule di supporto del cervello nella malattia di Alzheimer. Piuttosto che rispondere in modo uniforme, gli astrociti si organizzano in gruppi funzionali distinti definiti dalle loro cascate di segnalazione interne. Questi gruppi differiscono per dimensioni, capacità di pulizia delle proteine e modalità di comunicazione con le cellule vicine, e contribuiscono in modo differente alla crescita delle placche e ai comportamenti legati all’ansia e all’interazione sociale. Per terapie future, ciò suggerisce che attivare o inibire gli astrociti in modo generale potrebbe essere troppo grossolano. Invece, mirare con precisione specifiche vie di segnalazione in sottopopolazioni selezionate di astrociti potrebbe un giorno aiutare a trovare un equilibrio tra protezione dei circuiti cerebrali, limitazione dell’accumulo proteico dannoso e preservazione del comportamento normale.
Citazione: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Parole chiave: astrociti, morbo di Alzheimer, segnalazione cerebrale, neuroinfiammazione, eliminazione delle proteine