Clear Sky Science · fr
Les cascades de signalisation façonnent des sous-populations fonctionnelles d’astrocytes corticaux chez des souris mâles sauvages et dans le modèle de la maladie d’Alzheimer APP/PS1dE9
Aides discrètes du cerveau
La maladie d’Alzheimer est souvent présentée comme une histoire de neurones malades et d’amas protéiques collants appelés plaques. Mais les neurones ne fonctionnent pas seuls. Ils sont entourés de cellules de soutien en forme d’étoile, les astrocytes, qui maintiennent discrètement le fonctionnement des circuits cérébraux. Cette étude montre que, même parmi ces cellules « assistantes », il existe des équipes distinctes avec des tâches différentes, et que leurs systèmes de communication internes peuvent influencer à la fois l’accumulation de plaques et le comportement dans un modèle murin de la maladie d’Alzheimer.
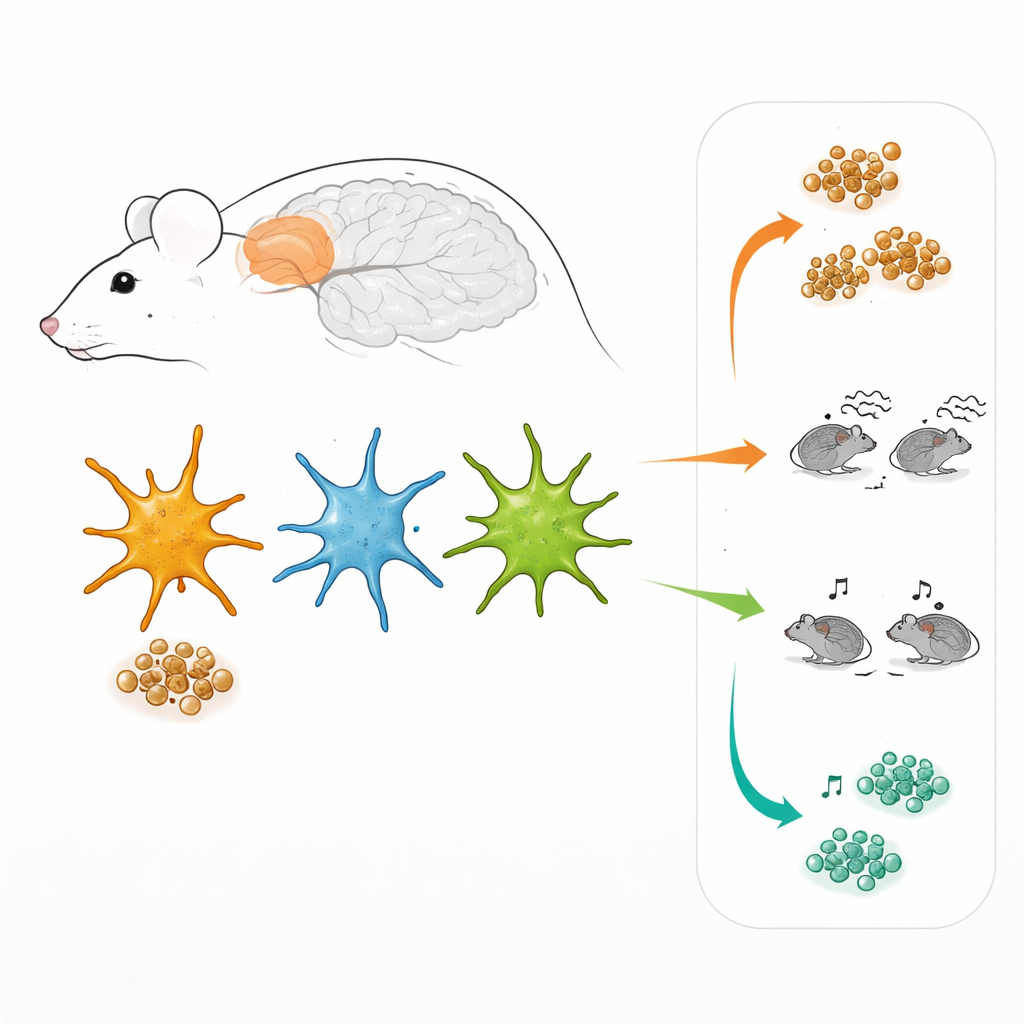
Équipes différentes de cellules de soutien
Les astrocytes ne forment pas un groupe uniforme. Travaillant dans le cortex préfrontal, une région cérébrale impliquée dans la prise de décision et le comportement social, les chercheurs ont utilisé des virus spécialement conçus pour faire s’allumer les astrocytes lorsque deux grandes voies de signalisation internes étaient actives. Une voie est contrôlée par un facteur appelé STAT3, l’autre par NF-kB. Dans le tissu cérébral vivant, cela leur a permis de « marquer » trois sous-groupes d’astrocytes : ceux utilisant principalement la voie STAT3, ceux utilisant principalement la voie NF-kB, et ceux utilisant les deux à la fois. Étonnamment, ces trois groupes étaient présents non seulement chez les souris de type Alzheimer, mais aussi chez les souris saines, et ils étaient disséminés dans tout le cortex plutôt que regroupés dans une couche particulière ou autour des plaques.
Pas seulement une réaction aux plaques
Parce que les plaques protéiques dans la maladie d’Alzheimer affectent fortement les cellules cérébrales voisines, on pourrait s’attendre à ce que ces sous-groupes d’astrocytes apparaissent principalement autour de ces dépôts. Au lieu de cela, les niveaux d’activité de STAT3 et de NF-kB dans les astrocytes ne dépendaient ni de la proximité des cellules par rapport aux plaques ni de la taille des plaques. Les mêmes trois types d’astrocytes étaient déjà présents chez les jeunes souris avant que de nombreuses plaques ne se forment, et chez des souris normales qui ne développent jamais d’accumulation d’amyloïde. Cela suggère que les différentes équipes d’astrocytes résultent de propriétés intrinsèques, « câblées » des cellules, la maladie modifiant ensuite ce que fait chaque équipe plutôt que de créer entièrement de nouveaux types.
Formes distinctes et tâches ménagères
Les trois équipes d’astrocytes différaient non seulement par leur signalisation, mais aussi par leur morphologie, leur composition moléculaire et leurs tâches quotidiennes. Les cellules dominées par la voie NF-kB avaient tendance à couvrir un territoire tissulaire plus large et montraient une activité plus forte des compartiments internes de recyclage qui dégradent les protéines. Les astrocytes dominés par STAT3, en revanche, étaient plus petits mais possédaient des « portes » membranaires plus actives appelées hémicanaux, qui régulent le passage de petites molécules entre la cellule et son environnement. Les mesures d’activité génique sur des cellules triées ont confirmé que chaque groupe activait un jeu différent de gènes, en particulier ceux impliqués dans l’inflammation et la gestion et l’élimination des protéines. Chez les souris modèles d’Alzheimer, ces différences moléculaires étaient amplifiées, certaines voies dans les cellules riches en STAT3 montrant des signes évidents de stress.
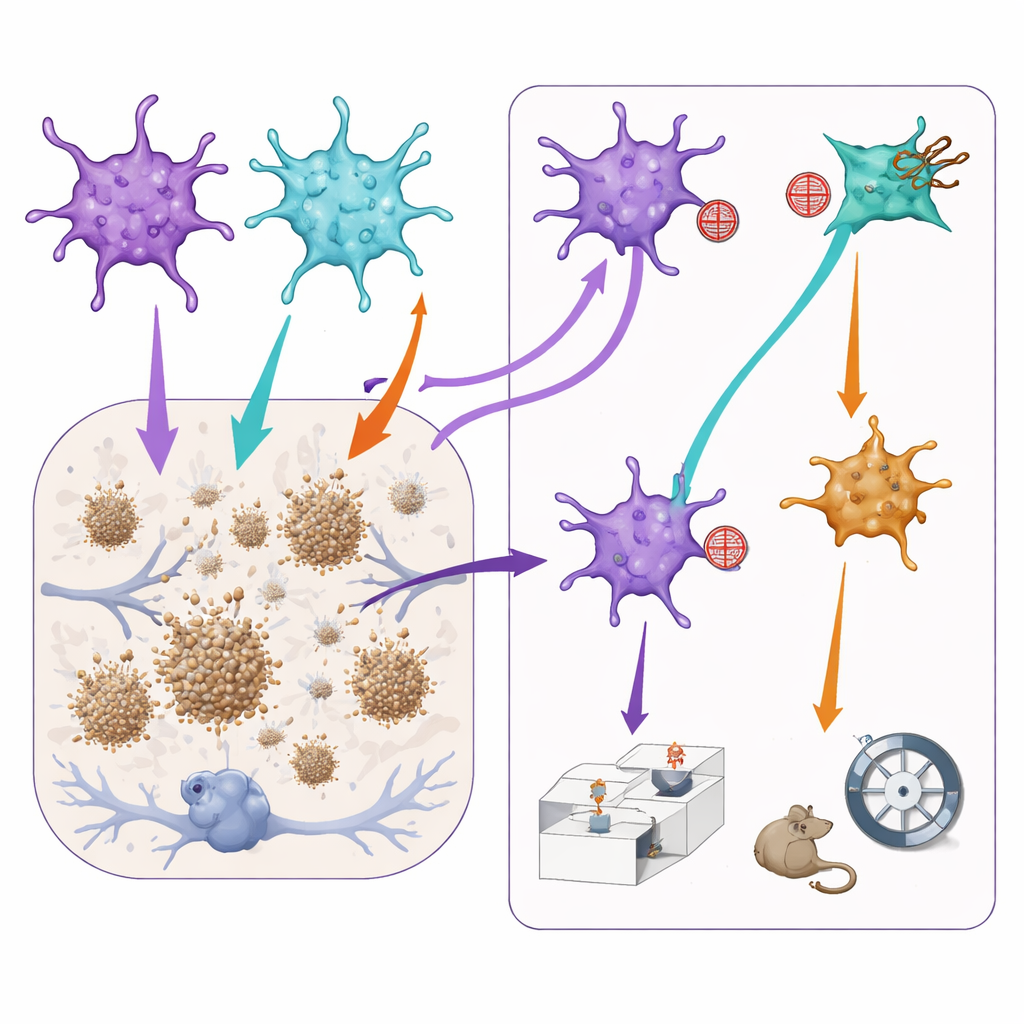
Moduler les signaux astrocytaires change plaques et comportement
Pour tester comment ces sous-groupes affectent les caractéristiques de la maladie, l’équipe a utilisé des outils viraux supplémentaires pour atténuer légèrement soit la signalisation STAT3 soit la signalisation NF-kB uniquement dans les astrocytes où ces voies étaient déjà actives. Chez les souris de type Alzheimer, bloquer la voie STAT3 a conduit à des plaques d’amyloïde plus petites dans le cortex préfrontal, suggérant que les astrocytes dominés par STAT3 peuvent, directement ou indirectement, favoriser la croissance des plaques. Cependant, cette même manipulation a aggravé certains aspects de la mémoire sociale : les souris avaient plus de mal à distinguer une souris familière d’une nouvelle. À l’inverse, réduire la signalisation NF-kB semblait soulager légèrement les comportements ressemblant à l’anxiété mais diminuait aussi l’intérêt social normal et la mémoire. Il est important de noter que réaliser les mêmes manipulations chez des souris saines avait peu d’effet, indiquant que ces équipes d’astrocytes deviennent particulièrement influentes dans un cerveau malade.
Ce que cela signifie pour la maladie d’Alzheimer
Ce travail dresse un portrait plus nuancé des cellules de soutien du cerveau dans la maladie d’Alzheimer. Plutôt que de répondre de manière uniforme, les astrocytes se répartissent en groupes fonctionnels distincts définis par leurs cascades de signalisation internes. Ces groupes diffèrent en taille, en capacité de nettoyage des protéines et dans leur façon de communiquer avec les cellules voisines, et ils contribuent différemment à la croissance des plaques ainsi qu’aux comportements liés à l’anxiété et aux interactions sociales. Pour les futures thérapies, cela suggère que stimuler ou inhiber globalement les astrocytes pourrait être trop grossier. À la place, cibler de manière précise certaines voies de signalisation dans des sous-populations sélectionnées d’astrocytes pourrait, un jour, aider à ajuster finement l’équilibre entre la protection des circuits cérébraux, la limitation de l’accumulation protéique nocive et la préservation du comportement normal.
Citation: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Mots-clés: astrocytes, maladie d’Alzheimer, signalisation cérébrale, neuroinflammation, élimination des protéines