Clear Sky Science · es
Las cascadas de señalización configuran subpoblaciones funcionales de astrocitos corticales en ratones macho de tipo salvaje y en el modelo de Alzheimer APP/PS1dE9
Ayudantes ocultos en el cerebro
La enfermedad de Alzheimer suele contarse como una historia de neuronas enfermas y grumos proteicos pegajosos llamados placas. Pero las neuronas no actúan solas. Están rodeadas por células de soporte con forma de estrella, los astrocitos, que mantienen en silencio el funcionamiento de los circuitos cerebrales. Este estudio muestra que incluso entre estas células “auxiliares” existen equipos distintos con tareas diferentes, y que sus sistemas de comunicación internos pueden influir tanto en la acumulación de placas como en el comportamiento en un modelo murino de la enfermedad de Alzheimer.
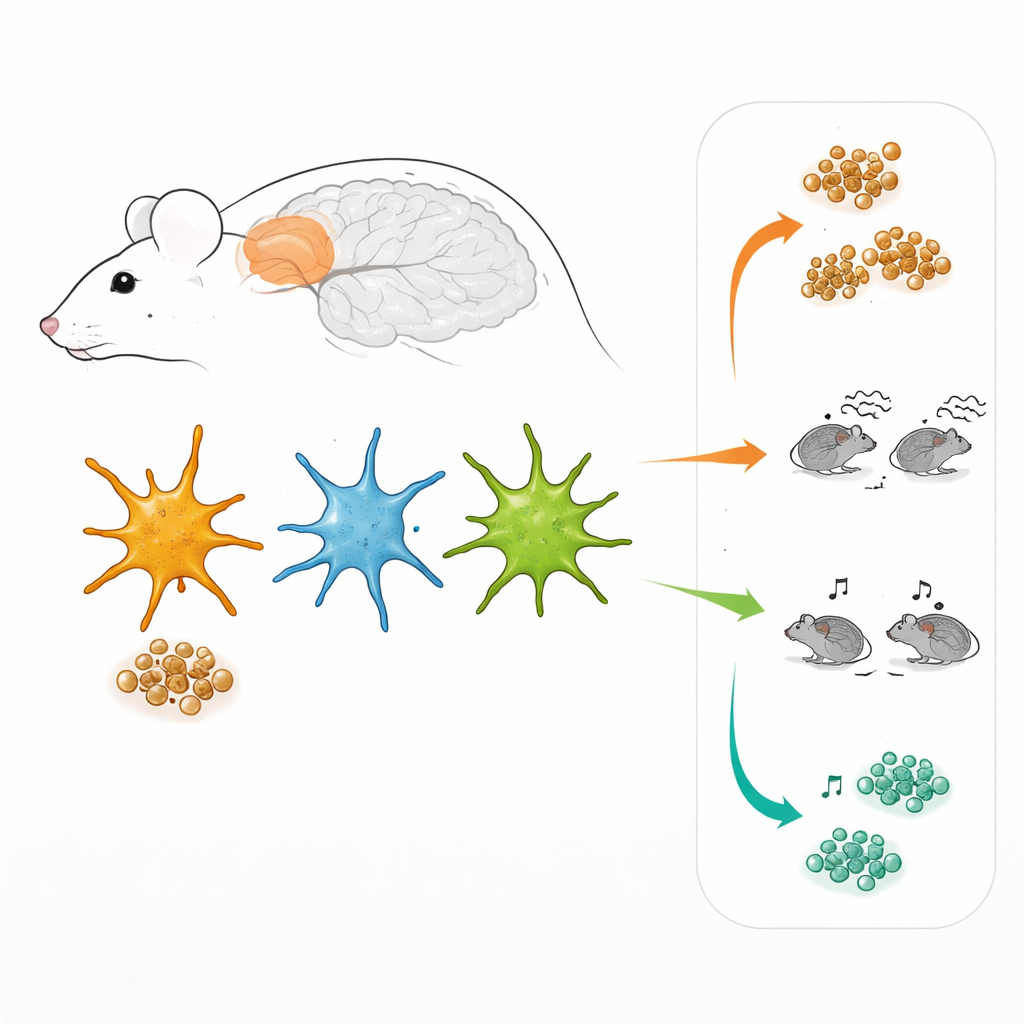
Diferentes equipos de células de soporte
Los astrocitos no son una multitud uniforme. Trabajando en la corteza prefrontal, una región cerebral implicada en la toma de decisiones y el comportamiento social, los investigadores utilizaron virus diseñados para que los astrocitos se iluminaran cuando dos rutas internas de señalización importantes estaban activas. Una ruta está controlada por un factor llamado STAT3, la otra por NF-kB. En tejido cerebral vivo, esto les permitió “marcar” tres subgrupos de astrocitos: los que usan principalmente la vía STAT3, los que usan principalmente la vía NF-kB y los que usan ambas a la vez. Sorprendentemente, estos tres grupos estaban presentes no solo en ratones con rasgos tipo Alzheimer sino también en ratones sanos, y se encontraban dispersos por toda la corteza en lugar de agruparse en una capa concreta o alrededor de las placas.
No solo una reacción a las placas
Dado que las placas proteicas en la enfermedad de Alzheimer afectan fuertemente a las células cerebrales cercanas, uno podría esperar que estos subgrupos de astrocitos aparecieran principalmente alrededor de esos depósitos. En cambio, los niveles de actividad de STAT3 y NF-kB en los astrocitos no dependían de la proximidad de las células a las placas ni del tamaño de estas. Los mismos tres tipos de astrocitos ya estaban presentes en ratones más jóvenes antes de que se formaran muchas placas, y en ratones normales que nunca desarrollan acumulación de amiloide. Esto sugiere que los distintos equipos de astrocitos surgen de propiedades intrínsecas, “cableadas” de antemano, y que la enfermedad modifica luego lo que hace cada equipo en lugar de crear tipos completamente nuevos.
Formas distintas y tareas de mantenimiento
Los tres equipos de astrocitos diferían no solo en su señalización, sino también en su forma, composición molecular y tareas cotidianas. Las células dominadas por la vía NF-kB tendían a abarcar un territorio mayor en el tejido y mostraban una actividad más intensa de los compartimentos internos de reciclaje que degradan proteínas. Los astrocitos dominados por STAT3, en contraste, eran más pequeños pero tenían más canales de membrana activos llamados hemicanales, que controlan el paso de pequeñas moléculas entre la célula y su entorno. Las mediciones de actividad génica en células separadas confirmaron que cada grupo activaba un conjunto distinto de genes, especialmente los implicados en la inflamación y en el manejo y eliminación de proteínas. En los ratones tipo Alzheimer, estas diferencias moleculares se amplificaron, con algunas vías en las células ricas en STAT3 mostrando claras señales de estrés.
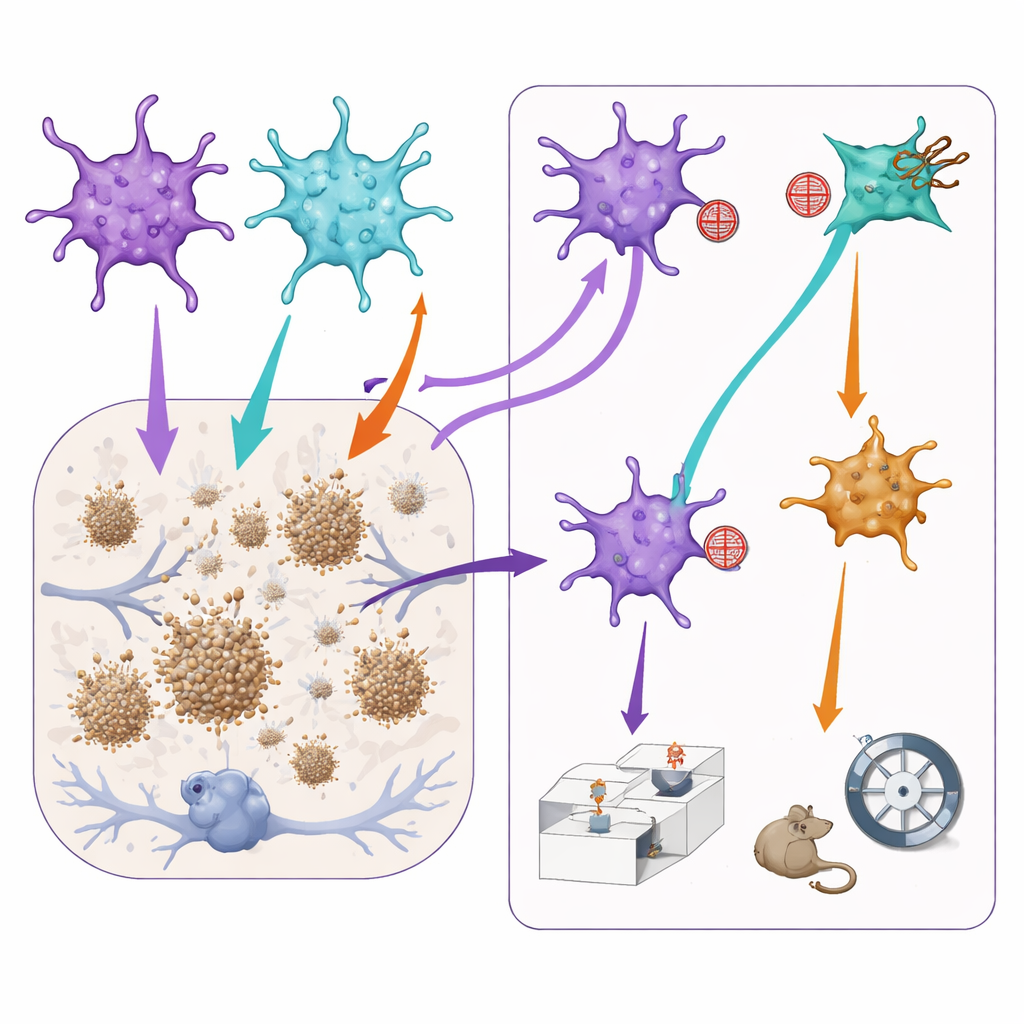
Modificar las señales de los astrocitos cambia placas y comportamiento
Para probar cómo afectan estos subgrupos a rasgos de la enfermedad, el equipo usó herramientas virales adicionales para atenuar suavemente ya sea la señalización STAT3 o NF-kB únicamente en los astrocitos donde esas vías ya estaban activas. En los ratones tipo Alzheimer, bloquear la vía STAT3 produjo placas de amiloide más pequeñas en la corteza prefrontal, lo que sugiere que los astrocitos dominados por STAT3 pueden, directa o indirectamente, favorecer el crecimiento de placas. Sin embargo, esa misma manipulación empeoró aspectos de la memoria social: los ratones tuvieron más dificultad para distinguir un ratón familiar de uno nuevo. Por el contrario, reducir la señalización NF-kB pareció aliviar ligeramente comportamientos de tipo ansioso pero también redujo el interés social y la memoria normales. Es importante destacar que realizar las mismas manipulaciones en ratones sanos tuvo poco efecto, lo que indica que estos equipos de astrocitos se vuelven especialmente influyentes en un cerebro enfermo.
Qué significa esto para la enfermedad de Alzheimer
Este trabajo ofrece una imagen más matizada de las células de soporte del cerebro en la enfermedad de Alzheimer. En lugar de responder de forma uniforme, los astrocitos se dividen en grupos funcionales definidos por sus cascadas internas de señalización. Estos grupos difieren en tamaño, capacidad de limpieza de proteínas y en cómo se comunican con las células vecinas, y contribuyen de manera distinta al crecimiento de placas y a conductas relacionadas con la ansiedad y la interacción social. Para futuras terapias, esto sugiere que activar o inhibir los astrocitos de forma general puede ser demasiado tosco. En su lugar, dirigir con cuidado rutas de señalización específicas en subpoblaciones seleccionadas de astrocitos podría algún día ayudar a ajustar el equilibrio entre proteger los circuitos cerebrales, limitar la acumulación dañina de proteínas y preservar el comportamiento normal.
Cita: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
Palabras clave: astrocitos, enfermedad de Alzheimer, señalización cerebral, neuroinflamación, eliminación de proteínas