Clear Sky Science · ar
مسارات الإشارة تشكل الفئات الوظيفية الفرعية للخلايا النجمية القشرية في ذكور الفئران البرية ونموذج مرض ألزهايمر APP/PS1dE9
مساعدون مخفيون في الدماغ
غالبًا ما يُروى مرض ألزهايمر كقصة عن خلايا عصبية مريضة وتكتلات بروتينية لزجة تسمى اللويحات. لكن الخلايا العصبية لا تعمل بمفردها. تحيط بها خلايا داعمة على شكل نجمي تُسمى الخلايا النجمية، والتي تحافظ بهدوء على عمل الدوائر الدماغية. تُظهر هذه الدراسة أن حتى بين هذه الخلايا «المساعدة» هناك فرق مميزة تقوم بمهام مختلفة، وأن أنظمة الاتصال الداخلية لديها يمكن أن تؤثر على تراكم اللويحات وعلى السلوك في نموذج فأري لمرض ألزهايمر.
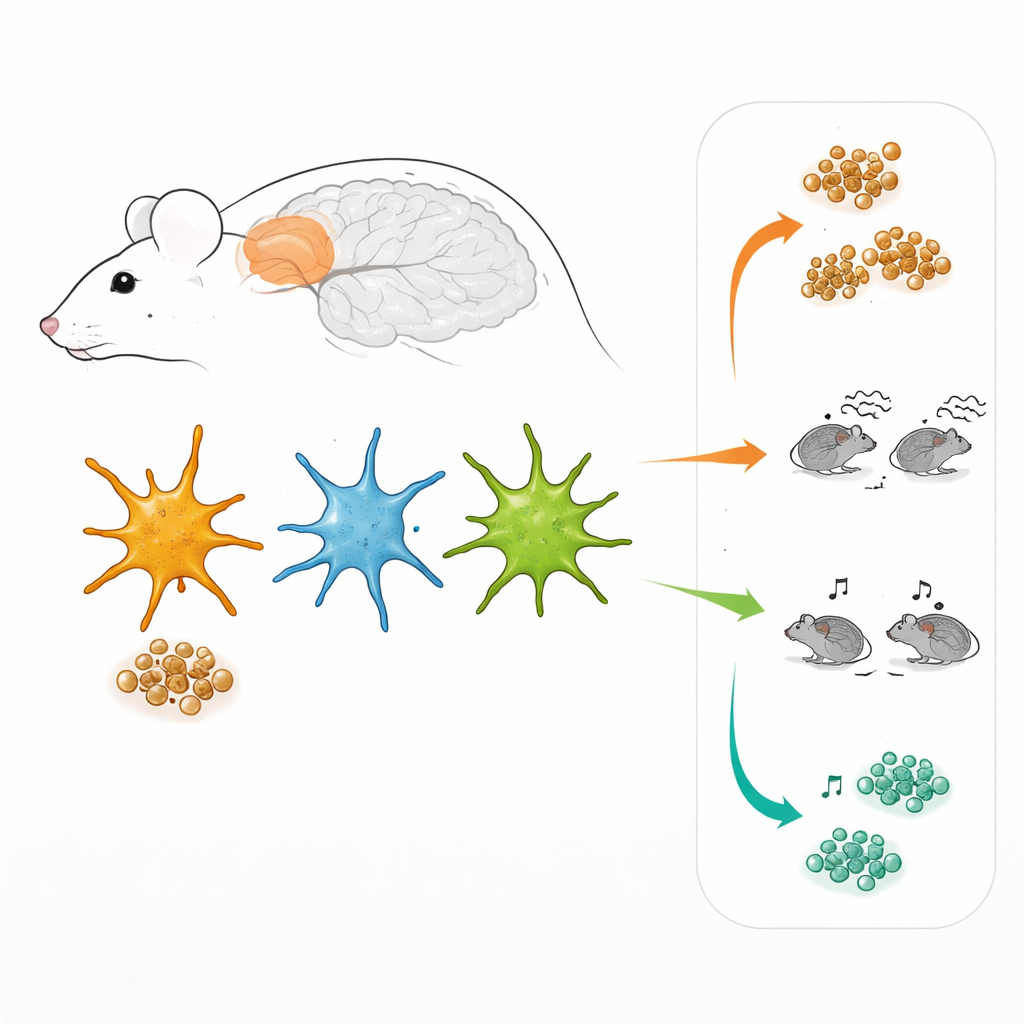
فرق مختلفة من الخلايا الداعمة
الخلايا النجمية ليست مجموعة متجانسة. في القشرة أمام الجبهية، وهي منطقة دماغية تشارك في اتخاذ القرار والسلوك الاجتماعي، استخدم الباحثون فيروسات مصممة خصيصًا لجعل الخلايا النجمية تتوهج عندما تكون مسارا إشارات داخليان رئيسيان نشطان. يتحكم في أحد المسارين عامل يدعى STAT3، وفي الآخر NF-kB. ضمن نسيج الدماغ الحي، سمح ذلك لهم بـ «وسم» ثلاث مجموعات فرعية من الخلايا النجمية: تلك التي تستخدم مسار STAT3 بصورة أساسية، وتلك التي تعتمد أساسًا على مسار NF-kB، وتلك التي تستخدم كلا المسارين معًا. ومن المدهش أن هذه المجموعات الثلاث وُجدت ليس فقط في الفئران الشبيهة بألزهايمر ولكن أيضًا في الفئران السليمة، وكانت مبعثرة في القشرة بدلاً من أن تتجمع في طبقة معينة أو حول اللويحات.
ليست مجرد استجابة للويحات
بما أن اللويحات البروتينية في مرض ألزهايمر تؤثر بقوة على الخلايا المحيطة بها، قد يتوقع المرء أن تظهر هذه المجموعات الفرعية من الخلايا النجمية بالأساس حول تلك الترسبات. بدلًا من ذلك، لم تعتمد مستويات نشاط STAT3 وNF-kB في الخلايا النجمية على مدى قرب الخلايا من اللويحات أو على حجم اللويحات. كانت نفس أنواع الخلايا النجمية الثلاثة موجودة بالفعل في فئران أصغر سنًا قبل تكون العديد من اللويحات، وفي فئران طبيعية لا تتطور لديها تراكمات أميلويدية أبدًا. هذا يشير إلى أن فرق الخلايا النجمية الناشئة تنبع من خصائص مدمجة و«مُبرمجة» داخل الخلايا، مع قيام المرض بعد ذلك بتعديل ما تفعله كل مجموعة بدلاً من خلق أنواع جديدة تمامًا.
أشكال ووظائف منزلية مميزة
اختلفت المجموعات الثلاث من الخلايا النجمية ليس فقط في إشاراتها، بل أيضًا في شكلها وتركيبها الجزيئي وأعمالها اليومية. الخلايا التي يهيمن عليها مسار NF-kB كانت تميل إلى تغطية مساحة أكبر داخل النسيج وأظهرت نشاطًا أقوى للحاويات الداخلية لإعادة التدوير التي تكسر البروتينات. أما الخلايا النجمية المهيمنة عليها STAT3 فكانت أصغر حجمًا لكنها امتلكت «بوابات» غشائية نشطة أكثر تُسمى القنوات النصفية، التي تتحكم في مرور الجزيئات الصغيرة بين الخلية وبيئتها. أكدت مقاييس نشاط الجينات من خلايا مصنفة أن كل مجموعة تُفعل مجموعة مختلفة من الجينات، خاصة تلك المشاركة في الالتهاب والتعامل مع البروتين وتنظيفه. وفي الفئران الشبيهة بألزهايمر، تضخمت هذه الاختلافات الجزيئية، حيث أظهرت بعض المسارات في الخلايا الغنية بـ STAT3 علامات واضحة على الإجهاد.
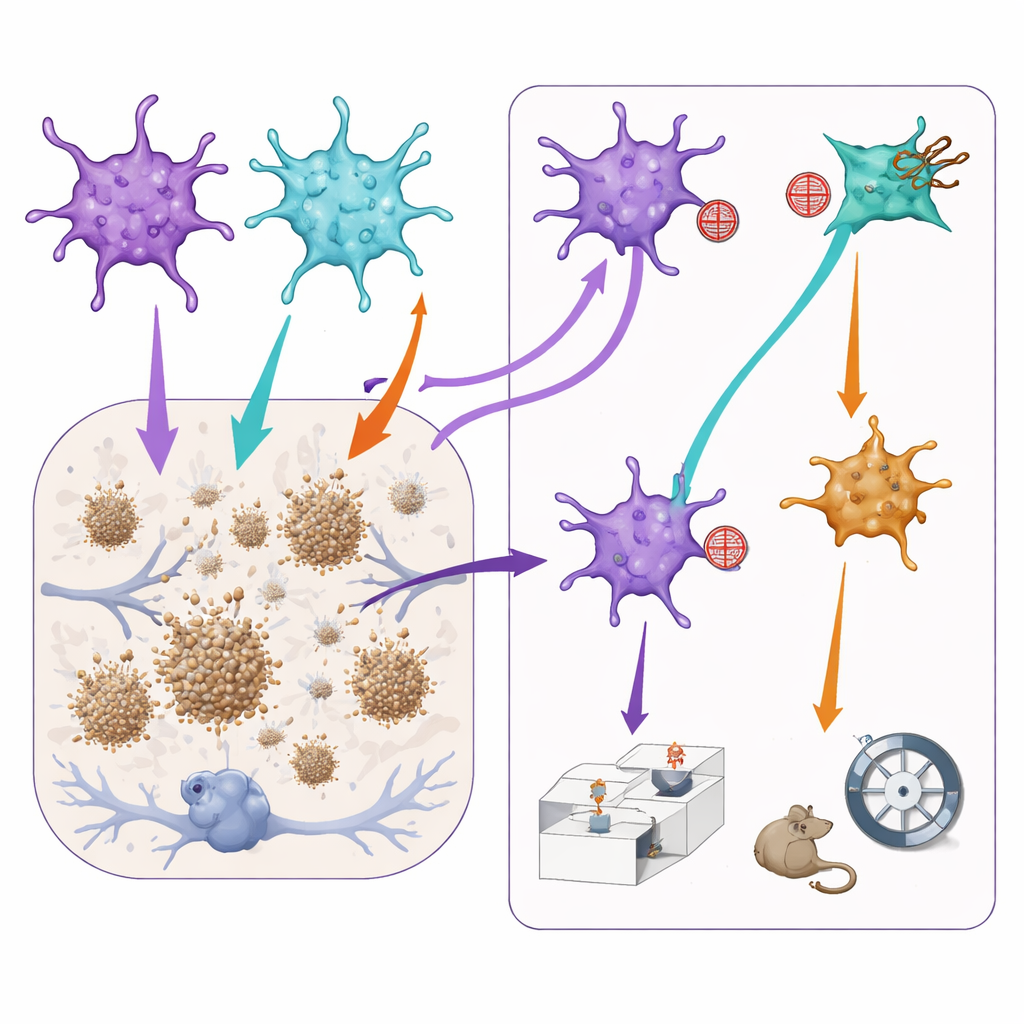
تعديل إشارات الخلايا النجمية يغير اللويحات والسلوك
لاختبار كيف تؤثر هذه المجموعات الفرعية على سمات المرض، استخدم الفريق أدوات فيروسية إضافية لتقليل نشاط إما مسار STAT3 أو NF-kB برفق فقط في الخلايا النجمية التي كانت تلك المسارات نشطة بالفعل. في الفئران الشبيهة بألزهايمر، أدى حجب مسار STAT3 إلى صغر حجم لويحات الأميلويد في القشرة أمام الجبهية، مما يوحي بأن الخلايا النجمية المهيمنة عليها STAT3 قد تساعد، بشكل مباشر أو غير مباشر، في نمو اللويحات. مع ذلك، أدى نفس التعديل إلى تدهور جوانب الذاكرة الاجتماعية: واجهت الفئران صعوبة أكبر في التمييز بين فأر مألوف وآخر جديد. وبالمقابل، بدا أن تقليل إشارات NF-kB يخفف قليلاً من سلوك يشبه القلق لكنه أيضًا قلل الاهتمام الاجتماعي والذاكرة الطبيعية. ومن المهم أن تنفيذ نفس التعديلات في الفئران السليمة كان له تأثير ضئيل، مما يشير إلى أن هذه الفرق من الخلايا النجمية تصبح مؤثرة بشكل خاص في الدماغ المريض.
ما الذي يعنيه هذا لمرض ألزهايمر
تُقدم هذه العمل صورة أكثر دقة لخلايا الدعم في الدماغ عند مرض ألزهايمر. فبدلاً من الاستجابة بطريقة موحدة، تنقسم الخلايا النجمية إلى مجموعات وظيفية مميزة تحددها مسارات الإشارة الداخلية. تختلف هذه المجموعات في الحجم وقدرات تنظيف البروتين، وفي كيفية تواصلها مع الخلايا المجاورة، وهي تسهم بطرق مختلفة في نمو اللويحات وفي السلوكيات المتعلقة بالقلق والتفاعل الاجتماعي. ولعلاجات المستقبل، يشير ذلك إلى أن رفع أو خفض نشاط الخلايا النجمية بشكل عام قد يكون إجراءً غير دقيق. وبدلاً من ذلك، قد يساعد استهداف مسارات إشارات محددة داخل مجموعات فرعية مختارة من الخلايا النجمية في يوم ما على ضبط التوازن بين حماية دوائر الدماغ، والحد من تراكم البروتين الضار، والحفاظ على السلوك الطبيعي.
الاستشهاد: Poulot-Becq-Giraudon, Y., Guillemaud, O., Degl’Innocenti, E. et al. Signaling cascades shape functional subpopulations of cortical astrocytes in male wild-type mice and APP/PS1dE9 Alzheimer’s disease model. Nat Commun 17, 4194 (2026). https://doi.org/10.1038/s41467-026-71826-w
الكلمات المفتاحية: الخلايا النجمية, مرض ألزهايمر, إشارات الدماغ, الالتهاب العصبي, تنقية البروتين