Clear Sky Science · pl
MSF-VMDNet do wieloklasowej segmentacji obrazów całego preparatu skóry przy użyciu sieci z podwójnym enkoderem i wieloczęstotliwościową analizą
Dlaczego mapowanie raka skóry ma znaczenie
Gdy lekarze rozpoznają raka skóry, często oglądają ultradokładne obrazy mikroskopowe zabarwionych skrawków tkanki. Zdjęcia te pokazują nie tylko nowotwór, lecz także wiele rodzajów prawidłowych struktur skórnych ściśle ze sobą splecionych. Ręczne rysowanie precyzyjnych granic każdej z tych stref jest czasochłonne i może się różnić w zależności od specjalisty. W tym badaniu zaprezentowano nową metodę komputerową, zaprojektowaną do automatycznego rozdzielania tych splątanych tkanek z bardzo wysoką dokładnością, co może oszczędzać czas i ujednolicać diagnozy.
Od prostych plam do splecionej tkanki
Rak skóry należy do najczęściej występujących nowotworów na świecie, częściowo z powodu zwiększonej ekspozycji na promieniowanie ultrafioletowe. Nowoczesne rozpoznanie zwykle zaczyna się od dermoskopii — specjalnego, powiększonego zdjęcia skóry — a często kontynuuje biopsją: niewielki fragment skóry jest usuwany, barwiony i badany pod mikroskopem. Na tych obrazach całych preparatów guzy przebiegają przez warstwy takie jak naskórek, głębsza tkanka łączna, mieszki włosowe, gruczoły potowe i tkanka tłuszczowa. Wiele z tych obszarów ma podobne kolory i tekstury, a ich granice mogą być rozmyte, co utrudnia nawet ekspertom jednoznaczne odróżnienie guza od tkanki zdrowej.
Nowy sposób odczytywania złożonych obrazów
Większość wcześniejszych narzędzi komputerowych traktowała problem jak kolorowanie obrazu dwoma kredkami: „zmiana” i „brak zmiany”. To może działać dla prostszych zdjęć powierzchniowych, ale zawodzi, gdy preparat trzeba podzielić jednocześnie na wiele typów tkanek. Autorzy koncentrują się na wymagającym zbiorze danych dotyczących raków skóry niezwiązanych z czerniakiem, w którym każdy obraz trzeba rozdzielić nawet na dziesięć odrębnych klas tkanek. Ich celem jest zbudowanie systemu, który potrafi zrozumieć ogólny układ tkanki, jednocześnie wychwytując drobne detale przy granicach — coś, z czym tradycyjne sieci neuronowe często mają trudność w znalezieniu równowagi.
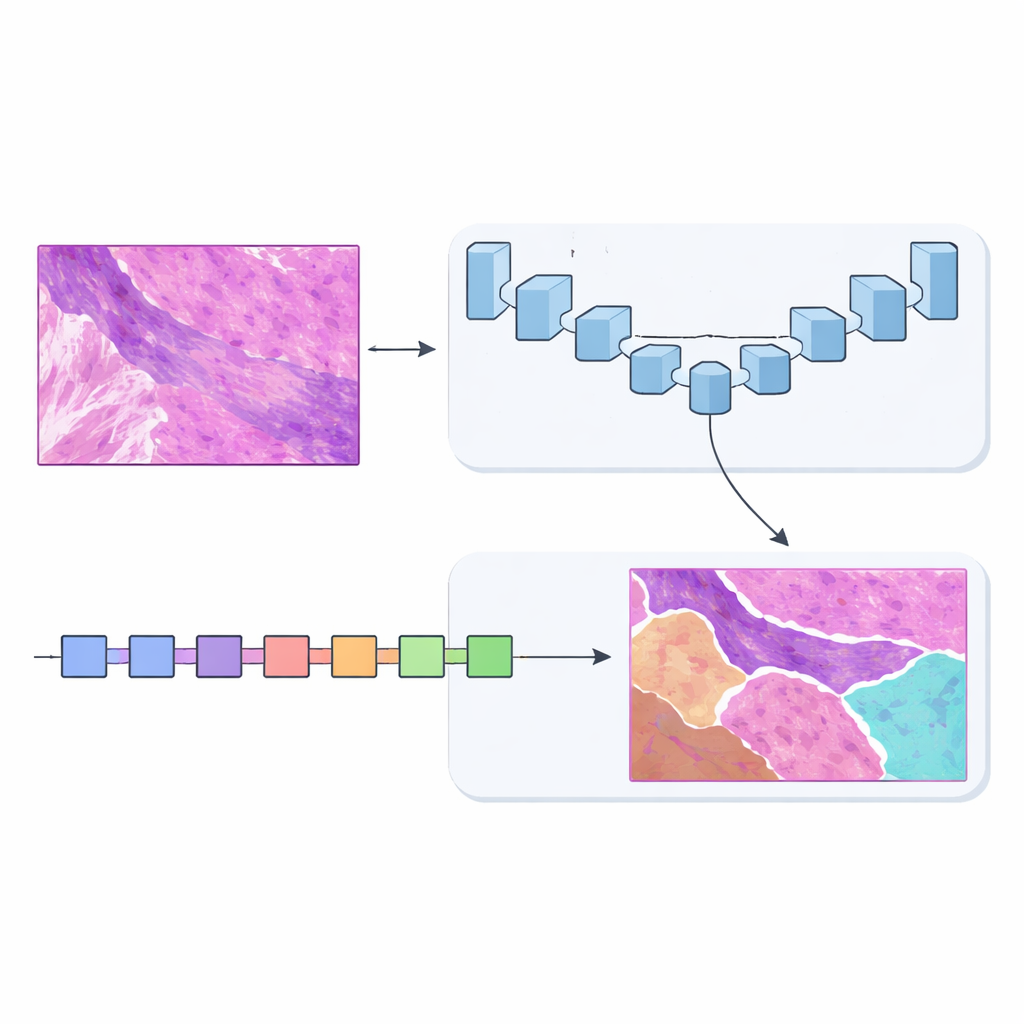
Dwie „inteligencje” zamiast jednej
Aby to rozwiązać, zespół zaprojektował MSF‑VMDNet — sieć z podwójnym enkoderem, którą można sobie wyobrazić jako dwa uzupełniające się „mózgi” analizujące ten sam preparat równolegle. Jeden oddział oparto na U‑Net, popularnym modelu w obrazowaniu medycznym, świetnym w uchwyceniu drobnych lokalnych detali. Autorzy wzbogacili go o moduł spektralny, który przekształca obraz w zbiór częstotliwości — niektóre opisują wolne, płynne zmiany, inne wychwytują ostre krawędzie i tekstury — a następnie scala je, by wzmocnić granice klas. Jednocześnie drugi oddział, zbudowany na nowszym podejściu zwanym Vision Mamba, skanuje preparat w bardziej uproszczony sposób, efektywnie modelując długozasięgowe relacje, tak aby odległe, lecz powiązane obszary mogły się wzajemnie informować.
Słuchanie wielu częstotliwości naraz
Informacja o częstotliwościach odgrywa centralną rolę w tej architekturze. Przechodząc między zwykłą przestrzenią obrazu a widokiem opartym na częstotliwościach, sieć może traktować szerokie formy i drobne struktury inaczej. Składowe niskoczęstotliwościowe pomagają zrozumieć ogólny układ guza i otaczających warstw skóry, podczas gdy składowe wysokoczęstotliwościowe wyostrzają krawędzie, gdzie jeden typ tkanki kończy się, a zaczyna inny. Starannie zaprojektowane moduły łączą te widoki z powrotem w mapę przestrzenną, a dodatkowy blok dekodujący (zwany SCConv) filtruje redundantne sygnały przy jednoczesnym wzmacnianiu naprawdę informacyjnych wzorców. Efektem jest czyściejsza, bardziej pewna mapa każdego obszaru tkanki.
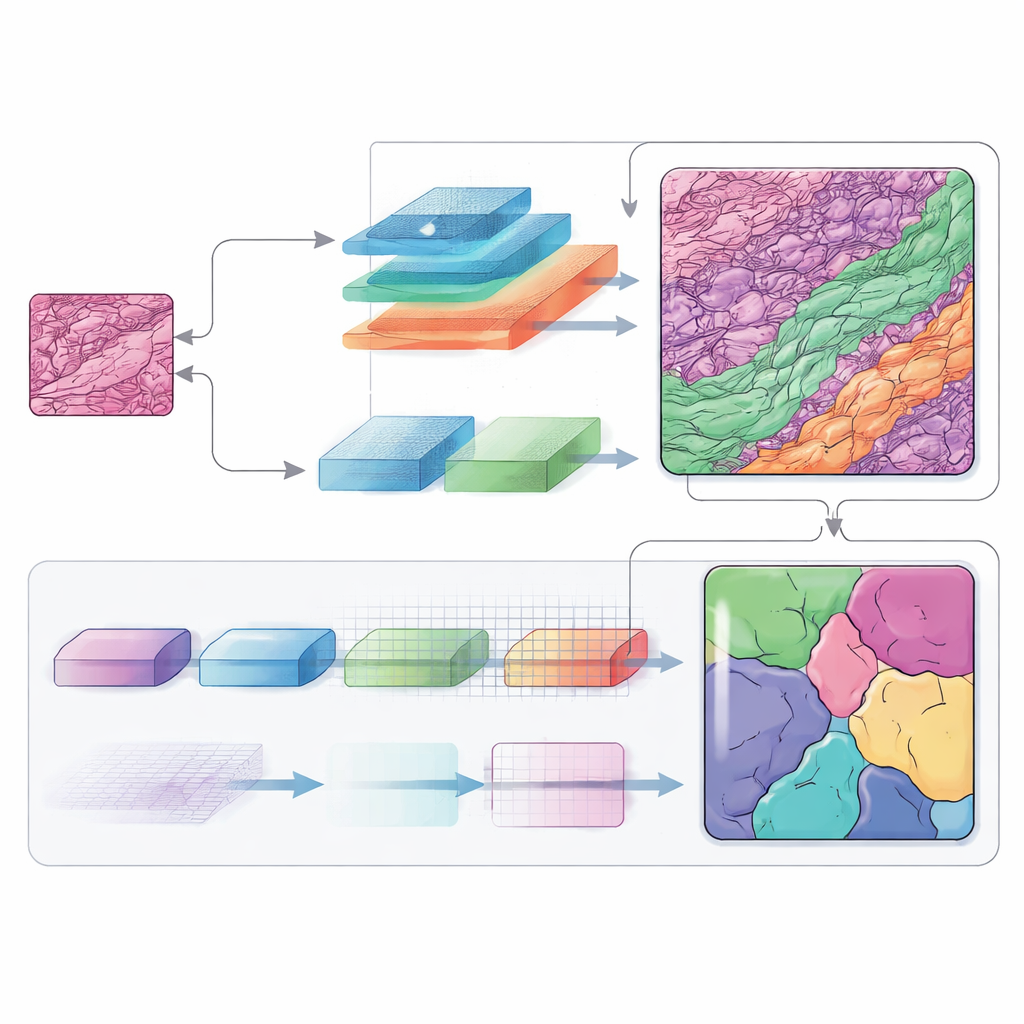
Jak dobrze to działa w praktyce?
Naukowcy przetestowali MSF‑VMDNet na zbiorze danych raka skóry niezwiązanego z czerniakiem i porównali go z szerokim zestawem wiodących modeli segmentacyjnych, w tym klasycznym U‑Net, metodami opartymi na Transformerach oraz innymi hybrydami Vision Mamba. Ich system wygenerował wyraźniejsze kontury nowotworu i mniej błędów w trudnych obszarach, gdzie guz, mieszki włosowe i tkanka zapalna są ze sobą splecione. W standardowych miarach nakładania przewyższył wszystkich konkurentów, osiągając około 95 procent zgodności z maskami narysowanymi przez ekspertów. Aby sprawdzić, czy metoda uogólnia się poza jedno laboratorium i jeden rodzaj nowotworu, zespół ocenił ją także na trzech dodatkowych zbiorach: zdjęciach dermoskopowych zmian skórnych, obrazach mikroskopowych różnych rodzajów jąder komórkowych oraz skanach CT narządów jamy brzusznej. We wszystkich przypadkach metoda pozostała wysoce dokładna i statystycznie przewyższała silne bazowe metody.
Co to oznacza dla pacjentów i lekarzy
W prostych słowach, MSF‑VMDNet to zautomatyzowany „twórca map” obrazów medycznych, który potrafi oddzielić guzy od zatłoczonego krajobrazu prawidłowej tkanki z niecodzienną precyzją. Choć nie zastępuje oceny patologa, może dostarczyć szybki, szczegółowy punkt wyjścia, zmniejszając nakład ręcznej pracy i pomagając zapewnić, że subtelne obszary nowotworowe nie zostaną pominięte. Ponieważ to samo podejście działa dobrze na bardzo różnych typach obrazów medycznych, może stać się wszechstronnym narzędziem do wielu zadań diagnostycznych. Przy dalszym rozwoju i integracji informacji klinicznej systemy tego typu mogą wspierać bardziej wiarygodne stopniowanie raka skóry i ostatecznie lepiej poinformowany dobór terapii.
Cytowanie: Zhang, J., Pu, Q., Tian, J. et al. MSF-VMDNet for multi class segmentation of skin cancer whole slide images using a multi frequency dual encoder network. Sci Rep 16, 11722 (2026). https://doi.org/10.1038/s41598-026-40044-1
Słowa kluczowe: obrazowanie raka skóry, segmentacja obrazów medycznych, uczenie głębokie w patologii, analiza histopatologiczna, diagnostyka AI