Clear Sky Science · nl
MSF-VMDNet voor multiclass-segmentatie van hele slide-beelden van huidkanker met een multi-frequentie dual-encoder netwerk
Waarom het in kaart brengen van huidkanker ertoe doet
Wanneer artsen huidkanker diagnosticeren, bekijken ze vaak uiterst gedetailleerde microscoopbeelden van gekleurde weefselplakjes. Deze afbeeldingen tonen niet alleen de tumor, maar ook vele soorten normaal huidweefsel die nauw met elkaar zijn verweven. Het met de hand nauwkeurig afbakenen van elk gebied is traag en kan variëren per specialist. Deze studie presenteert een nieuwe computermethode die is ontworpen om deze verwarde weefsels automatisch en met hoge nauwkeurigheid te onderscheiden, wat tijd kan besparen en diagnoses consistenter kan maken.
Van eenvoudige vlekken tot verstrengeld weefsel
Huidkanker behoort tot de meest voorkomende vormen van kanker wereldwijd, mede door toenemende blootstelling aan ultraviolet licht. De moderne diagnose begint meestal met dermoscopie, een vergrote huidfoto, en gaat vaak verder met een biopsie: een klein stukje huid wordt verwijderd, gekleurd en onder de microscoop onderzocht. In deze hele-slide beelden slingeren tumoren door lagen zoals de opperhuid, dieper liggend bindweefsel, haarzakjes, zweetklieren en vet. Veel van deze gebieden lijken qua kleur en textuur op elkaar en hun grenzen kunnen vaag zijn, waardoor het zelfs voor experts lastig is om tumor en gezond weefsel duidelijk te scheiden.
Een nieuwe manier om complexe beelden te lezen
De meeste eerdere computertools behandelden het probleem alsof je een afbeelding met slechts twee kleuren inkleurde: "laesie" en "geen laesie." Dat kan werken voor eenvoudiger oppervlakkige foto’s, maar faalt wanneer een slide in veel weefseltypen tegelijk moet worden verdeeld. De auteurs richten zich op een uitdagende dataset van non-melanoma huidkankers waarbij elke afbeelding in tot wel tien verschillende weefselklassen moet worden opgesplitst. Hun doel is een systeem te bouwen dat zowel het algemene weefselpatroon begrijpt als kleine details langs de randen opvangt—iets waar traditionele neurale netwerken vaak moeite mee hebben een balans in te vinden.
Twee breinen zijn beter dan één
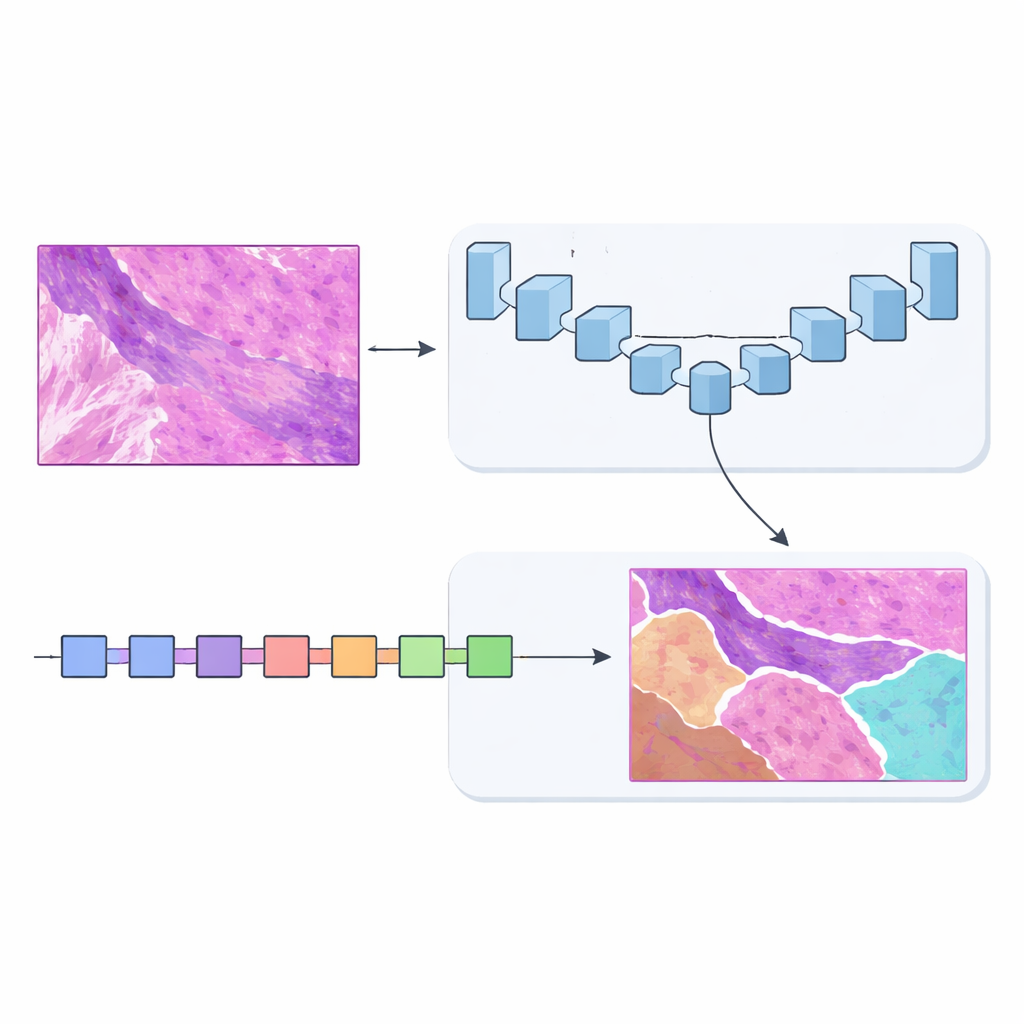
Om dit op te lossen ontwierp het team MSF‑VMDNet, een dual-encoder netwerk dat kan worden gezien als twee complementaire "breinen" die dezelfde slide parallel onderzoeken. De ene tak is gebaseerd op U‑Net, een populair medisch-beeldvormingmodel dat uitstekend is in het vastleggen van fijne lokale details. De auteurs breiden dit uit met een spectraal module die het beeld omzet in een verzameling frequenties—sommige beschrijven langzame, vloeiende veranderingen, andere leggen scherpe randen en texturen vast—en deze vervolgens weer combineert om klassegrenzen te versterken. Tegelijk scant een tweede tak, gebouwd op een nieuwere benadering genaamd Vision Mamba, de slide op een meer gestroomlijnde manier en modelleert efficiënt langeafstandsrelaties zodat verafgelegen maar gerelateerde gebieden elkaar kunnen informeren.
Naar veel frequenties tegelijk luisteren
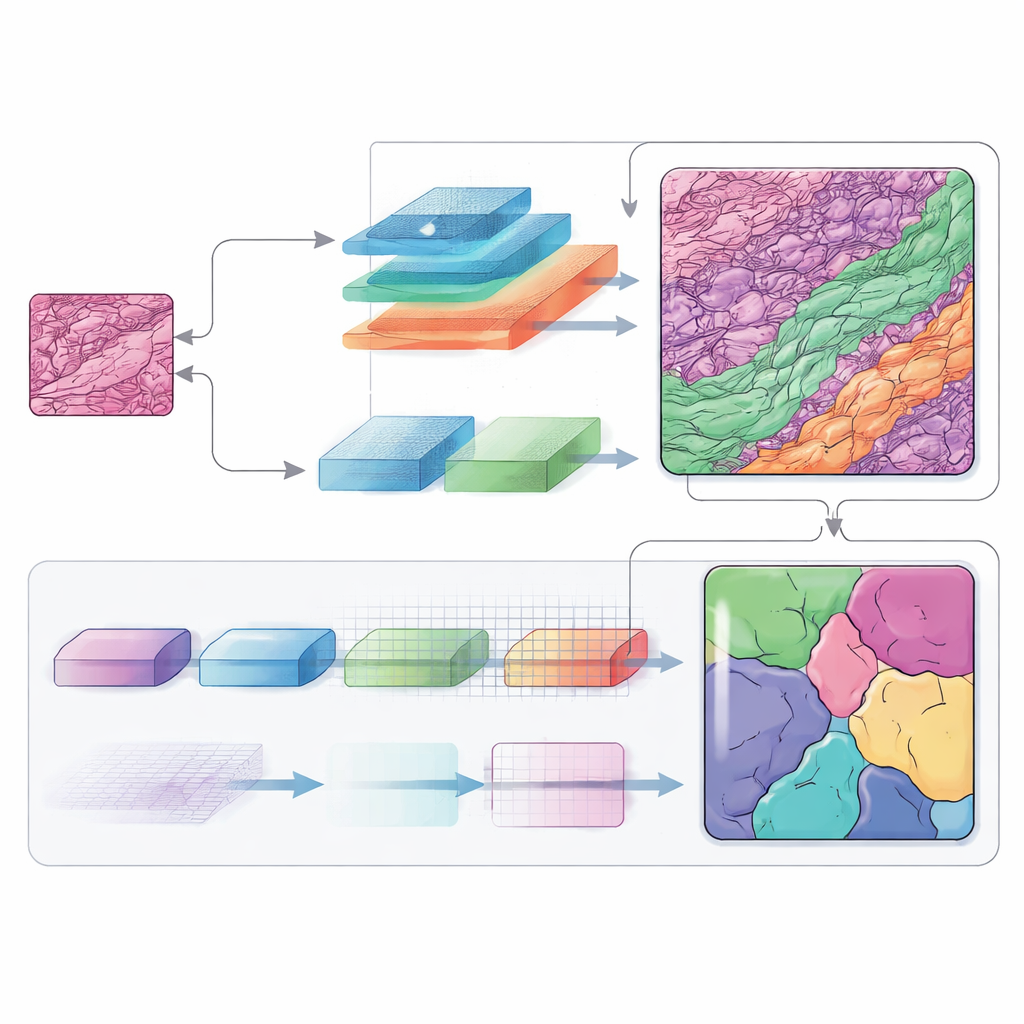
Frequentie-informatie speelt een centrale rol in deze architectuur. Door te schakelen tussen de gewone afbeeldingsruimte en een frequentie-gebaseerd zicht kan het netwerk brede vormen en kleine structuren anders behandelen. Lage-frequentiecomponenten helpen het systeem het algemene patroon van de tumor en de omliggende huidlagen te begrijpen, terwijl hoge-frequentiecomponenten de randen verscherpen waar het ene weefseltype eindigt en het andere begint. Zorgvuldig ontworpen modules voegen deze visies weer samen tot een ruimtelijke kaart, en een aanvullende decodeerblok (SCConv genoemd) filtert redundante signalen weg terwijl echt informatieve patronen worden versterkt. Het resultaat is een schonere, vertrouwdere kaart van elk weefselgebied.
Hoe goed werkt het in de praktijk?
De onderzoekers testten MSF‑VMDNet op de dataset voor non-melanoma huidkanker en vergeleken het met een breed scala aan toonaangevende segmentatiemodellen, waaronder klassiek U‑Net, op Transformers gebaseerde methoden en andere Vision Mamba-hybriden. Hun systeem produceerde duidelijkere tumorranden en minder fouten in lastige gebieden waar tumor, haarzakjes en ontstoken weefsel door elkaar lopen. Op gangbare overlapmaten overtrof het alle concurrenten en bereikte het ongeveer 95 procent overeenstemming met door experts getekende maskers. Om te onderzoeken of de methode generaliseert buiten één laboratorium en één kankertype, evalueerde het team het ook op drie aanvullende collecties: dermoscopische foto’s van huidlaesies, microscoopbeelden van verschillende typen celkernen en CT-scans van abdominale organen. In alle gevallen bleef de methode zeer nauwkeurig en presteerde statistisch beter dan sterke referentiemodellen.
Wat dit betekent voor patiënten en artsen
Concreet is MSF‑VMDNet een geautomatiseerde kaartmaker voor medische beelden die tumoren met uitzonderlijke precisie kan scheiden van het drukke landschap van normaal weefsel. Hoewel het niet het oordeel van pathologen vervangt, kan het een snel, gedetailleerd startpunt bieden, de handmatige inspanning verminderen en helpen voorkomen dat subtiele tumorgebieden over het hoofd worden gezien. Omdat dezelfde benadering goed werkt op zeer verschillende soorten medische beelden, zou het een veelzijdig hulpmiddel voor veel diagnostische taken kunnen worden. Met verdere ontwikkeling en integratie van klinische informatie kunnen systemen als deze bijdragen aan betrouwbaardere gradaties van huidkanker en uiteindelijk beter onderbouwde behandelingskeuzes ondersteunen.
Bronvermelding: Zhang, J., Pu, Q., Tian, J. et al. MSF-VMDNet for multi class segmentation of skin cancer whole slide images using a multi frequency dual encoder network. Sci Rep 16, 11722 (2026). https://doi.org/10.1038/s41598-026-40044-1
Trefwoorden: beeldvorming van huidkanker, segmentatie van medische beelden, deep learning in pathologie, histopathologische analyse, AI-diagnostiek