Clear Sky Science · ja
機械学習とディープラーニングが明かす、二重性ヒストン修飾を符号化する配列決定因子
DNAの句読点が細胞の将来をどう形作るか
体内のほぼすべての細胞は同じDNAを持ちながら、脳細胞と筋肉細胞がまったく異なる振る舞いを示します。その一因は、DNAを包むタンパク質に付く化学的タグが遺伝コードを変えずに遺伝子をオン・オフに切り替えられることです。本研究は一見単純だが示唆に富む問いを投げかけます:重要な遺伝子を沈黙と活性の間で待機させる特殊な“混合”タグを、細胞がどこに置くかをDNA配列に隠れたパターンが示しているのだろうか?
相反する二つのタグの物語
核内でDNAはヒストンと呼ばれるタンパク質の周りに巻き付いています。これらのヒストンは遺伝子の活性を促す信号(「進め」)や抑える信号(「止め」)を担うことがあります。時に、両方のタイプの信号が同じ領域に共存し、研究者が「二重性(バイバレント)」と呼ぶ状態を作り出します—遺伝子は準備されつつも待機している状態です。ほぼすべての組織に分化可能なマウス胚性幹細胞を用いて、研究者らはゲノム全域で三つの主要なヒストン修飾をマップしました。混合タグを持つ領域は単一タグの領域と異なり:やや狭く、GおよびCの塩基が多く、進化的により強く保存されていることが分かり、これらの待機状態にあるDNA領域が特に重要かつ慎重に保持されていることを示唆しました。
発生と疾患のための待機スイッチ
これらのタグ付けされた領域を近傍の遺伝子に結びつけると、明確なパターンが浮かび上がりました。混合ヒストン信号でマークされた遺伝子は控えめにしか発現しておらず、初期発生や幹細胞が柔軟性を保つか分化するかの決定に深く関与していました。Hippo、MAPK、Wnt、TGF-βといった成長や組織形成の中核となる経路が強く表れていました。いくつかの二重にマークされた遺伝子はがんと関連づけられており、正常な発生を導く同じ待機制御システムが疾患で乗っ取られることがあることを示唆します。総じて、混合マークは微調整されたディマー(調光)スイッチのように機能し、信号が来たときに増強や遮断ができる準備を保ちながら遺伝子に穏やかな基底活性を与えているようです。
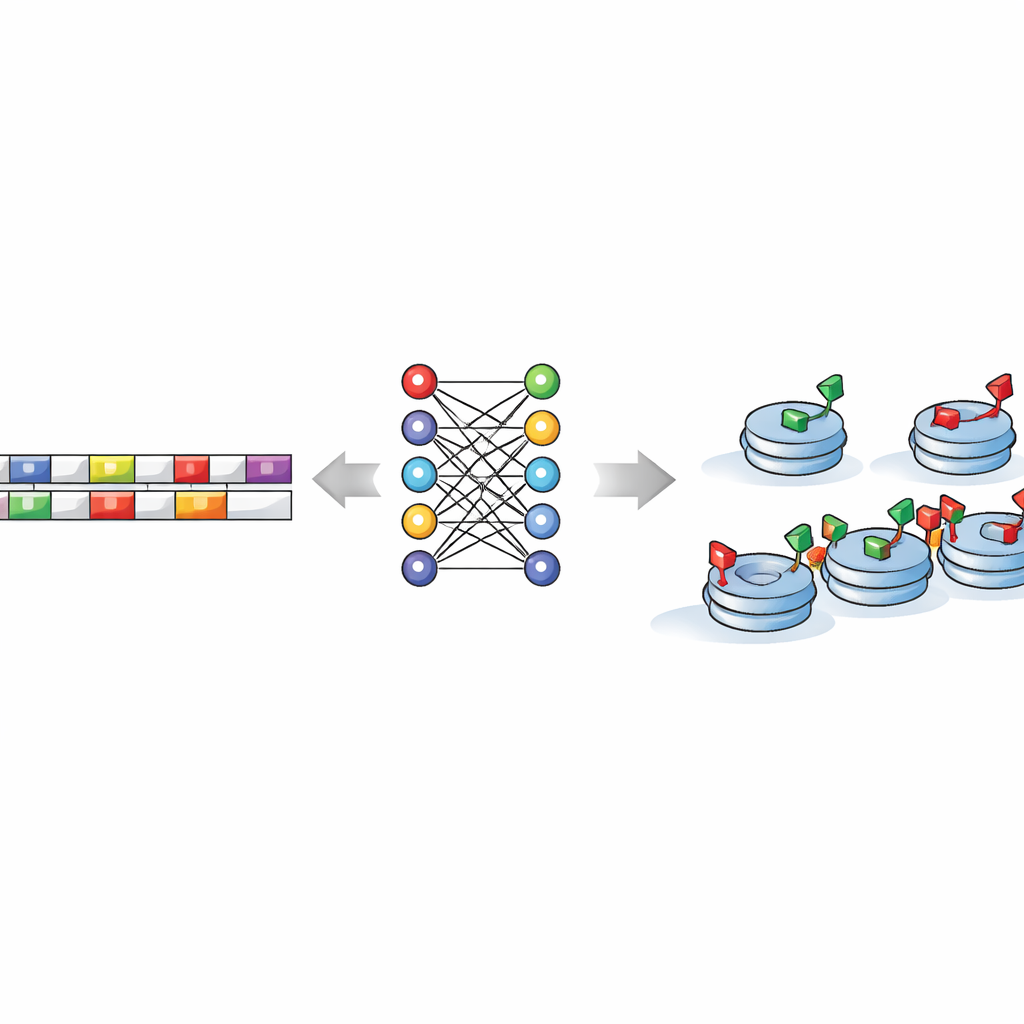
隠れたDNAパターンを読む機械を教える
本研究の核心は、これらの待機状態が形成される場所についてDNA配列自体が指示を符号化しているかどうかです。これを確かめるために、研究者らは短いDNA配列を—数塩基の全ての可能な小さな「単語」に分解して—機械学習およびディープラーニングモデル群に入力しました。これらのアルゴリズムは、混合タグ領域と活性化のみ、あるいは抑制のみの領域を高い精度で区別することを学びました。決定的なのは、DNA塩基をランダムにシャッフルするとモデルは失敗し、実際のゲノムには偶然のノイズではなく本物の予測信号が含まれていることを示した点です。つまり実験的測定を一切見なくても、コンピュータは配列だけを用いて細胞が混合ヒストンマークを配置しやすい場所を推測できるのです。
配列モチーフは分子の標識である
モデルの内部を解析することで、著者らは特に情報量の多い短いDNAモチーフのいくつかを明らかにしました。TCTGAAやTCACAGに似た配列は、OCT4、SOX2、ESRRB、TCFCP2l1といった幹細胞の主要な調節因子の既知の結合部位と一致しました。他のモチーフは二重にマークされた領域の端近くに集中する傾向があり、特定のモチーフがこれらの待機クロマチン領域の境界を定めるのに寄与している可能性を示唆します。モチーフの組み合わせや配置の違いが、同じ規制タンパク質の多くを共有しながらも異なるタイプの混合マークを区別しており、各クラスの二重性が独自の配列“文法”に従っていることを示唆しています。
幹細胞とその先にある意味
要するに、この研究はDNAが単なる遺伝子のリストではなく、遺伝子がどれだけ厳密にパッケージされ、どれだけ応答準備ができているかについて埋め込まれた指示も持っていることを示します。胚性幹細胞では、特定の短いDNAパターンがタンパク質因子を呼び寄せ、相反するヒストン修飾が共存する領域を形作ることで、発生遺伝子をオンとオフの宙ぶらりんの状態に保っています。機械学習とディープラーニングを用いてこの隠れたコードを読むことで、著者らは配列からエピジェネティック状態を予測する実用的なツールと、初期発生期に細胞がゲノムに柔軟性をプログラムする仕組み、さらにはそのプログラムが疾患でどのように狂うかについてのより明確な像を提供しています。
引用: Zhao, X., Wu, J., Che, Y. et al. Machine and Deep Learning Reveal Sequence Determinants Encoding Bivalent Histone Modifications. Commun Biol 9, 491 (2026). https://doi.org/10.1038/s42003-026-09962-8
キーワード: 二重性クロマチン, ヒストン修飾, 胚性幹細胞, DNA配列モチーフ, ゲノミクスにおける機械学習