Clear Sky Science · it
Apprendimento automatico e profondo rivelano i determinanti di sequenza che codificano modificazioni istoniche bivalenti
Come la punteggiatura del DNA plasma il futuro di una cellula
Ogni cellula del tuo corpo porta sostanzialmente lo stesso DNA, eppure le cellule cerebrali e quelle muscolari si comportano in modo molto diverso. Una delle ragioni è che sui proteine che avvolgono il DNA possono comparire segnali chimici che accendono o spengono i geni senza modificare il codice genetico. Questo studio pone una domanda sorprendentemente semplice ma dalle grandi implicazioni: esistono pattern nascosti nella sequenza del DNA che indicano alla cellula dove collocare un tipo speciale di marcatura “mista” che mantiene geni cruciali in uno stato di prontezza, a metà strada tra silenzio e attività?
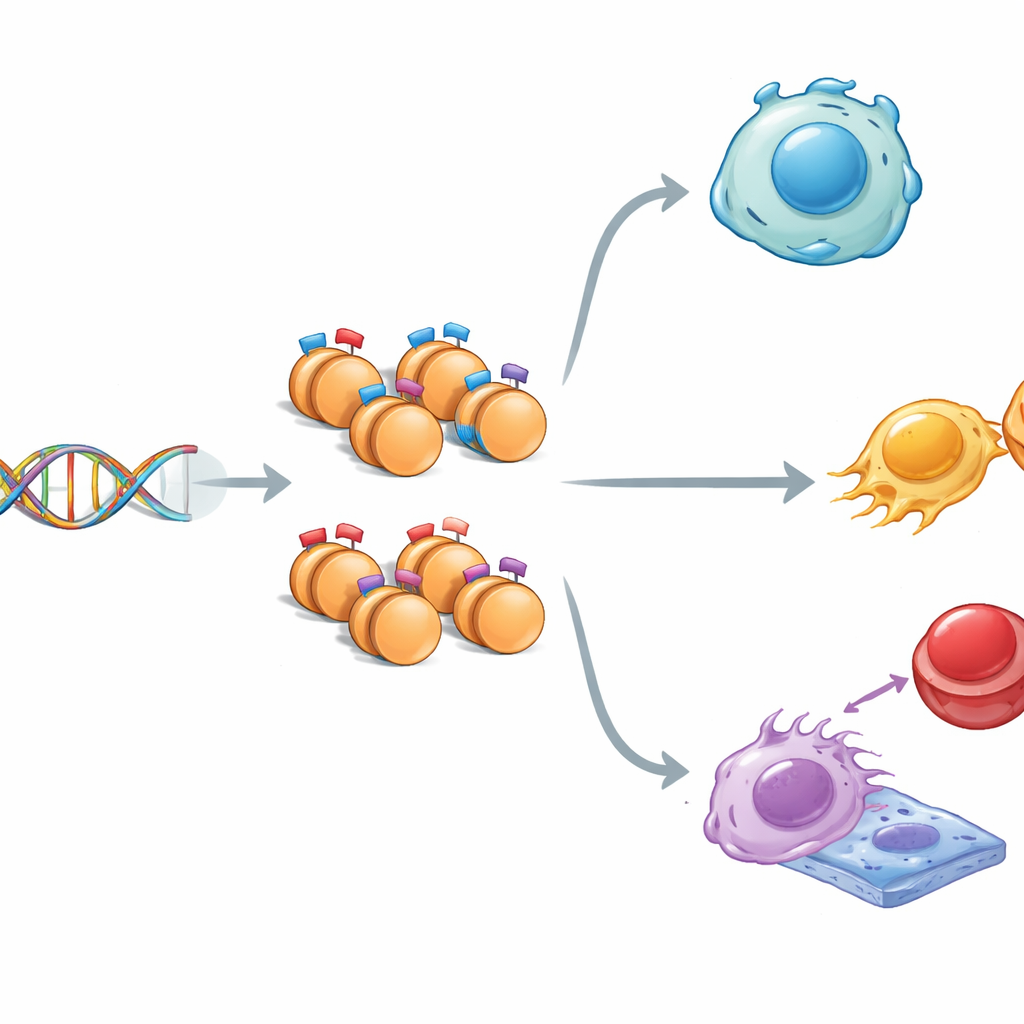
La storia di due marcature opposte
Nel nucleo il DNA è avvolto attorno a spool proteici chiamati istoni. Questi istoni possono portare segnali che o incoraggiano l’attività genica (“vai”) o la reprimono (“stop”). A volte, entrambi i tipi di segnali coesistono nello stesso punto, creando ciò che gli scienziati chiamano uno stato “bivalente”: i geni vengono mantenuti in modalità pronti-ma-in-attesa. Utilizzando cellule staminali embrionali di topo, che possono diventare quasi qualsiasi tessuto, i ricercatori hanno mappato tre marcature istoniche chiave lungo il genoma. Hanno scoperto che le regioni con marcature miste differivano da quelle con una sola marcatura: erano leggermente più strette, più ricche delle basi G e C e più fortemente conservate nell’evoluzione, suggerendo che questi tratti di DNA in stato di prontezza siano particolarmente importanti e attentamente protetti.
Interruttori pronti per sviluppo e malattia
Quando il gruppo ha collegato queste regioni marcate ai geni vicini è emerso un quadro coerente. I geni contrassegnati da segnali istonici misti tendevano a essere espressi solo moderatamente e partecipavano intensamente allo sviluppo precoce e alla decisione delle cellule staminali di rimanere flessibili o specializzarsi. Vie come Hippo, MAPK, Wnt e TGF-beta—circuiti centrali per la crescita e la formazione dei tessuti—erano fortemente rappresentate. Alcuni geni con marcature bivalenti sono inoltre stati associati a tumori, suggerendo che lo stesso sistema di controllo in stato di prontezza che guida lo sviluppo sano può essere sfruttato nella malattia. Nel complesso, le marcature miste sembrano agire come dimmer finemente regolati, fornendo ai geni un livello sottile di attività di base mentre li mantengono pronti a intensificare o spegnersi quando arrivano segnali.
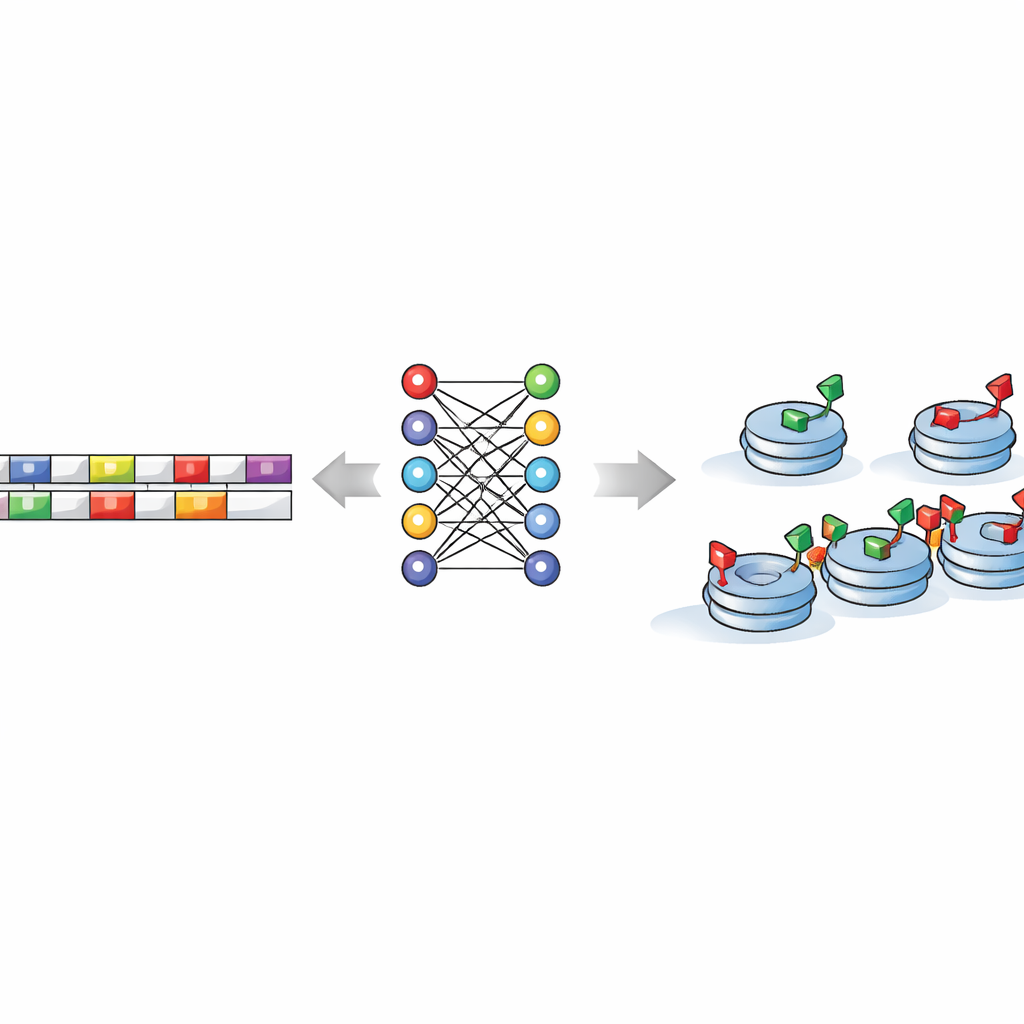
Insegnare alle macchine a leggere i pattern nascosti del DNA
Il fulcro dello studio è chiedersi se la sequenza del DNA stessa codifichi istruzioni su dove si debbano formare questi stati pronti. Per testarlo, i ricercatori hanno alimentato brevi tratti di DNA—scomposti in tutte le possibili piccole “parole” di poche lettere—in una serie di modelli di machine learning e deep learning. Questi algoritmi hanno imparato a distinguere regioni con marcature miste da quelle con solo marcature attivanti o repressorie, spesso con elevata accuratezza. Crucialmente, quando le lettere del DNA venivano mescolate casualmente, i modelli fallivano, mostrando che il genoma reale porta segnali predittivi autentici e non rumore casuale. Ciò significa che, senza guardare a misurazioni sperimentali, un computer può usare solo il testo del DNA per indovinare dove la cellula è probabile che apponga queste marcature istoniche miste.
I motivi di sequenza come segnali stradali molecolari
Ispezionando l’interno dei modelli, gli autori hanno individuato una manciata di brevi motivi del DNA—schemi di lettere ricorrenti—particolarmente informativi. Alcuni, come sequenze somiglianti a TCTGAA e TCACAG, corrispondevano a siti di legame noti di regolatori chiave delle cellule staminali come OCT4, SOX2, ESRRB e un fattore chiamato TCFCP2l1. Altri tendevano a raggrupparsi vicino ai bordi delle regioni bivalenti, suggerendo che certi motivi possano contribuire a definire i confini di queste zone di cromatina in stato di prontezza. Diverse combinazioni e posizionamenti di motivi distinguevano un tipo di marcatura mista da un’altra, implicando che ogni classe di bivalenza segua una propria “grammatica” di regole di sequenza pur condividendo molti degli stessi fattori regolatori.
Cosa significa per le cellule staminali e oltre
In termini semplici, lo studio dimostra che il DNA non è solo un elenco di geni; porta anche istruzioni incorporate su quanto strettamente quei geni debbano essere impacchettati e quanto siano pronti a rispondere. Nelle cellule staminali embrionali, specifici brevi motivi di DNA aiutano a reclutare fattori proteici e a plasmare regioni dove marcature istoniche opposte coesistono, mantenendo i geni dello sviluppo su un sottile equilibrio tra acceso e spento. Sfruttando machine learning e deep learning per leggere questo codice nascosto, gli autori forniscono sia uno strumento pratico per prevedere stati epigenetici a partire dalla sequenza sia un quadro più chiaro di come le cellule programmino la flessibilità nei loro genomi durante la vita precoce—e di come tale programmazione possa deragliare nelle malattie.
Citazione: Zhao, X., Wu, J., Che, Y. et al. Machine and Deep Learning Reveal Sequence Determinants Encoding Bivalent Histone Modifications. Commun Biol 9, 491 (2026). https://doi.org/10.1038/s42003-026-09962-8
Parole chiave: cromatina bivalente, modificazioni degli istoni, cellule staminali embrionali, motivi della sequenza del DNA, machine learning in genomica