Clear Sky Science · es
El aprendizaje automático y profundo revelan determinantes de la secuencia que codifican modificaciones histonas bivalentes
Cómo las marcas de puntuación del ADN moldean el futuro de una célula
Cada célula de tu cuerpo porta esencialmente el mismo ADN, sin embargo las neuronas y las células musculares actúan de forma muy distinta. Una razón es que etiquetas químicas en las proteínas que empaquetan el ADN pueden encender o apagar genes sin cambiar el código genético en sí. Este estudio plantea una pregunta sorprendentemente simple pero con grandes implicaciones: ¿existen patrones ocultos en la secuencia de ADN que indiquen a la célula dónde colocar un tipo especial de etiqueta “mixta” que mantiene genes cruciales en una posición intermedia entre silencio y actividad?
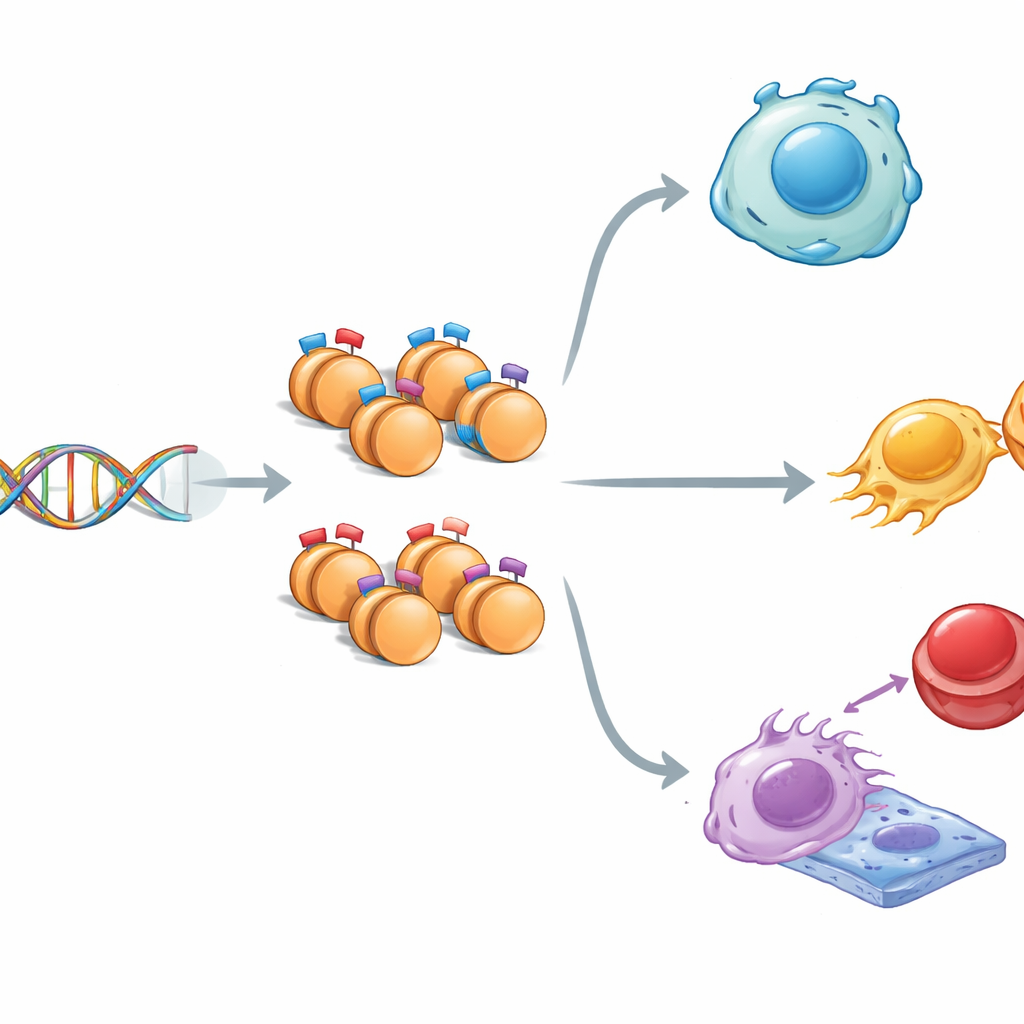
Una historia de dos marcas opuestas
Dentro del núcleo, el ADN se enrolla alrededor de carretes proteicos llamados histonas. Estas histonas pueden portar señales que o bien fomentan la actividad genética (“avanzar”) o bien la reprimen (“detener”). A veces, ambos tipos de señales coexisten en el mismo lugar, creando lo que los científicos denominan un estado “bivalente”: los genes quedan en una modalidad lista-pero-en-espera. Usando células madre embrionarias de ratón, que pueden convertirse en casi cualquier tejido, los investigadores cartografiaron tres marcas histonas clave a lo largo del genoma. Encontraron que las regiones con marcas mixtas diferían de las regiones con una sola marca: eran algo más estrechas, más ricas en las letras G y C del ADN, y más fuertemente conservadas a lo largo de la evolución, lo que sugiere que estos tramos en estado de espera son especialmente importantes y están cuidadosamente protegidos.
Interruptores preparados para el desarrollo y la enfermedad
Cuando el equipo relacionó estas regiones marcadas con genes cercanos, surgió un patrón. Los genes marcados por señales histonas mixtas tendían a activarse solo de forma moderada y estaban muy implicados en el desarrollo temprano y en la decisión de las células madre de permanecer flexibles o especializarse. Se representaron con fuerza vías como Hippo, MAPK, Wnt y TGF-beta —circuitos de comunicación centrales para el crecimiento y la formación de tejidos—. Algunos genes con marcas bivalentes también se han vinculado con cánceres, lo que sugiere que el mismo sistema de control en espera que guía el desarrollo saludable puede ser secuestrado en la enfermedad. En conjunto, las marcas mixtas parecen funcionar como reguladores finamente ajustados, dando a los genes una actividad basal sutil mientras los mantienen listos para aumentar o apagarse cuando lleguen señales.
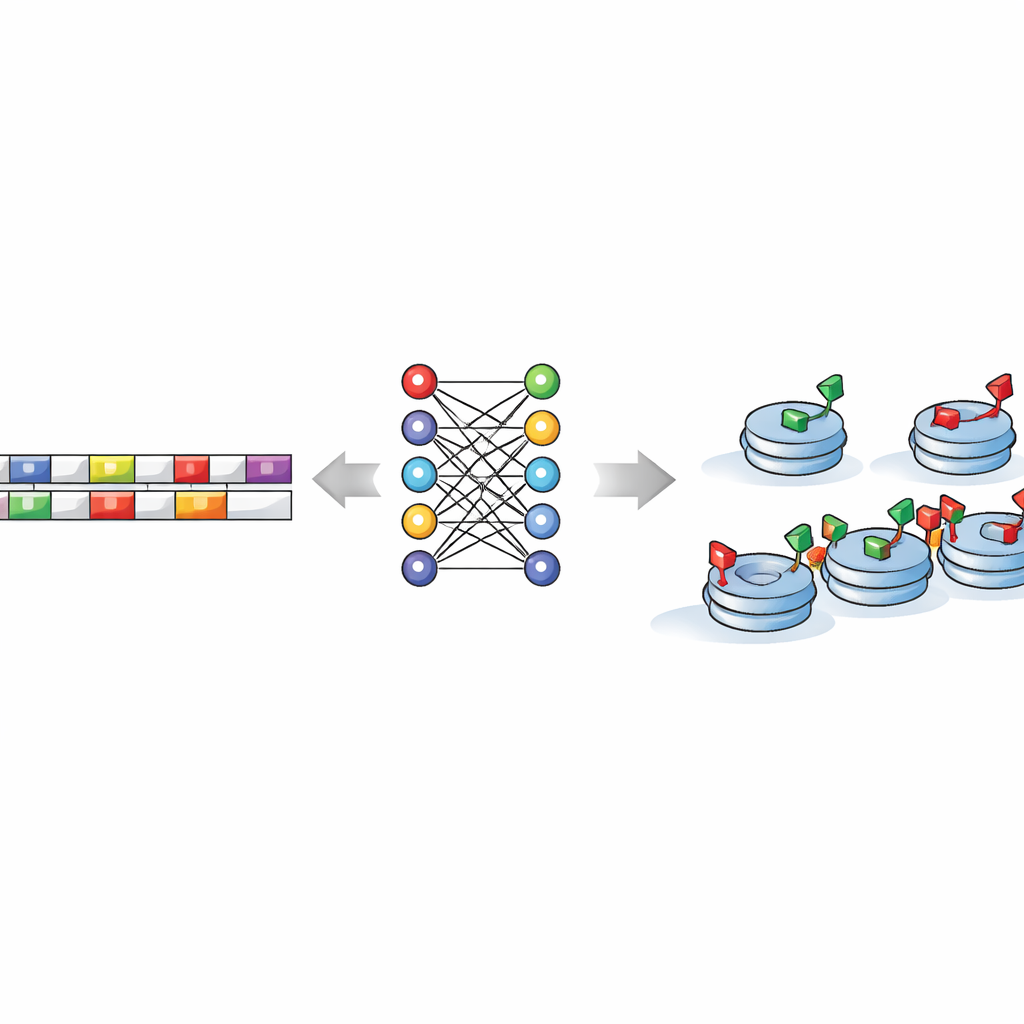
Enseñar a las máquinas a leer patrones ocultos del ADN
El núcleo del estudio pregunta si la propia secuencia de ADN codifica instrucciones sobre dónde deberían formarse estos estados en espera. Para probarlo, los investigadores alimentaron tramos cortos de ADN —descompuestos en todas las posibles “palabras” diminutas de pocas letras— a un conjunto de modelos de aprendizaje automático y aprendizaje profundo. Estos algoritmos aprendieron a distinguir regiones con marcas mixtas de aquellas con marcas solo activadoras o solo represoras, a menudo con alta precisión. De forma crucial, cuando se barajaron las letras del ADN al azar, los modelos fracasaron, mostrando que el genoma real contiene señales predictivas auténticas y no ruido accidental. Esto significa que, sin recurrir a mediciones experimentales, un ordenador puede usar solo el texto del ADN para adivinar dónde es probable que la célula coloque estas marcas histonas mixtas.
Motivos de secuencia como señales de tránsito molecular
Al examinar el interior de los modelos, los autores descubrieron un puñado de motivos de ADN cortos —patrones de letras recurrentes— que resultaron especialmente informativos. Algunos, como secuencias que recuerdan a TCTGAA y TCACAG, coincidían con sitios de unión conocidos de reguladores maestros de células madre como OCT4, SOX2, ESRRB y un factor llamado TCFCP2l1. Otros tendían a agruparse cerca de los bordes de las regiones marcadas de forma bivalente, lo que sugiere que ciertos motivos pueden ayudar a fijar los límites de estas zonas de cromatina en espera. Diferentes combinaciones y ubicaciones de motivos distinguían un tipo de marcado mixto de otro, lo que implica que cada clase de bivalencia sigue su propia “gramática” de reglas de secuencia, aun compartiendo muchas de las mismas proteínas reguladoras.
Qué significa esto para las células madre y más allá
En pocas palabras, el estudio demuestra que el ADN no es solo una lista de genes; también contiene instrucciones integradas sobre cuán apretadamente deben empaquetarse esos genes y qué tan preparados están para responder. En las células madre embrionarias, patrones cortos de ADN específicos ayudan a reclutar factores proteicos y a moldear regiones donde coexisten marcas histonas opuestas, manteniendo los genes del desarrollo en un equilibrio precario entre encendido y apagado. Al aprovechar el aprendizaje automático y profundo para leer este código oculto, los autores aportan tanto una herramienta práctica para predecir estados epigenéticos a partir de la secuencia como una imagen más clara de cómo las células programan la flexibilidad en sus genomas durante la etapa temprana de la vida —y cómo esa programación puede fallar en la enfermedad.
Cita: Zhao, X., Wu, J., Che, Y. et al. Machine and Deep Learning Reveal Sequence Determinants Encoding Bivalent Histone Modifications. Commun Biol 9, 491 (2026). https://doi.org/10.1038/s42003-026-09962-8
Palabras clave: cromatina bivalente, modificaciones de histonas, células madre embrionarias, motivos de secuencia de ADN, aprendizaje automático en genómica