Clear Sky Science · fr
Smoothie : inférence et intégration efficaces de réseaux de co‑expression spatiale à partir de données de transcriptomique spatiale débruitées
Voir les voisinages cellulaires avec un nouveau niveau de détail
Chaque tissu du corps est une ville animée de cellules, chacune activant ou désactivant des gènes à des emplacements précis. Les nouvelles technologies de « transcriptomique spatiale » peuvent désormais lire quels gènes sont actifs à presque chaque point d’une coupe de tissu, mais les données brutes sont extrêmement bruitées et incomplètes. Cet article présente Smoothie, une méthode computationnelle qui nettoie ces mesures floues et révèle des groupes de gènes qui agissent ensemble dans l’espace, aidant les scientifiques à déchiffrer comment les tissus se construisent, comment ils fonctionnent et comment ils évoluent au cours du temps ou en cas de maladie.
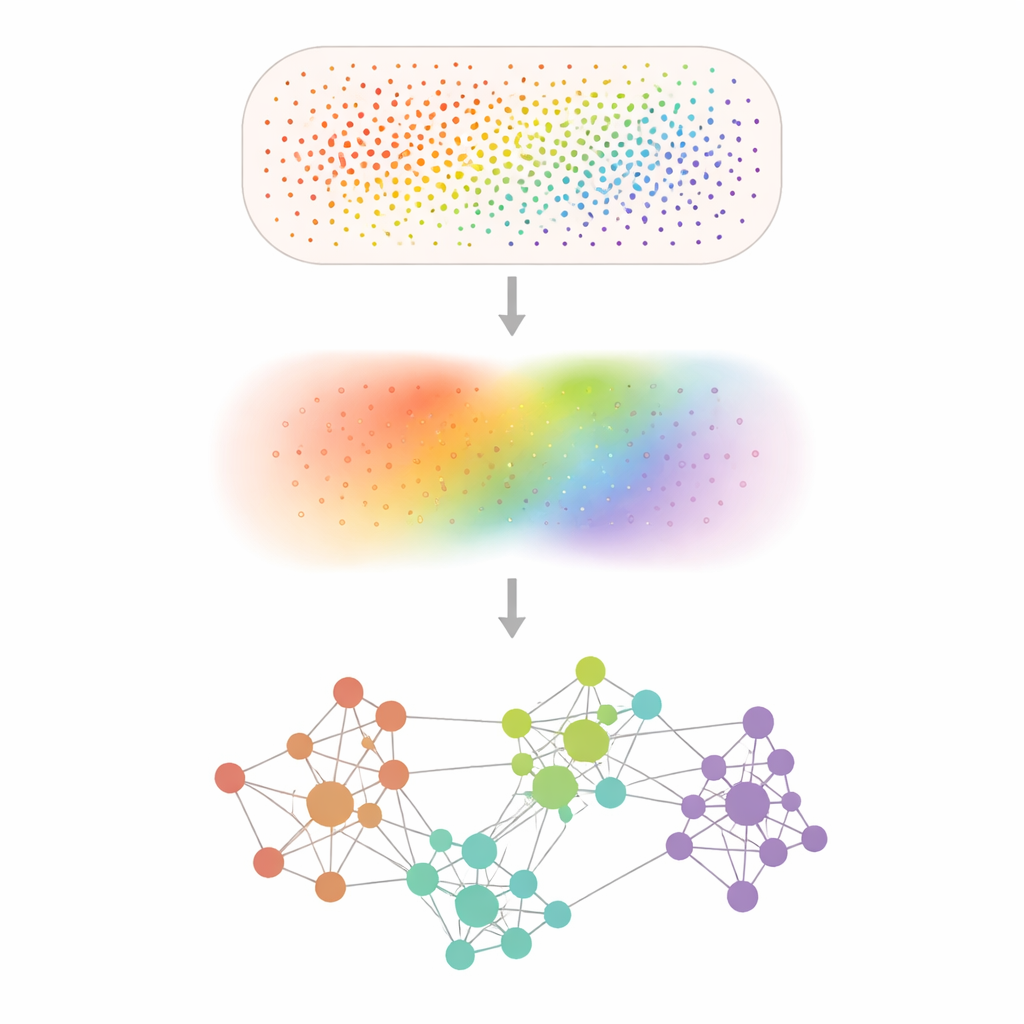
Transformer des points bruités en motifs clairs
Les expériences de transcriptomique spatiale enregistrent l’activité génique à des dizaines de milliers jusqu’à des centaines de millions de positions minuscules, mais de nombreux gènes sont à peine détectés et les mesures sont ponctuées de bruit aléatoire. Smoothie traite cela en lissant légèrement les données avec une étape mathématique de « lissage » qui moyenne chaque mesure avec ses voisines, un peu comme appliquer un filtre doux à une photo pixellisée. Après ce débruitage, Smoothie compare chaque paire de gènes pour voir où leurs profils lissés montent et descendent ensemble à travers le tissu. Les paires fortement synchronisées sont reliées dans un réseau, et les groupes au sein de ce réseau révèlent des ensembles de gènes partageant un motif spatial commun et vraisemblablement un rôle biologique commun.
Lire la carte génique du cerveau et de l’embryon
Les auteurs ont d’abord testé Smoothie sur une carte à haute résolution de l’activité génique dans le cervelet adulte de la souris, une région du cerveau impliquée dans l’équilibre et la coordination. Smoothie a mis au jour des groupes de gènes distincts correspondant proprement à des types cellulaires connus, notamment les neurones de Purkinje, les cellules granulaires, les oligodendrocytes et les cellules de soutien. En comparant les résultats avec trois méthodes de pointe, l’équipe a montré que Smoothie identifie davantage de groupes de gènes, inclut plus de gènes au total et forme des clusters plus compacts et mieux séparés, tout en fonctionnant beaucoup plus rapidement. De manière cruciale, l’étape de lissage a rendu les relations biologiques réelles plus faciles à détecter en renforçant les corrélations entre gènes marqueurs connus partageant un type cellulaire.
Découvrir des types cellulaires cachés et des gènes inconnus
Ensuite, les chercheurs ont soumis Smoothie à un test exigeant : un jeu de données spatial massif provenant d’un embryon de souris en mi‑gestation mesuré à une résolution sub‑micronique. Sans recourir à un prétraitement important, Smoothie a analysé plus de 175 millions de points spatiaux et plus de 20 000 gènes en environ une heure. Il a révélé des centaines de modules géniques correspondant à des organes, à des sous‑régions d’organes et à des types cellulaires spécialisés dans le foie, le rein, le cerveau et la peau. Parce qu’un très grand nombre de gènes pouvaient être inclus, Smoothie a aussi attribué des fonctions probables à des dizaines de gènes peu caractérisés en les plaçant dans des modules contenant des marqueurs connus. Fait intrigant, certains modules étaient constitués de gènes voisins sur le génome, suggérant que l’organisation locale de l’ADN contribue à déterminer quels gènes sont actifs ensemble dans l’espace.
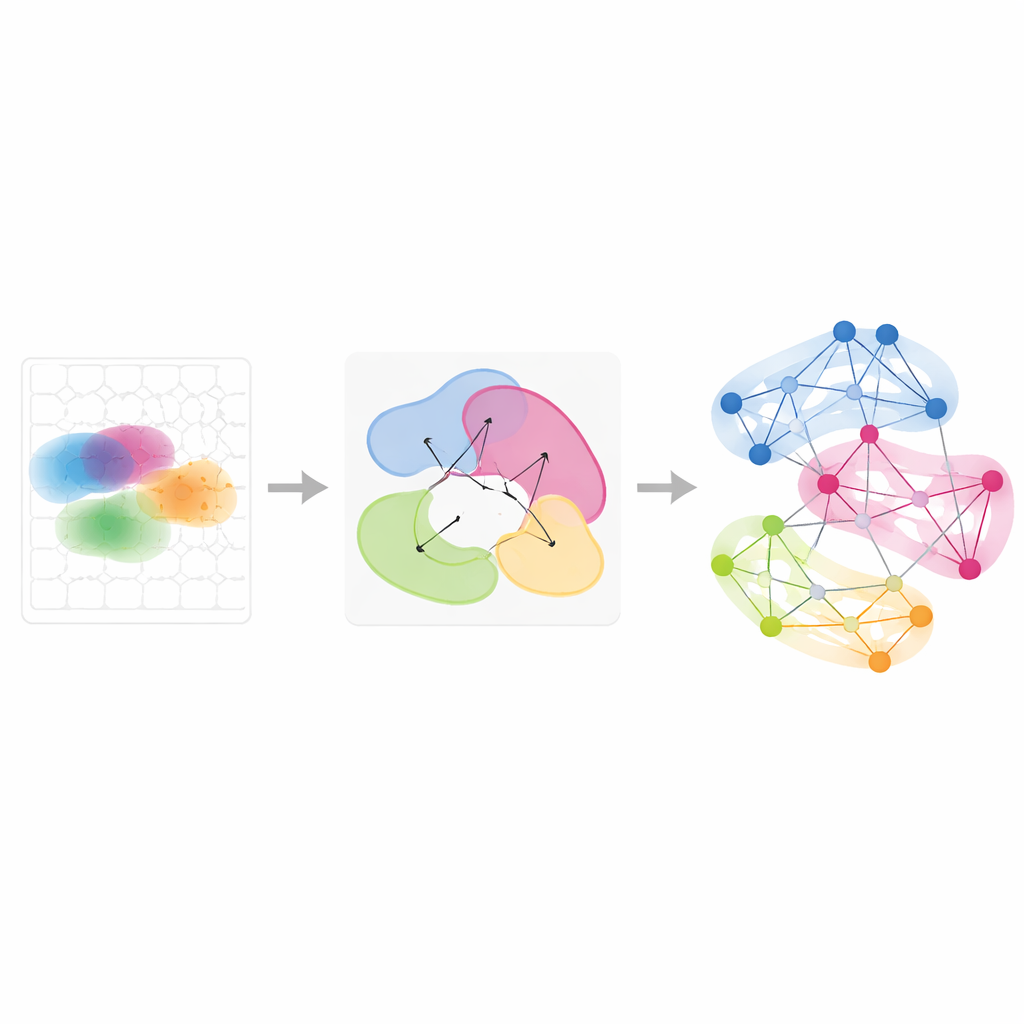
Suivre les programmes géniques à travers le temps et les conditions
Au-delà des tissus isolés, Smoothie peut intégrer plusieurs expériences spatiales pour observer comment les motifs géniques sont partagés ou évoluent. Les auteurs ont appliqué cela à une série d’embryons de souris à des stades développementaux légèrement différents et à des ovaires échantillonnés en huit points temporels pendant l’ovulation induite par des hormones. En comparant comment les partenaires d’un gène dans le réseau changent entre les échantillons, Smoothie classe les gènes en stables ou dynamiques. Cela a révélé, par exemple, des groupes de gènes qui passent du foie aux vaisseaux sanguins alors que les globules rouges migrent au cours du développement, et des programmes géniques en forme d’onde dans les cellules de soutien ovariennes qui s’activent en séquence pour déclencher l’ovulation. Ces analyses montrent que les réseaux géniques, plutôt que les images brutes, fournissent un langage commun puissant pour aligner des tissus et des points temporels qui ne correspondent pas exactement.
Une nouvelle lentille pour la biologie spatiale
Concrètement, Smoothie transforme d’immenses cartes géniques spatiales bruitées en réseaux clairs et interprétables qui mettent en évidence où et comment les gènes travaillent ensemble dans des tissus réels. Pour les non‑spécialistes, le message clé est que cette méthode facilite grandement la détection de motifs significatifs, la connexion de gènes inconnus à des types cellulaires connus et le suivi des changements tissulaires au fil du temps ou en réponse à un traitement. À mesure que les technologies de la génomique spatiale continueront à se préciser, des outils comme Smoothie aideront à transformer des millions de petites mesures moléculaires en récits cohérents sur le développement, la santé et la maladie.
Citation: Holdener, C., De Vlaminck, I. Smoothie: efficient inference and integration of spatial co-expression networks from denoised spatial transcriptomics data. Commun Biol 9, 459 (2026). https://doi.org/10.1038/s42003-026-09898-z
Mots-clés: transcriptomique spatiale, réseaux de co‑expression génique, architecture tissulaire, biologie du développement, génomique computationnelle