Clear Sky Science · de
Smoothie: effiziente Inferenz und Integration räumlicher Ko‑Expressionsnetzwerke aus entrauschten Spatial‑Transcriptomics‑Daten
Zellnachbarschaften in neuer Detailstufe sehen
Jedes Gewebe im Körper ist eine geschäftige Stadt von Zellen, die Gene an genau definierten Orten ein‑ und ausschalten. Neue "spatial transcriptomics"‑Technologien können inzwischen ablesen, welche Gene an nahezu jedem Punkt eines Gewebescheibchens aktiv sind, doch die Rohdaten sind extrem verrauscht und unvollständig. Diese Arbeit stellt Smoothie vor, eine rechnerische Methode, die diese unscharfen Messungen säubert und Gruppen von Genen aufdeckt, die räumlich zusammenwirken. Das hilft Forschenden zu entschlüsseln, wie Gewebe aufgebaut sind, wie sie funktionieren und wie sie sich im Verlauf der Zeit oder bei Krankheit verändern.
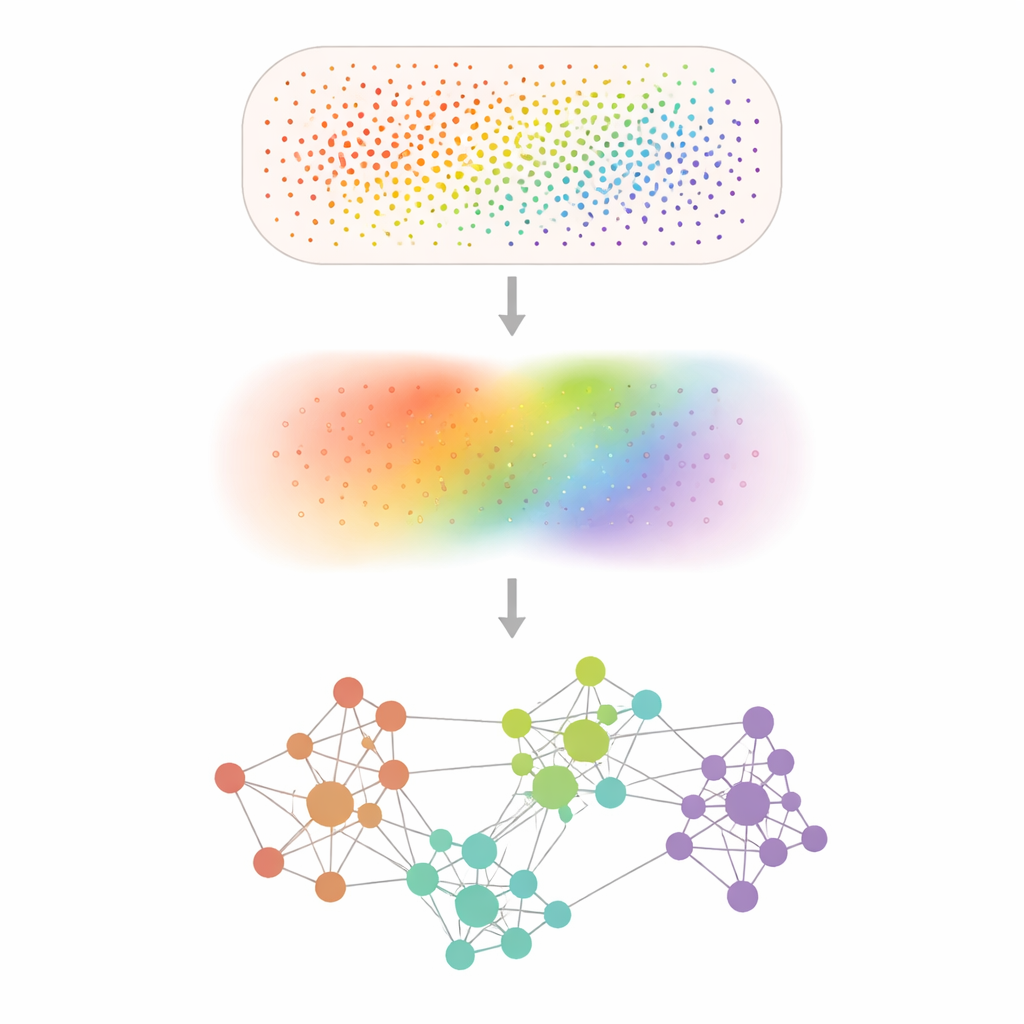
Aus verrauschten Punkten klare Muster machen
Spatial‑Transcriptomics‑Experimente zeichnen Genaktivität an Zehntausenden bis Hunderten Millionen winziger Positionen auf, doch viele Gene werden kaum erfasst und die Messungen sind von zufälligem Rauschen durchsetzt. Smoothie begegnet dem mit einem behutsamen Verwischen der Daten durch einen mathematischen "Smoothing"‑Schritt, der jede Messung mit ihren Nachbarn mittelt – ähnlich wie ein Weichzeichner auf ein pixeliges Foto angewendet wird. Nach diesem Entrauschen vergleicht Smoothie jedes Genpaar, um zu sehen, wo sich ihre geglätteten Muster im Gewebe gemeinsam erhöhen und senken. Paare, die stark synchron sind, werden in einem Netzwerk verbunden, und Cluster innerhalb dieses Netzwerks zeigen Gen‑gruppen, die ein gemeinsames räumliches Muster und vermutlich eine gemeinsame biologische Rolle teilen.
Die Genkarte von Gehirn und Embryo lesen
Die Autorinnen und Autoren testeten Smoothie zuerst an einer hochauflösenden Karte der Genaktivität im erwachsenen Mauskleinhirn, einem Hirnbereich, der an Gleichgewicht und Koordination beteiligt ist. Smoothie enthüllte deutlich abgegrenzte Gen‑Gruppen, die bekannten Zelltypen wie Purkinje‑Neuronen, Körnerzellen, Oligodendrozyten und Stützzellen entsprachen. Im Vergleich mit drei führenden Methoden zeigte das Team, dass Smoothie mehr Gen‑Gruppen findet, insgesamt mehr Gene einschließt und dichtere, besser getrennte Cluster bildet – und das bei deutlich schnellerer Laufzeit. Entscheidend machte der Glättungsschritt reale biologische Zusammenhänge leichter erkennbar, indem er die Korrelationen zwischen bekannten Marker‑Genen desselben Zelltyps verstärkte.
Versteckte Zelltypen und unbekannte Gene entdecken
Als Nächstes stellten die Forschenden Smoothie auf eine harte Probe: einen riesigen räumlichen Datensatz aus einem Maus‑Embryo Mitte der Trächtigkeitsperiode, gemessen in Sub‑Mikrometer‑Auflösung. Ohne aufwendige Vorverarbeitung analysierte Smoothie über 175 Millionen räumliche Punkte und mehr als 20.000 Gene in etwa einer Stunde. Es offenbarte Hunderte von Genmodulen, die Organen, Unterregionen innerhalb von Organen und spezialisierten Zelltypen in Leber, Niere, Gehirn und Haut entsprachen. Weil so viele Gene einbezogen werden konnten, ordnete Smoothie außerdem dutzenden schlecht charakterisierten Genen wahrscheinliche Funktionen zu, indem es sie in Module mit bekannten Markern platzierte. Interessanterweise bestanden manche Module aus Genen, die nebeneinander im Genom liegen, was darauf hindeutet, dass lokale DNA‑Organisation beeinflusst, welche Gene räumlich gemeinsam aktiv sind.
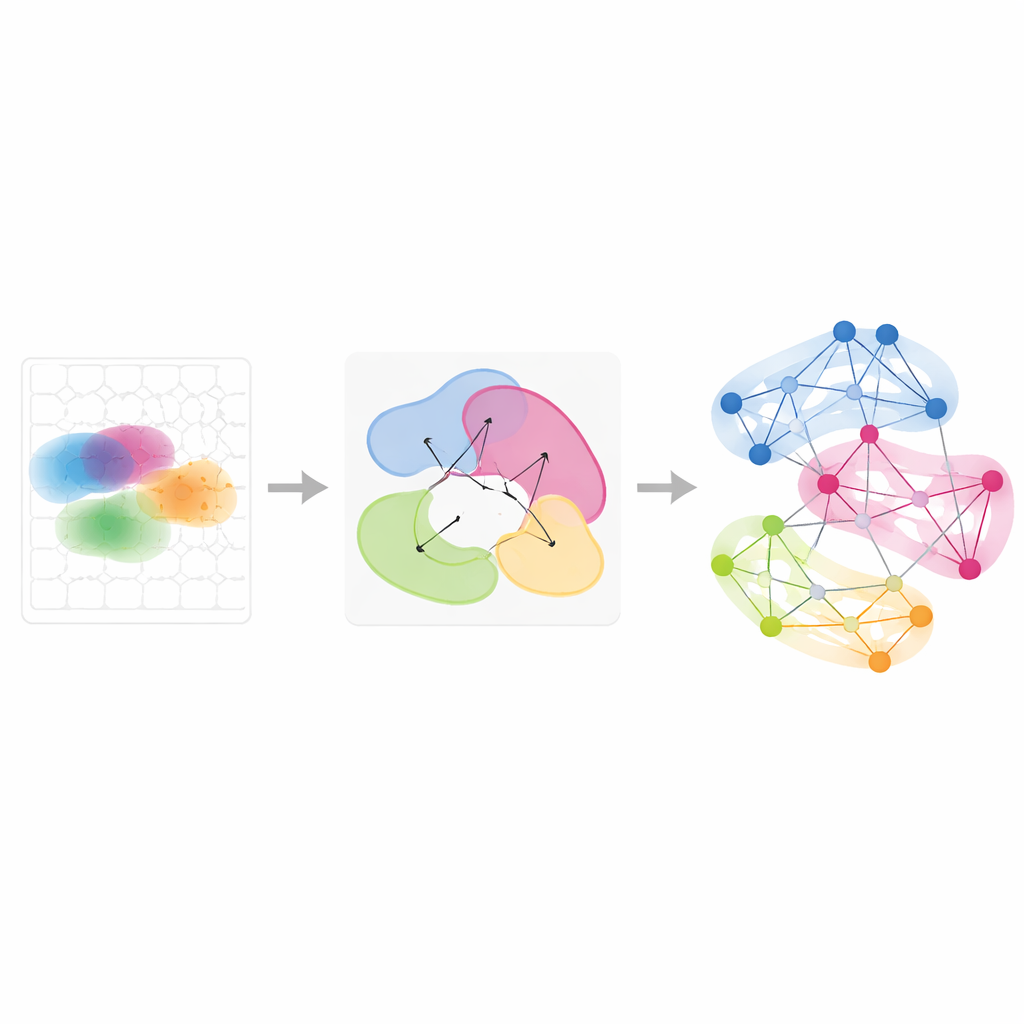
Genprogramme über Zeit und Bedingungen verfolgen
Über einzelne Gewebe hinaus kann Smoothie mehrere räumliche Experimente integrieren, um zu sehen, wie Genmuster geteilt werden oder sich verändern. Die Autorinnen und Autoren wandten dies auf eine Reihe von Maus‑Embryonen in leicht unterschiedlichen Entwicklungsstadien und auf Eierstöcke an, die zu acht Zeitpunkten während hormonell induzierter Ovulation entnommen wurden. Indem Smoothie vergleicht, wie sich die Partner eines Gens im Netzwerk zwischen Proben verschieben, bewertet es Gene als stabil oder dynamisch. So wurden etwa Gen‑Gruppen entdeckt, die sich während der Entwicklung vom Lebergewebe zu Blutgefäßen verlagern, während rote Blutkörperchen wandern, sowie wellenartige Genprogramme in ovikulären Stütz‑Zellen, die nacheinander anschalten und die Ovulation antreiben. Diese Analysen zeigen, dass Gen‑Netzwerke, anders als rohe Bilder, eine mächtige gemeinsame Sprache liefern, um nichtübereinstimmende Gewebe und Zeitpunkte auszurichten.
Eine neue Linse für die räumliche Biologie
Praktisch verwandelt Smoothie riesige, verrauschte räumliche Genkarten in klare, interpretierbare Netzwerke, die hervorheben, wo und wie Gene in realen Geweben zusammenarbeiten. Für Nicht‑Expertinnen und Nicht‑Experten lautet die Kernbotschaft: Diese Methode macht es deutlich leichter, sinnvolle Muster zu erkennen, unbekannte Gene mit bekannten Zelltypen zu verbinden und nachzuvollziehen, wie sich Gewebe über Zeit oder Behandlung verändern. Während sich die Technologien der räumlichen Genomik weiter schärfen, werden Werkzeuge wie Smoothie helfen, Millionen winziger molekularer Messungen in kohärente Geschichten über Entwicklung, Gesundheit und Krankheit zu verwandeln.
Zitation: Holdener, C., De Vlaminck, I. Smoothie: efficient inference and integration of spatial co-expression networks from denoised spatial transcriptomics data. Commun Biol 9, 459 (2026). https://doi.org/10.1038/s42003-026-09898-z
Schlüsselwörter: räumliche Transkriptomik, Gen‑Koexpressionsnetzwerke, Gewebearchitektur, Entwicklungsbiologie, computationale Genomik