Clear Sky Science · fr
Prédiction améliorée des associations médicament–maladie par intégration de données multimodales et fusion globale-locale guidée par des méta‑chemins
Pourquoi trouver de nouveaux usages pour des médicaments existants est important
Mettre au point un nouveau médicament de A à Z est long, risqué et extrêmement coûteux. Pourtant, dans les pharmacies d’aujourd’hui se cachent de nombreux médicaments qui pourraient aussi servir à traiter d’autres maladies, si l’on parvenait à découvrir ces usages supplémentaires. Cette étude présente MedPathEx, une approche informatique qui fouille de vastes ensembles de données biomédicales pour prédire quels médicaments existants sont susceptibles d’être efficaces pour quelles maladies, accélérant potentiellement la recherche de nouveaux traitements et optimisant l’utilisation des médicaments déjà disponibles.
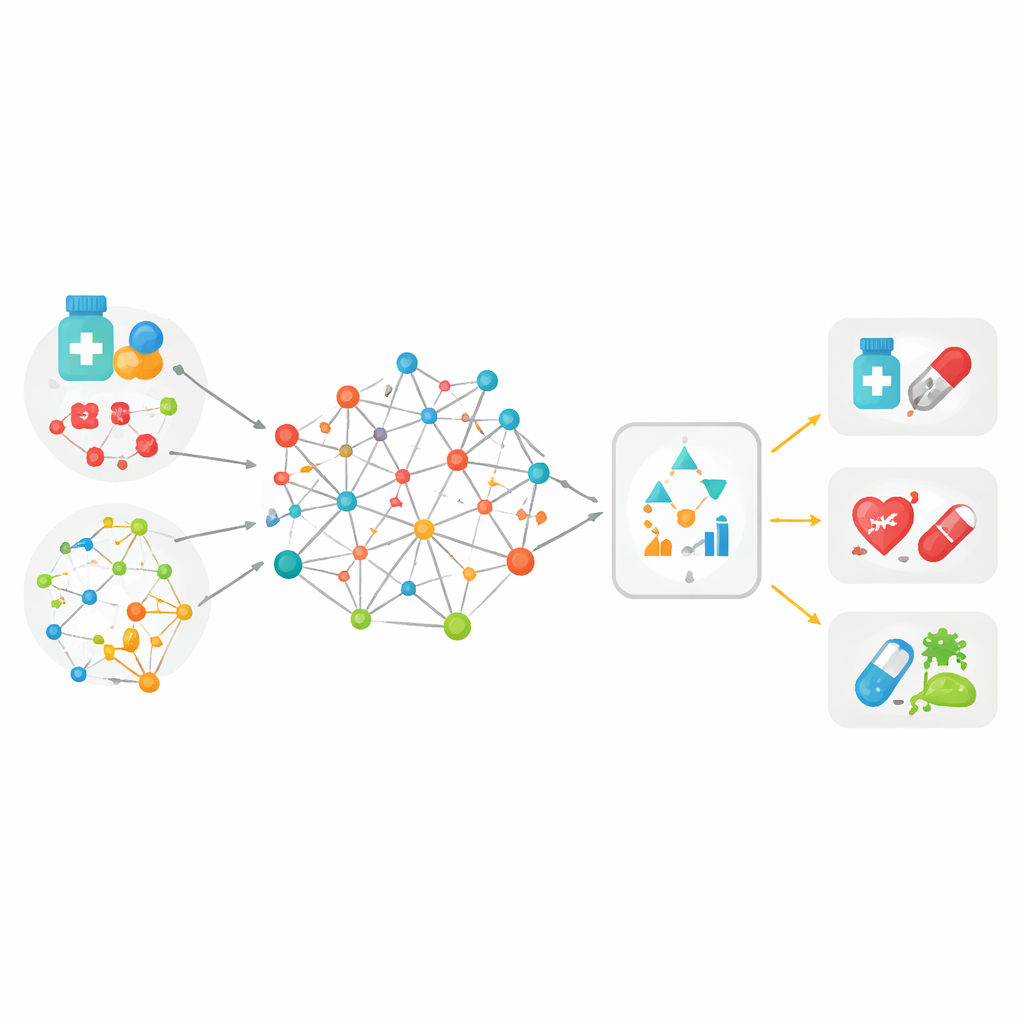
Rassembler de nombreux indices dans une grande carte
La plupart des outils antérieurs pour apparier médicaments et maladies se basaient sur un seul type d’information — par exemple, la similitude de structures moléculaires entre deux médicaments ou la proximité de deux maladies dans les dossiers médicaux. MedPathEx part du constat qu’aucun indice unique n’est suffisant. Les auteurs construisent une grande « carte » qui relie trois types d’acteurs : médicaments, maladies et gènes. Sur ces liens, ils superposent plusieurs types d’indices : la composition des molécules médicamenteuses, leur classification thérapeutique, les effets secondaires qu’elles provoquent, la manière dont les maladies se manifestent chez les patients et dans le langage médical, et les connaissances sur la fonction des gènes. En tissant toutes ces informations multimodales dans un réseau hétérogène, chaque médicament, maladie et gène est décrit de façon plus riche et plus réaliste qu’auparavant.
Voir à la fois le voisinage et toute la ville
Face à une carte aussi vaste, un défi consiste à décider quels motifs sont pertinents. MedPathEx relève ce défi en combinant deux vues complémentaires du réseau. D’abord, il se concentre sur les voisinages locaux, en retraçant des chemins courts et significatifs — par exemple, médicament → gène → maladie — pour capter comment des gènes spécifiques peuvent relier un médicament à une pathologie. Ces promenades structurées, appelées méta‑chemins, mettent en évidence des relations fines. Ensuite, la méthode adopte une vue d’ensemble globale, permettant à chaque nœud d’« accorder de l’attention » à de nombreux autres à travers toute la carte. Cette vue d’attention globale saisit des tendances plus larges et des connexions à longue portée qui seraient manquées en ne suivant que des chemins locaux.
Fusionner différentes vues en un seul signal
Pour transformer ces vues du réseau en prédictions, MedPathEx utilise des techniques modernes de réseaux neuronaux afin de convertir la carte complexe en empreintes numériques compactes pour chaque médicament, maladie et gène. Une partie du modèle apprend à partir de graphes de similarité construits au sein de chaque type (médicament–médicament, maladie–maladie, gène–gène). Une autre partie se concentre sur les voisinages locaux issus des méta‑chemins, tandis qu’une troisième capture la structure globale de l’ensemble du réseau. Le modèle apprend ensuite quel poids attribuer à chacune de ces sources et les fusionne en une représentation combinée pour chaque nœud. Lorsqu’il compare les empreintes combinées d’un médicament et d’une maladie donnés, il produit un score reflétant la probabilité que le couple soit réellement associé dans le monde réel.
Tester les performances et sonder ce qui compte
Les chercheurs ont testé MedPathEx en utilisant des bases de données publiques recensant des centaines de milliers de liens connus entre des milliers de médicaments, maladies et gènes. Dans une validation croisée rigoureuse en cinq plis, MedPathEx a surpassé diverses approches concurrentes, y compris des méthodes classiques d’apprentissage automatique et plusieurs modèles avancés basés sur les graphes. Des mesures de précision telles que l’AUC, la précision moyenne et le score F1 étaient toutes supérieures, montrant que la méthode sépare plus fiablement les paires médicament–maladie vraies des paires fausses. Lorsque des composants ont été retirés un à un, les performances ont chuté, en particulier lorsque la vue locale des méta‑chemins ou la vue d’attention globale était supprimée, soulignant que les deux perspectives sont essentielles. L’analyse a également montré que l’information issue des méta‑chemins locaux contribue le plus, tandis que les caractéristiques globales et de similarité apportent des raffinements importants.
Exemples concrets en cardiologie et hypertension artérielle
Au‑delà des chiffres, les auteurs ont vérifié si les suggestions les mieux classées par MedPathEx pour deux affections courantes — la maladie coronarienne et l’hypertension — correspondaient aux connaissances de la littérature médicale. Pour chaque maladie, le système a proposé plusieurs médicaments, dont certains sont déjà utilisés en clinique pour des problèmes cardiaques connexes, ce qui renforce la crédibilité de l’approche. D’autres sont des candidats moins évidents mais présentent néanmoins des liens biologiques, tels que des effets sur l’inflammation, la fonction vasculaire ou l’accumulation de plaque dans les artères. Des diagrammes de réseau montrant médicaments, gènes et maladies illustrent comment ces médicaments pourraient influencer des voies liées à la maladie, pointant vers des mécanismes plausibles à explorer en laboratoire ou en études cliniques.
Ce que cela signifie pour les médicaments de demain
En termes simples, MedPathEx montre qu’en combinant de nombreuses sources de données biomédicales et en observant à la fois les motifs locaux et globaux des connexions entre médicaments, gènes et maladies, les ordinateurs peuvent mieux estimer quels médicaments pourraient être utiles pour quelles maladies. Si cet outil ne remplace pas les essais cliniques ou les tests en conditions réelles, il peut réduire l’immense espace de recherche et mettre en évidence des candidats prometteurs — en particulier pour des maladies complexes comme les affections cardiaques et l’hypertension. À mesure que des données biologiques plus détaillées deviendront disponibles et que de tels modèles seront davantage validés, des approches comme MedPathEx pourraient devenir des partenaires puissants dans la réaffectation de médicaments existants et la conception de stratégies de traitement plus efficaces.
Citation: Wu, S., Wang, W., Jiao, H. et al. Enhanced drug disease association prediction through multimodal data integration and meta path guided global local feature fusion. Sci Rep 16, 11038 (2026). https://doi.org/10.1038/s41598-026-36223-9
Mots-clés: réaffectation de médicaments, associations médicament–maladie, réseaux hétérogènes, réseaux de neurones sur graphes, découverte de médicaments par calcul