Clear Sky Science · de
Zusammenstellung der Genomsequenz der 5S rDNA-Loci klärt Haplotypenspezifität und Evolution bei der Großen Entengrütze Spirodela polyrhiza
Warum winzige Schwimmpflanzen wichtig sind
Die Große Entengrütze ist eine kleine Wasserpflanze, die sich schnell über Teiche und Kanäle ausbreitet, doch in ihren Zellen steckt ein überraschend schlankes Genom. Diese Studie untersucht einen der rätselhaftesten Abschnitte dieses Genoms: die DNA‑Abschnitte, die die Kernbausteine für den Proteinaufbau, die Ribosomen der Zelle, kodieren. Durch die vollständige Entschlüsselung dieser schwer lesbaren Regionen in der Entengrütze zeigen die Autorinnen und Autoren, wie essentielle Gene organisiert und feinabgestimmt sind, und liefern Hinweise darauf, wie Pflanzengenome sich entwickeln und wie Zellen eines ihrer grundlegendsten Systeme regulieren.
Bausteine der zellulären Proteinfabriken
Ribosomen, die molekularen Maschinen zur Proteinsynthese, bestehen aus Proteinen und speziellen RNA‑Molekülen. Ein Teil dieser RNAs wird von der sogenannten 5S ribosomalen DNA (5S rDNA) kodiert, die in Pflanzengenomen üblicherweise in Hunderten oder Tausenden nahezu identischer Kopien vorkommt. Weil diese Wiederholungen lang und sehr ähnlich sind, sind sie mit Standard‑Sequenzierverfahren berüchtigt schwer zusammenzusetzen. Bei der Großen Entengrütze (Spirodela polyrhiza) jedoch zeigten frühere Arbeiten, dass die Zahl der 5S‑Kopien ungewöhnlich niedrig ist, was diese Pflanze zu einem idealen Modell macht, um endlich eine ganze 5S rDNA‑Region von Anfang bis Ende zu kartieren und zu sehen, wie ihre Kopien auf den Chromosomen angeordnet sind.
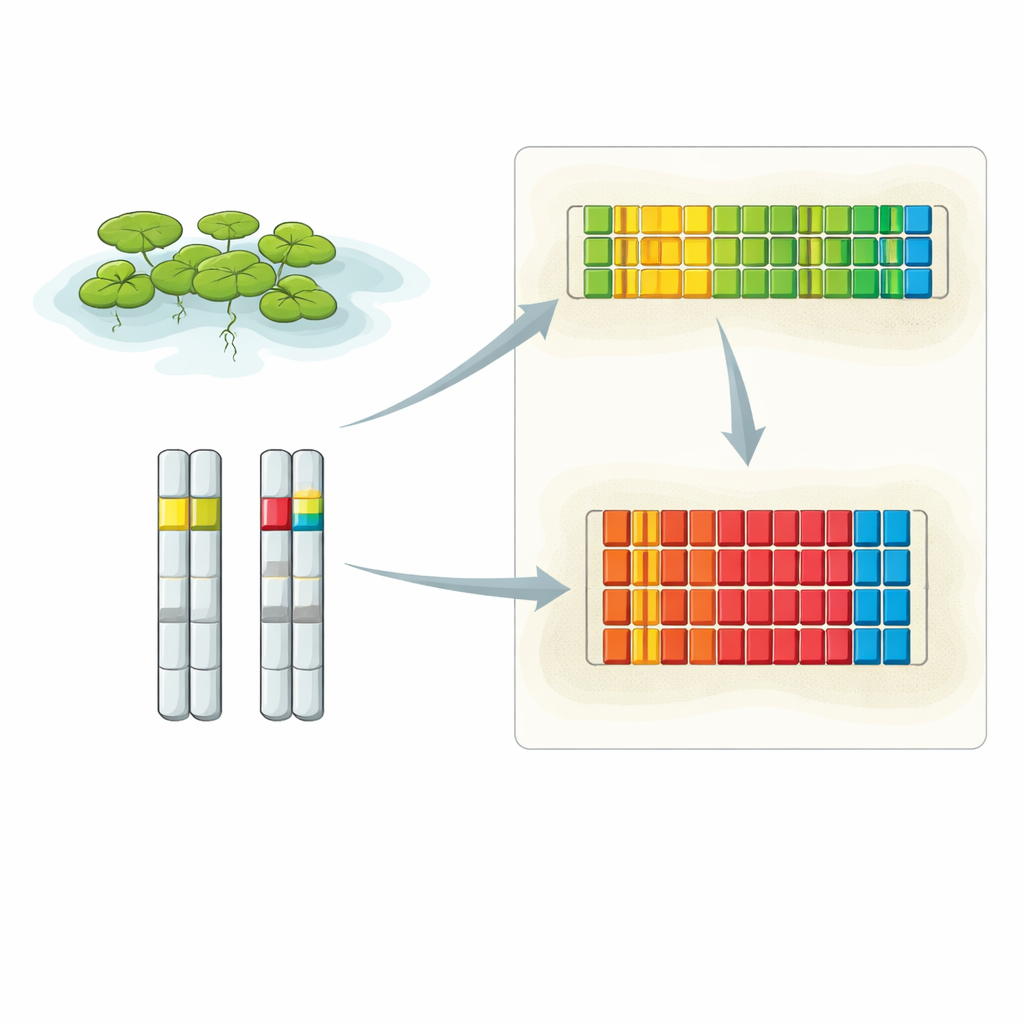
Detailaufnahme zweier zentraler DNA‑Nachbarschaften
Die Forschenden kombinierten mehrere fortschrittliche Techniken, um das vollständige Layout der 5S rDNA in der Entengrütze zu entschlüsseln. Sie nutzten besonders lange DNA‑Reads von Oxford‑Nanopore‑Sequenzierung, konventionelle hochgenaue Sequenzierung von klonierten Fragmenten und hochauflösende Fluoreszenz‑in‑situ‑Hybridisierung (FISH), mit der spezifische DNA‑Abschnitte in intakten Zellkernen sichtbar gemacht werden. Ihre Analysen zeigten, dass die 5S rDNA in zwei Hauptregionen konzentriert ist, jeweils auf unterschiedlichen Chromosomen. Ein Locus liegt auf Chromosom 6 und besteht aus einer Reihe kurzer Wiederholungseinheiten, der andere sitzt auf Chromosom 13 und ist aus längeren Repeats aufgebaut. FISH‑Bilder zeigten, dass die Signalstärke dieser Loci zwischen den beiden Chromosomenkopien in jeder Zelle variiert, was darauf hindeutet, dass ein Homolog deutlich mehr 5S‑Wiederholungen tragen kann als das andere.
Ungleiche Wiederholungen und gespiegelte Cluster
Indem das Team lange Sequenzierreads sorgfältig zusammensetzte, stellten sie nahezu vollständige DNA‑Sequenzen für beide Loci zusammen. Auf einer Variante von Chromosom 6 rekonstruierten sie einen durchgehenden Abschnitt mit 40 5S‑Wiederholungseinheiten; das Partnerchromosom trägt mehr als 65 Einheiten desselben kurzen Typs. Auf Chromosom 13 zeichnet sich eine komplexere Struktur ab: ein großer Cluster von mindestens 64 langen Repeats und ein kleinerer Cluster aus zwei Repeats in entgegengesetzter Orientierung, getrennt durch über 12.000 Basenpaare gewöhnlicher Chromosomen‑DNA. Innerhalb des Lang‑Repeat‑Locus tragen einige Einheiten eine winzige 13‑Basen‑Insertion im Spacer zwischen den Genen, und diese leicht abweichenden Einheiten neigen dazu, sich zu Subclustern zusammenzufinden. Insgesamt machen die beiden Loci zusammen schätzungsweise etwa 320–390 5S‑Genkopien pro diploidem Genom aus, was mit unabhängigen Schätzungen der Kopienzahl übereinstimmt.
DNA‑Chemie und Schaltstellen der Kontrolle
Bei der Untersuchung der chemischen Beschaffenheit dieser Regionen trat ein markantes Muster zutage. Die 5S‑Repeat‑Arrays selbst sind ungewöhnlich reich an den Basen G und C, während die flankierenden Chromosomensegmente stark in A und T angereichert sind. Diese AT‑reichen Randzonen ähneln DNA‑Elementen, die in anderen Organismen mit Replikationsursprüngen und offener, aktiver Chromatinstruktur assoziiert sind, und ähnliche Motive finden sich verstreut auf allen 20 Chromosomen der Entengrütze. Auf der feinen Ebene einzelner Repeat‑Einheiten identifizierte das Team kleine, aber konsistente Unterschiede in kurzen Kontrollsequenzen stromaufwärts und stromabwärts des 5S‑Gens, einschließlich Variationen in TATA‑ähnlichen Motiven und GA‑Wiederholungen. Diese Sequenzen sind aus anderen Arten bekannt dafür, mit allgemeinen Transkriptionsfaktoren und GAGA‑bindenden Proteinen zu interagieren, was darauf hindeutet, dass jeder Locus unterschiedlich abgestimmt sein könnte, obwohl das produzierte 5S‑RNA identisch ist.
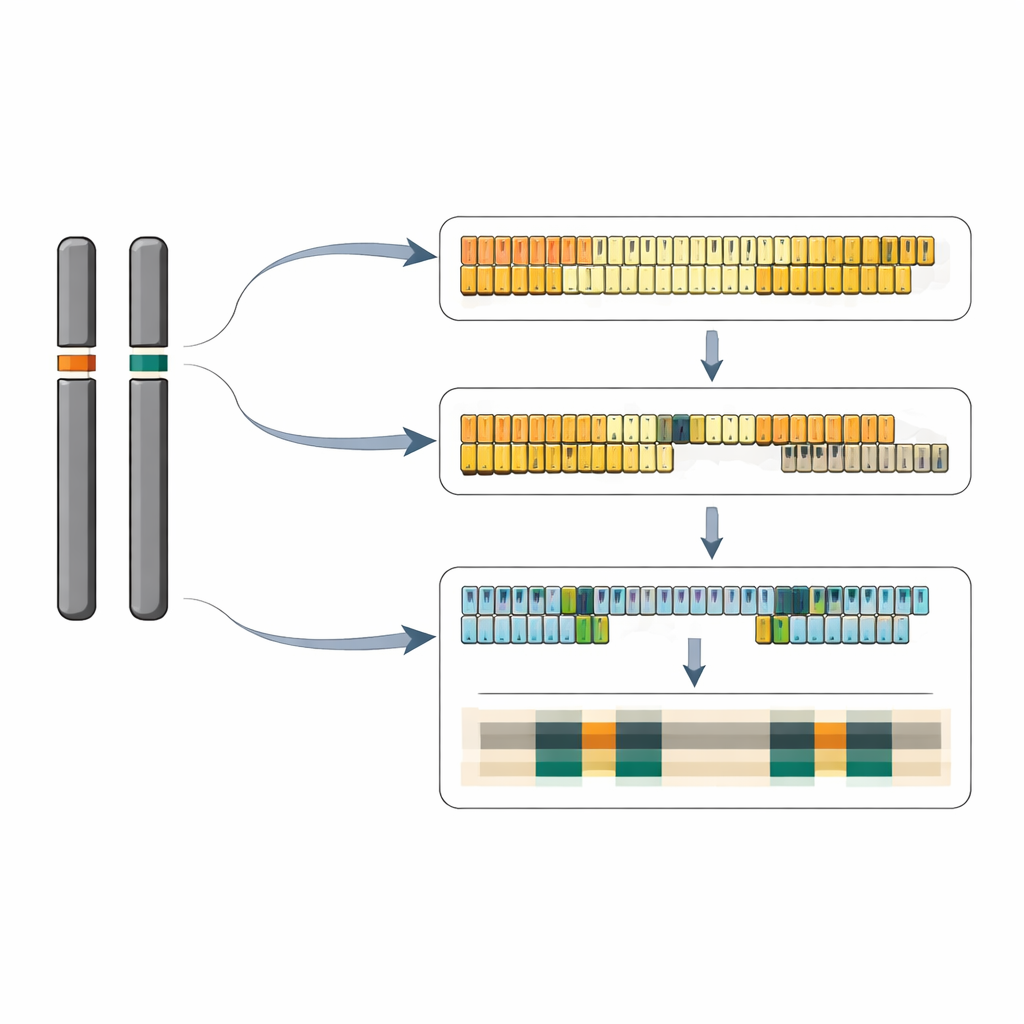
Was das für Pflanzen‑Genome bedeutet
Insgesamt liefert die Arbeit die erste vollständige, nukleotidgenaue Darstellung eines pflanzlichen 5S rDNA‑Systems und zeigt, wie Wiederholungszahl, Sequenzvarianten und der umgebende Chromosomenkontext in einem kompakten Genom zusammenwirken. Die Große Entengrütze scheint im Vergleich zu anderen Blütenpflanzen viele überschüssige ribosomale Genkopien verloren zu haben, bewahrt aber dennoch zwei unterscheidbare, wahrscheinlich aktive 5S‑Loci mit sorgfältig organisierten Clustern von Genvarianten. Die Autorinnen und Autoren schlagen vor, dass beide Loci je nach Bedingungen zur 5S‑RNA‑Produktion beitragen können und dass subtile Unterschiede in Nachbar‑DNA und Spacer‑Sequenzen regulieren, wann und wie stark jeder Cluster genutzt wird. Über die Entengrütze hinaus bietet die Studie eine Blaupause zum Entschlüsseln ähnlicher repetitiver Regionen in anderen Arten und vertieft unser Verständnis dafür, wie essentielle Genfamilien im Verlauf der Evolution geformt werden.
Zitation: Stepanenko, A., Schubert, V., Chen, G. et al. Genome sequence assembly of the 5S rDNA loci informs haplotype specificity and evolution in the greater duckweed Spirodela polyrhiza. Commun Biol 9, 516 (2026). https://doi.org/10.1038/s42003-026-09598-8
Schlüsselwörter: ribosomale DNA, Entengrütze-Genom, Pflanzengenetik, repetitive DNA, Genom‑Evolution