Clear Sky Science · de
Wachstumsdynamik von 3.909 Escherichia-coli-Einzelgen‑Deletionen in nährstoffreichem und minimalem Medium
Warum das Verfolgen bakteriellen Wachstums wichtig ist
Bakterien sind allgegenwärtig, von unserem Darm bis zu industriellen Fermentern, und ihr Erfolg hängt davon ab, wie schnell und wie gut sie wachsen. Selbst für den vertrauten Labororganismus Escherichia coli fehlen Wissenschaftlern jedoch noch detaillierte, standardisierte Aufzeichnungen darüber, wie Tausende verschiedener genetischer Varianten sich im Zeitverlauf vermehren. Dieser Artikel stellt einen großen, sorgfältig organisierten Datensatz vor, der erfasst, wie nahezu viertausend E.-coli-Stämme, jeweils mit einem fehlenden Einzelgen, in nährstoffreichem und minimalem Medium wachsen. Die Ressource ist als gemeinsame Grundlage gedacht, die jede*r nutzen kann, um neue Fragen zu Genen, Umweltbedingungen und bakteriellen Verhaltensweisen zu untersuchen.
Viele Mutantenstämme, zwei sehr unterschiedliche Nährbedingungen
Die Arbeit basiert auf der Keio-Sammlung, einer bedeutenden Bibliothek von E.-coli-Stämmen, in der fast jedes nicht-essentielle Gen präzise entfernt wurde. Aus dieser Sammlung untersuchten die Autor*innen 3.909 unterschiedliche Mutanten. Jede wurde parallel in zwei Arten von Flüssignährmedien kultiviert: einer nährstoffreichen Brühe und einem minimalen Medium, das nur grundlegende Salze, Vitamine und einen einzelnen Zucker enthält. Diese kontrastierenden Nährbedingungen entsprechen einem Festmahl versus einer einfachen Überlebensration und ermöglichen es Forschenden zu erkennen, wie sich fehlende Gene unter Fülle im Vergleich zu Knappheit auswirken. 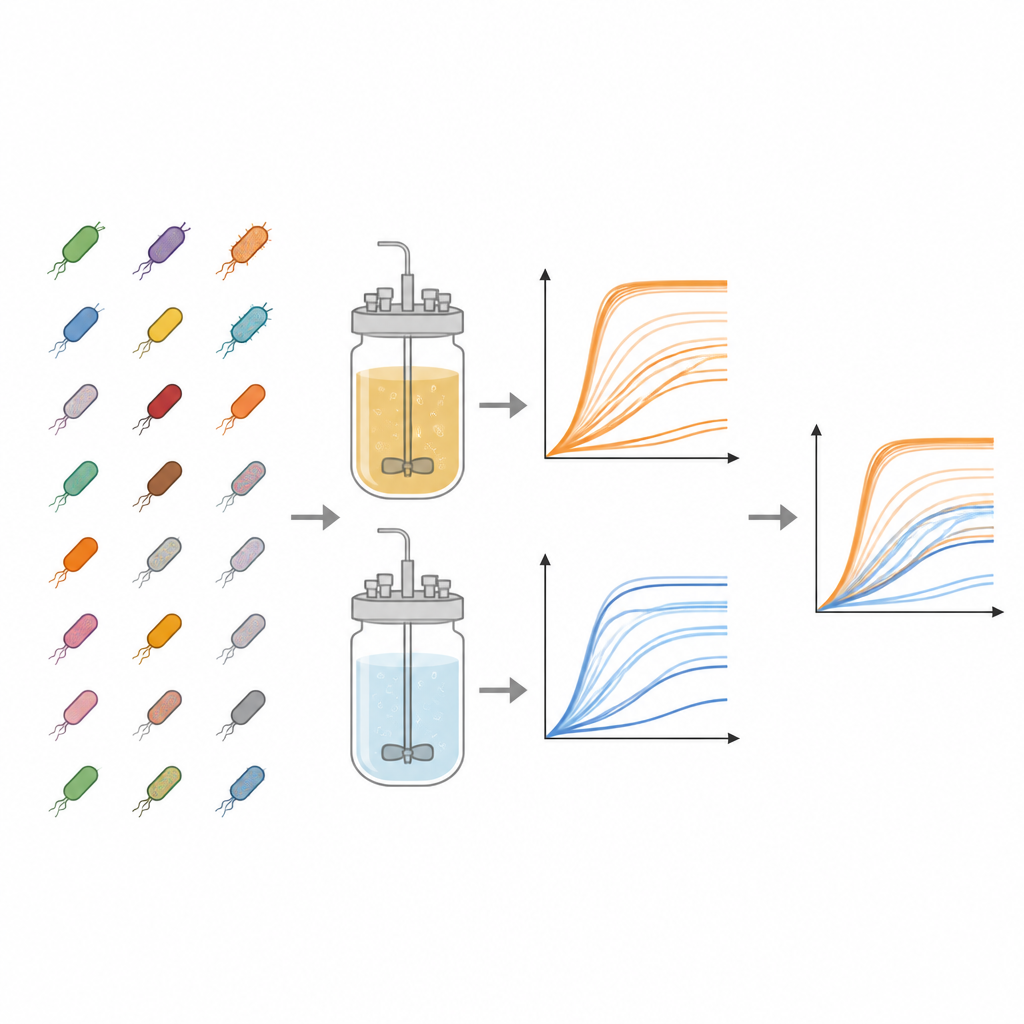
Hochdurchsatz-Monitoring des Wachstums über die Zeit
Um zu verfolgen, wie sich jeder Stamm vermehrte, nutzte das Team standardisierte Kunststoffplatten mit 96 kleinen Vertiefungen, füllte jede Vertiefung mit Medium und einer kleinen Menge aufgetauter Bakterien. Die Platten wurden bei körperähnlicher Temperatur mit Schütteln inkubiert, während ein Gerät die Trübung jeder Vertiefung alle 15 Minuten bis zu zwei Tage lang maß. Die Trübung, gemessen als optische Dichte bei 600 Nanometern, nimmt mit der Zellvermehrung zu und ergibt eine Wachstumskurve, die Lag-Phase, schnelles Wachstum und schließlich Sättigung zeigt. Für jede Kombination aus Stamm und Medium führten die Forschenden drei unabhängige Experimente durch, wodurch insgesamt 23.454 einzelne Wachstumskurven entstanden. Sie zogen einen plattenspezifischen Hintergrundwert ab, um die Daten zu bereinigen, und speicherten alle Zeitpunkte in zugänglichen Tabellen-Dateien.
Von Rohkurven zu einfachen Kennzahlen
Weil Wachstumskurven reichhaltig, aber komplex sind, berechneten die Autor*innen zusätzlich zwei weit verbreitete Zusammenfassungsgrößen für jede Kurve. Die eine ist die Tragfähigkeit (carrying capacity), die ungefähre maximale Trübung, welche die Dichte der Kultur widerspiegelt. Die andere ist die maximale Wachstumsrate, der steilste Abschnitt der Kurve, der angibt, wie schnell sich die Population in ihrer schnellsten Phase ausbreitet. Diese Werte wurden von einem Python-Programm direkt aus den unglätteten Messwerten mithilfe kurzer Fenster aufeinanderfolgender Zeitpunkte extrahiert, und die Forschenden markierten Fälle, in denen unvollständige Kurven oder rauschende Daten das Ergebnis verzerren könnten. Im Allgemeinen waren sowohl die maximale Populationsgröße als auch die schnellste Wachstumsrate in der nährstoffreichen Brühe höher als im minimalen Medium, wie man aus ernährungswissenschaftlicher Sicht erwarten würde. 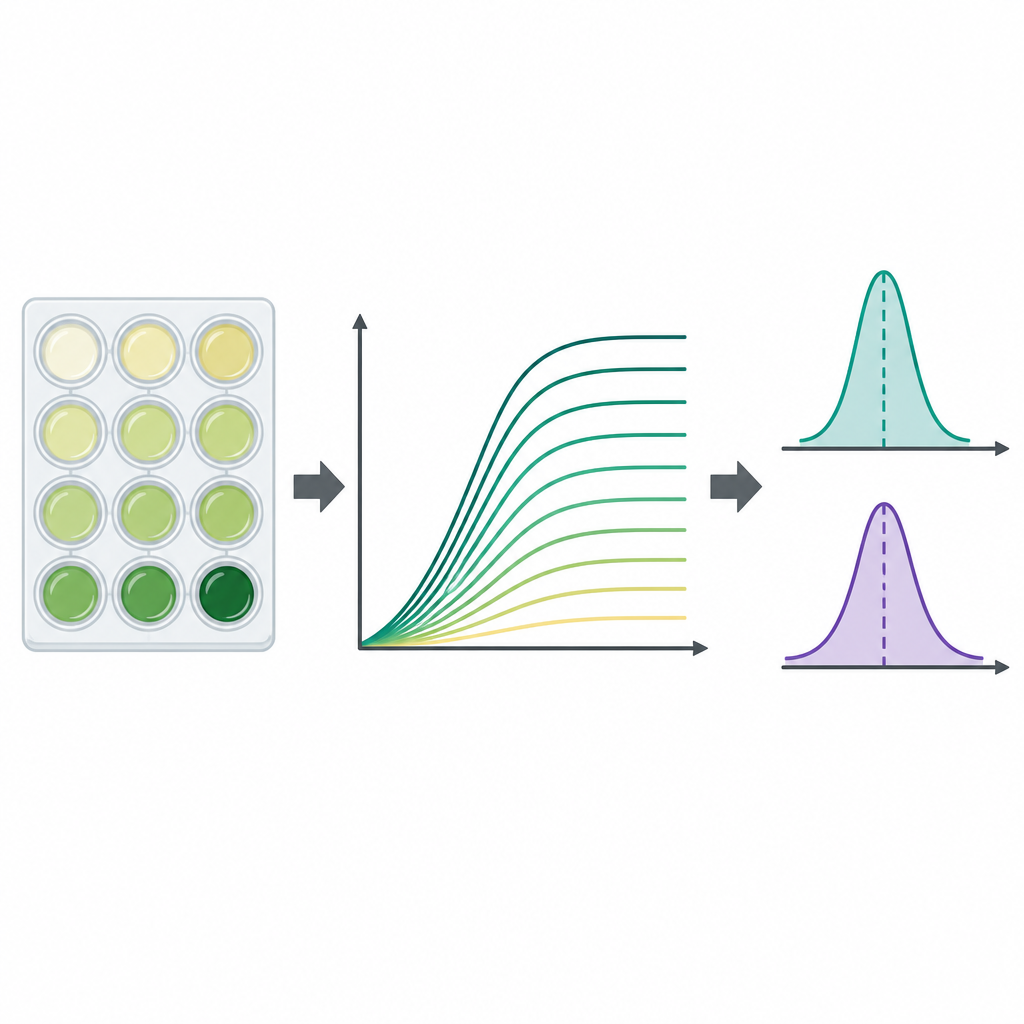
Qualitätskontrollen und Nutzungsmöglichkeiten der Daten
Hochdurchsatzexperimente können anfällig für subtile Fehler sein, daher quantifizierten die Autor*innen sorgfältig, wie reproduzierbar ihre Messungen sind. Für jeden Stamm und jedes Medium verglichen sie die drei Replikate und berechneten, wie sehr Tragfähigkeit und Wachstumsrate variierten. Sie fü gten auch Kennzeichen für potenzielle Ausreißer und für Kurven hinzu, bei denen wichtige Phasen aufgrund des festen Aufzeichnungsfensters möglicherweise verpasst wurden. All diese Informationen sind mit den Hauptdatendateien gebündelt, sodass zukünftige Nutzer*innen die Teilmengen auswählen können, die ihren eigenen Qualitätsstandards am besten entsprechen. Der Datensatz ist maschinenlesbar formatiert und wird von Genbezeichnungen, Identifikatoren und groben funktionalen Kategorien für jedes gelöschte Gen begleitet.
Was diese Ressource für künftige Studien bedeutet
Anstatt eine einzelne biologische Aussage zu treffen, liefert dieser Artikel eine gemeinsame, gut dokumentierte Landkarte darüber, wie Tausende von E.-coli-Mutanten in zwei kontrastierenden Umgebungen wachsen. Indem jede Messzeit und jede Zuverlässigkeitsmarke öffentlich verfügbar gemacht wird, laden die Autor*innen andere dazu ein, die Kurven neu zu analysieren, neue mathematische Methoden zu testen und Wachstumsverhalten mit Genfunktionen, Stoffwechselnetzwerken oder anderen Datenschichten der Zelle zu verknüpfen. Für Nicht‑Spezialist*innen ist die Kernbotschaft, dass das Wachstum von Bakterien gemeinsam von ihren Genen und ihrer Umgebung geformt wird und dass ein gemeinsamer Datensatz wie dieser es vielen Gruppen deutlich erleichtert, diese Einflüsse konsistent zu untersuchen und zu vergleichen.
Zitation: Lao, Z., Ying, BW. Growth dynamics of 3,909 Escherichia coli single-gene knockouts in rich and minimal media. Sci Data 13, 717 (2026). https://doi.org/10.1038/s41597-026-07075-9
Schlüsselwörter: bakterielles Wachstum, Escherichia coli, Genlöschungen, Wachstumskurven, mikrobielle Phänotypisierung