Clear Sky Science · de
HRCHY-CytoCommunity erkennt hierarchische Gewebeorganisation in zelltypischen Raumkarten
Wie Zellen Nachbarschaften in unserem Gewebe aufbauen
Unsere Organe sind nicht einfach nur Zellansammlungen; sie sind sorgfältig geordnete Städte, in denen verschiedene Zell"nachbarn" zusammenarbeiten, um uns am Leben zu erhalten – und im Krankheitsfall mitunter gegen uns. Neue Bildgebungs- und Sequenzierverfahren können inzwischen festhalten, wo jede Zelle in einem Gewebeschnitt sitzt und was sie gerade tut. Aus diesen überwältigenden räumlichen Details Sinn zu ziehen, ist jedoch schwierig. Diese Studie stellt HRCHY‑CytoCommunity vor, eine rechnerische Methode, die automatisch rekonstruiert, wie Zellen sich zu Nachbarschaften und größeren Bezirken in gesunden Organen und Tumoren zusammenfügen, und diese Muster mit klinischen Ergebnissen verknüpft.
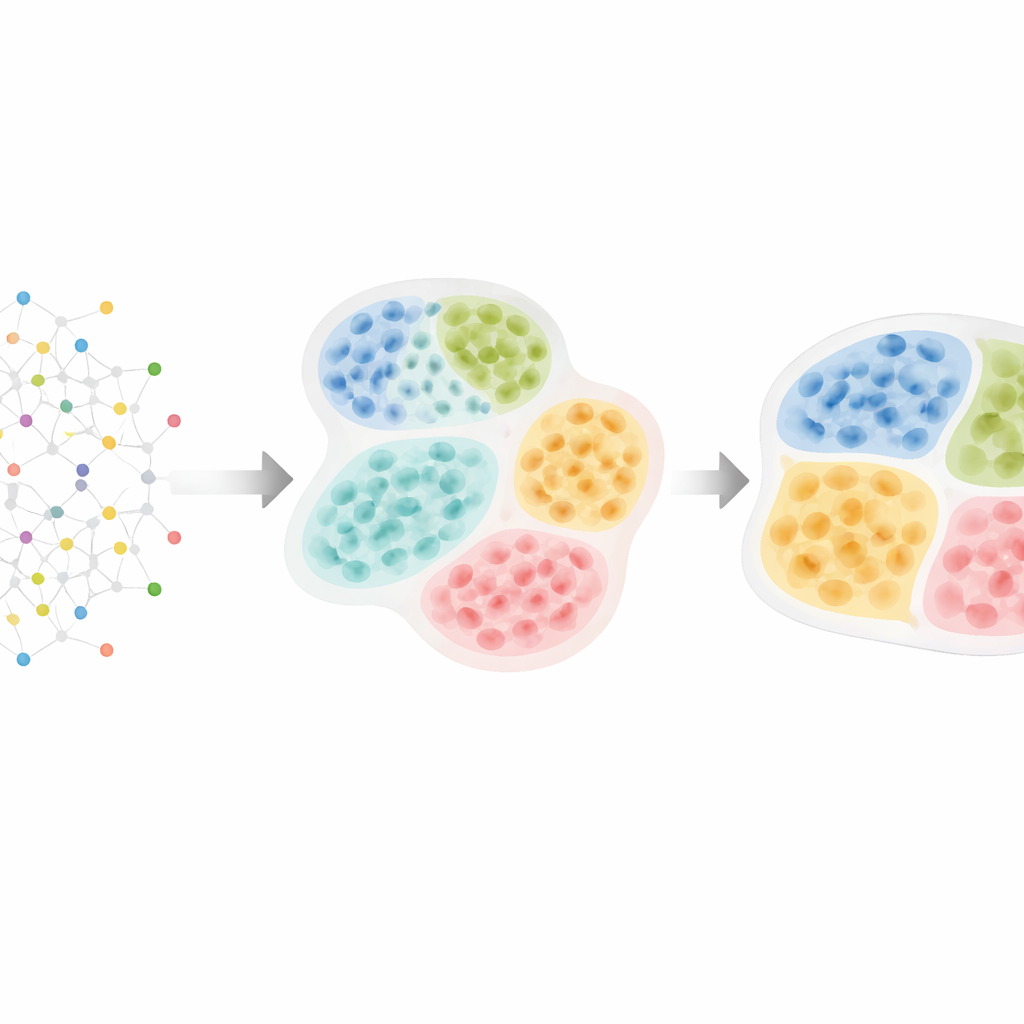
Von Zellkarten zur verborgenen Gewebestruktur
Moderne räumliche „Omics“-Technologien messen Tausende von Molekülen in Zehntausenden bis Hunderttausenden von Zellen, während deren genaue Lage im Gewebe erhalten bleibt. Forschende wissen, dass Zellen sich in Schichten, Zonen und Kompartimenten organisieren – etwa Immun‑ versus Tumorregionen in Tumoren oder verschiedene Kerne im Gehirn. Diese Muster sind bedeutsam: Tumoren, in denen Immunzellen von Krebszellen getrennt liegen, verhalten sich oft anders als solche, in denen sie durchmischt sind; spezielle Immunaggregate, tertiäre lymphoide Strukturen, sagen in mehreren Krebsarten ein besseres Überleben voraus. Die meisten existierenden Computerwerkzeuge ignorieren jedoch diese natürliche Hierarchie oder identifizieren Strukturen nur auf einer einzigen Ebene, sodass es schwerfällt nachzuvollziehen, wie kleine zelluläre Nachbarschaften in größere Gewebebezirke eingebettet sind.
Ein neuer Zugang zum Lesen zellulärer Nachbarschaften
HRCHY‑CytoCommunity begegnet dieser Herausforderung, indem es ein Gewebe als Netzwerk von Zellen behandelt. Jede Zelle ist ein Knoten in einem Graphen, verbunden mit ihren räumlich nächsten Nachbarn. Anstatt direkt auf rohe Gen‑ oder Proteinmessungen zu bauen, verwendet die Methode den Zelltyp jeder Zelle (etwa Krebszelle, T‑Zelle oder Fibroblast) als Haupteingabe. Ein graphisches neuronales Netzwerk lernt dann Muster, wie sich diese Zelltypen anordnen. In einem Schritt gruppiert es nahe beieinander liegende Zellen zu feinmaßstäbigen „zellulären Nachbarschaften“. In einem zweiten Schritt fasst es diese Nachbarschaften zu gröberen „Gewebekompartimenten“ zusammen, wobei sichergestellt wird, dass jede Zelle genau zu einer Nachbarschaft gehört und jede Nachbarschaft sauber in einem einzelnen Kompartiment liegt. Besondere Trainingsstrategien – wie das Beschneiden schwacher Verbindungen, das Hinzufügen von zufälligem Rauschen und das Fördern stabiler, ausgewogener Cluster – helfen der Methode, fragile oder triviale Gruppierungen zu vermeiden.
Strukturen finden über Organe, Technologien und Krankheiten hinweg
Die Autorinnen und Autoren testeten HRCHY‑CytoCommunity an einer breiten Palette räumlicher Datensätze von Maus und Mensch, die sowohl bildgebungsbasierte Protein‑Karten als auch sequencingbasierte RNA‑Karten abdecken und von Milz über Gehirn und Darm bis zu Tumoren reichen. In der Maussplene rekonstruierte die Methode klassische Strukturen wie das rote Mark und lymphoide Regionen, selbst wenn diese Regionen in diskrete Flicken zerteilt waren. In kolorektalem Tumorgewebe trennte sie Tumor‑ und Normalbereiche klar und hob unterschiedliche Nachbarschaften an Tumorrändern und -kernen hervor. In Hirnregionen der Maus zeichnete sie bekannte, oft sehr kleine Kerne und kortikale Schichten präzise nach, die viele andere Methoden verwischten, und sie bewältigte sehr große Datensätze mit Hunderttausenden von Messpunkten in nur wenigen Minuten. Das Framework funktioniert auch, wenn jeder gemessene Spot Mischungen von Zelltypen enthält: Indem zunächst abgeschätzt wird, welche Zellen in jedem Spot vorhanden sind, lassen sich dennoch anatomisch sinnvolle Schichten und Subregionen rekonstruieren.
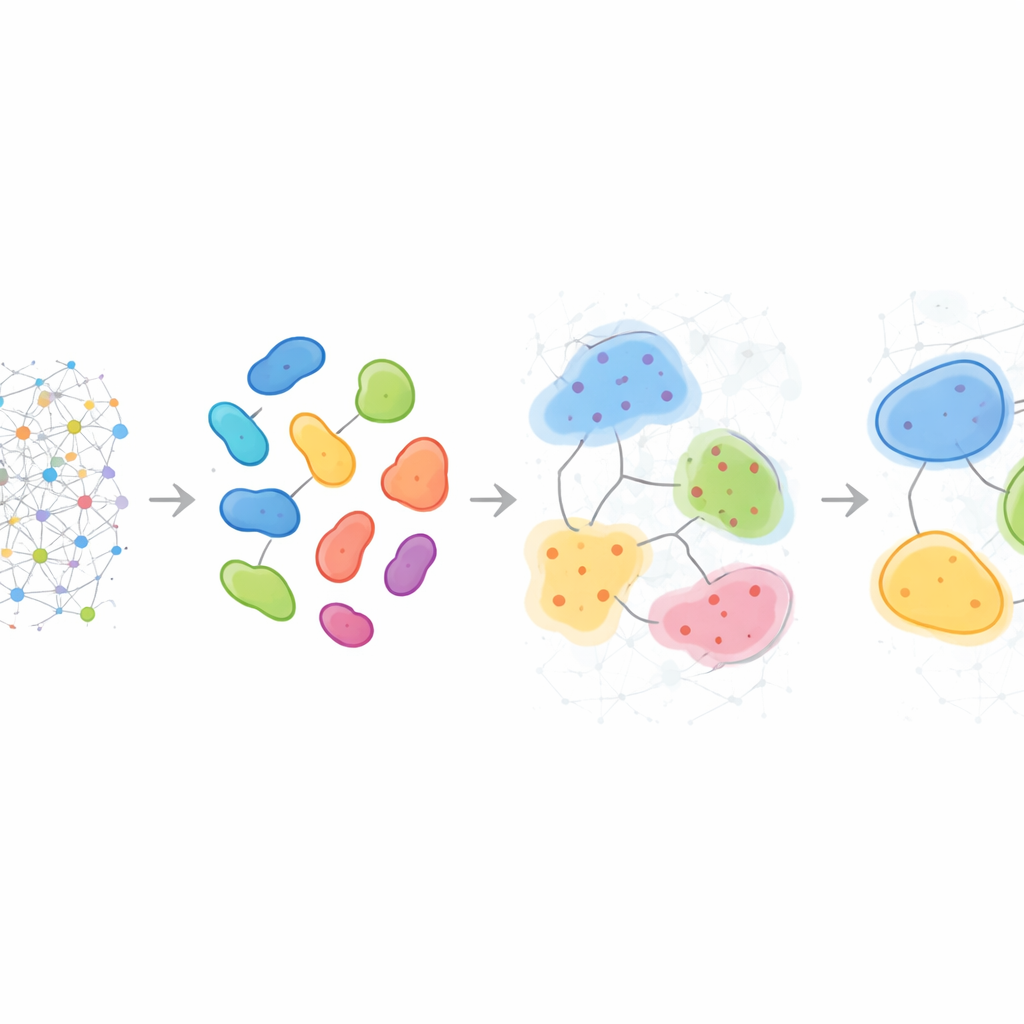
Muster, die von Patient zu Patient variieren
Über die Beschreibung einzelner Proben hinaus kann HRCHY‑CytoCommunity Nachbarschaften und Kompartimente über viele Patientinnen und Patienten hinweg ausrichten, um ein gemeinsames „Vokabular“ multizellulärer Strukturen zu definieren. Beim triple-negativen Brustkrebs fand die Methode konsistent breite, immunreiche und krebseriche Kompartimente, doch die feineren Nachbarschaften darin unterschieden sich von Person zu Person. Manche Tumoren enthielten einzigartige Kombinationen aus Makrophagen, T‑Zellen und Blutgefäßen oder gemischte Krebs–Neutrophil‑Flecken, was individualisierte Mikroökologien offenbarte, die sich einfachen Zellzahlauswertungen entziehen. Auf eine große Brustkrebskohorte angewandt, halfen diese mehrstufigen Strukturen, Patientinnen und Patienten nach Überleben zu stratifizieren: Ein Kompartiment, das in einem bestimmten Krebszellphänotyp angereichert war, kennzeichnete Patienten mit besseren Ergebnissen, während bestimmte Nachbarschaften, reich an Fibroblasten oder speziellen T‑Zell‑ und Makrophagenkombinationen, Gruppen mit deutlich schlechterer Prognose markierten – wahrscheinlich als Ausdruck physischer oder funktionaler Barrieren für eine effektive antitumorale Immunantwort.
Was das für das Verständnis und die Behandlung von Krankheiten bedeutet
Indem komplexe räumliche Karten von Zelltypen in eine klare Hierarchie aus Nachbarschaften und Bezirken übersetzt werden, bietet HRCHY‑CytoCommunity eine kraftvolle Linse dafür, wie Gewebe aufgebaut sind und wie sie in Krankheit zusammenbrechen. Die Fähigkeit der Methode, über verschiedene experimentelle Plattformen hinweg zu arbeiten, enorme Datensätze zu bewältigen und eine vollständige, verschachtelte Abdeckung der Zellen zu liefern, macht sie zu einem praktischen Werkzeug für Grundlagenforschung und klinische Studien. Bei Krebs kann sie Mikroarchitekturen aufdecken, die mit Überleben und Therapierespons verknüpft sind; in gesunden Organen kann sie kartieren, wie spezialisierte Regionen zusammenwirken. Letztlich könnten Ansätze wie dieser Ärztinnen und Ärzten helfen, Gewebeorganisation so routinemäßig zu interpretieren wie heute Laborwerte, und so präzisere Diagnosen und Behandlungen zu ermöglichen.
Zitation: Xie, R., Wang, Z., Liu, J. et al. HRCHY-CytoCommunity identifies hierarchical tissue organization in cell-type spatial maps. Nat Commun 17, 3312 (2026). https://doi.org/10.1038/s41467-026-70069-z
Schlüsselwörter: räumliche Omics, Gewebearchitektur, graphische neuronale Netze, Tumormikroumgebung, zelluläre Nachbarschaften