Clear Sky Science · zh
胎儿特异性的造血祖细胞从卵黄囊和脐动脉的成血内皮产生
早期造血如何塑造终生格局
在我们出生之前,必须迅速建立起一个能维持不断增长胎儿生命的血液与免疫系统。本文探讨小鼠胚胎中新发现的一类“早期一代”造血细胞——它们在胎儿期高度活跃,但在出生后大多消失。弄清这些短寿命细胞如何以及从何处产生,有助于解释儿童的血液与免疫系统为何不同于成人,并可能揭示一些起源于胎内的疾病机制。
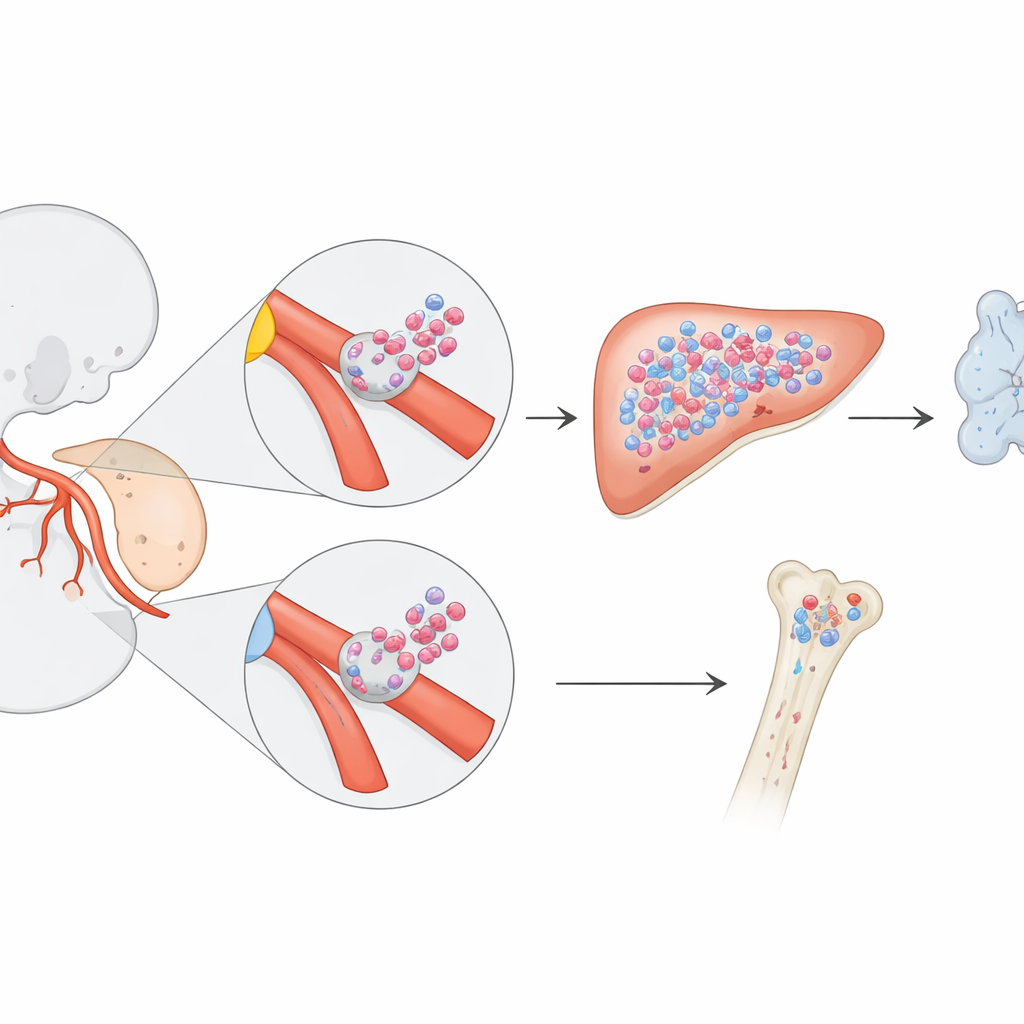
被隐藏的一代造血细胞
胚胎发育过程中,血细胞的产生呈波次进行。早期工作表明,能在成年期维持终生造血的长寿干细胞出现在靠近胚胎主动脉的区域。但研究者猜测还可能存在仅在胎内出现的特殊祖细胞——在出生前建立大部分血液和免疫系统,随后逐渐消失。为追踪这些难以捉摸的细胞,作者在小鼠中使用了遗传学的“时间戳”。通过在特定的内皮细胞(即衬里血管并能转化为造血细胞的细胞)上短暂激活标记,他们追踪了这些细胞的后代从胚胎早期到成体的命运。
精确定位胎儿特异性细胞的来源
通过精确改变激活标记的时间,团队可以标记不同波次出现的造血细胞。当他们在胚胎第8.5天标记成血内皮时,观察到一个显著的模式:晚孕期胎儿中许多血液与免疫细胞带有该标记,但出生后带标记的细胞明显减少。精细成像显示,这些被标记的祖细胞最初以从两条关键血管壁出芽的细胞簇形式出现——即连接胚胎与卵黄囊并通向胎盘的卵黄囊动脉和脐动脉。这些细胞簇比背主动脉中经典的长期干细胞出现得更早,代表了先前未被认识到的造血来源。
供养胎儿免疫系统,然后让位
研究者接着询问这些胎儿特异性祖细胞实际承担什么功能。利用流式细胞术检查血液和器官,他们发现第8.5天被标记的细胞供献了胎儿B细胞的大部分、许多T细胞以及大量胎儿髓系细胞——这些髓系细胞负责抗感染并参与组织建构。然而出生后,它们的贡献逐步下降,另一波在更晚时间点被标记的典型成年型干细胞逐渐接管。这一“交接”揭示了分层的体系:一种为快速胎儿生长和免疫播种优化的早期方案,随后是为终身维持而设计的持久成年方案。
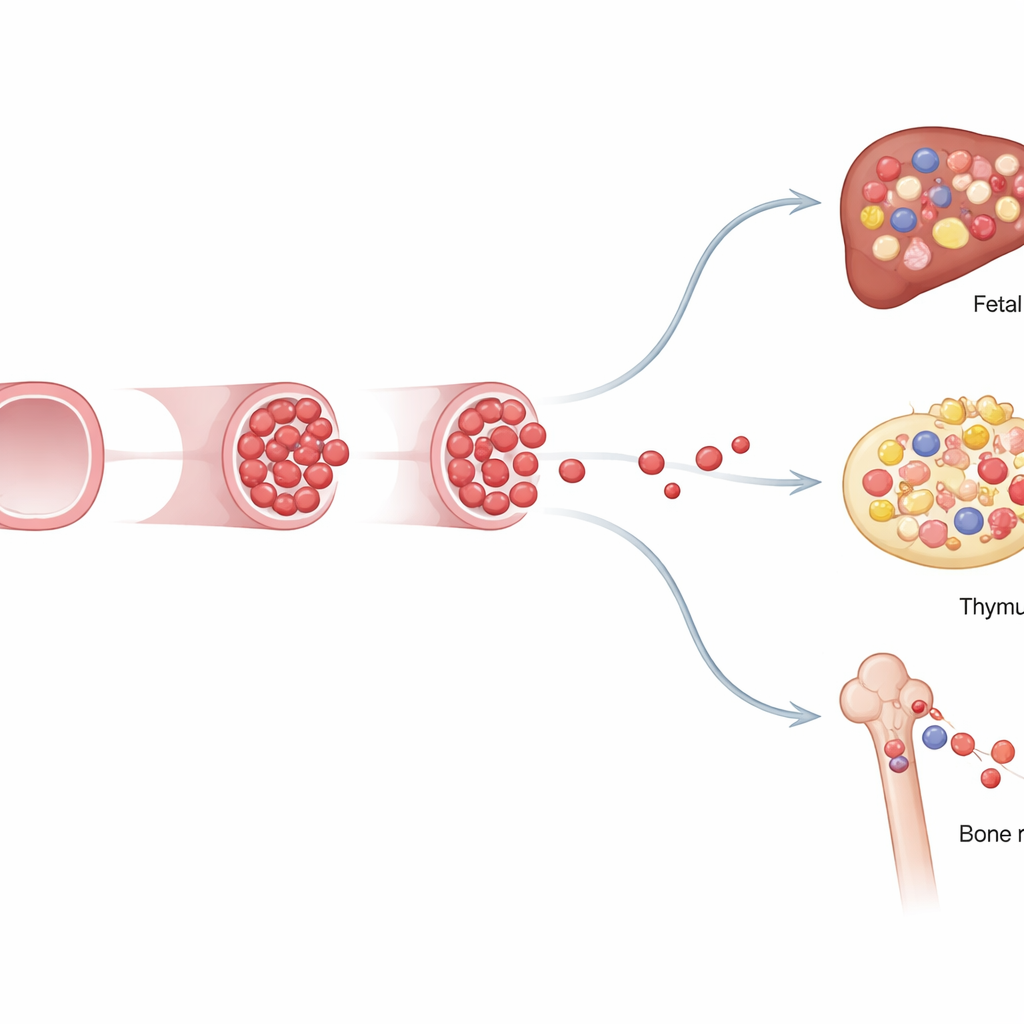
独特身份与有限的持续能力
为探明这些胎儿特异性细胞与成年干细胞的差异,团队将它们移植到受照射的小鼠体内,并对单细胞基因活动进行分析。移植实验显示,胎儿特异性祖细胞能在受体内短暂重建多条血液与免疫谱系,但在二次移植中其供献显著衰退,表明其长期自我更新能力有限。单细胞RNA测序显示,这些细胞具有混合身份:有些更像未成熟的类干前体,而另一些已被激活为特定免疫细胞,尤其是淋巴细胞。它们的基因表达与能量代谢模式也因来源不同而异——来自胚内血管或靠近卵黄囊的胚外动脉的细胞在特性上存在差别,强调了位置如何塑造细胞命运。
为何这波早期造血重要
该研究表明,在经典干细胞出现之前,一股短寿但功能强大的造血祖细胞波次自位于卵黄囊和脐动脉的特化血管内皮产生。这些胎儿特异性祖细胞构建了胎儿大部分的血液与免疫系统,然后逐步被居于骨髓的成年型干细胞取代。对于非专业读者,关键结论是:我们的血液系统并非由单一、超然的干细胞构建,而是由几代承担不同任务与寿命的细胞接力完成。认识到这股早期胎儿波次,能够更精确地描述血液与免疫多样性如何形成,并可能有助于解释为何一些儿童期的血液疾病与白血病可追溯到发生在出生前的事件。
引用: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
关键词: 胚胎造血, 胎儿血液干细胞, 卵黄囊和脐动脉, 成血内皮, 胎儿免疫发育