Clear Sky Science · pt
Progenitores hematopoiéticos restritos ao feto surgem do endotélio hemogênico nas artérias vitelina e umbilical
Como a formação precoce do sangue molda uma vida inteira
Antes de nascermos, nossos corpos precisam montar rapidamente um sistema sanguíneo e imunológico funcional para manter o feto em crescimento vivo. Este artigo explora uma “geração precoce” recém‑descoberta de células formadoras de sangue em embriões de camundongo que atuam intensamente durante a vida fetal, mas desaparecem em grande parte após o nascimento. Entender como e onde essas células de curta duração surgem ajuda a explicar por que o sangue e o sistema imune de crianças diferem dos de adultos e pode lançar luz sobre doenças que têm início antes do nascimento.
Uma geração oculta de construtoras do sangue
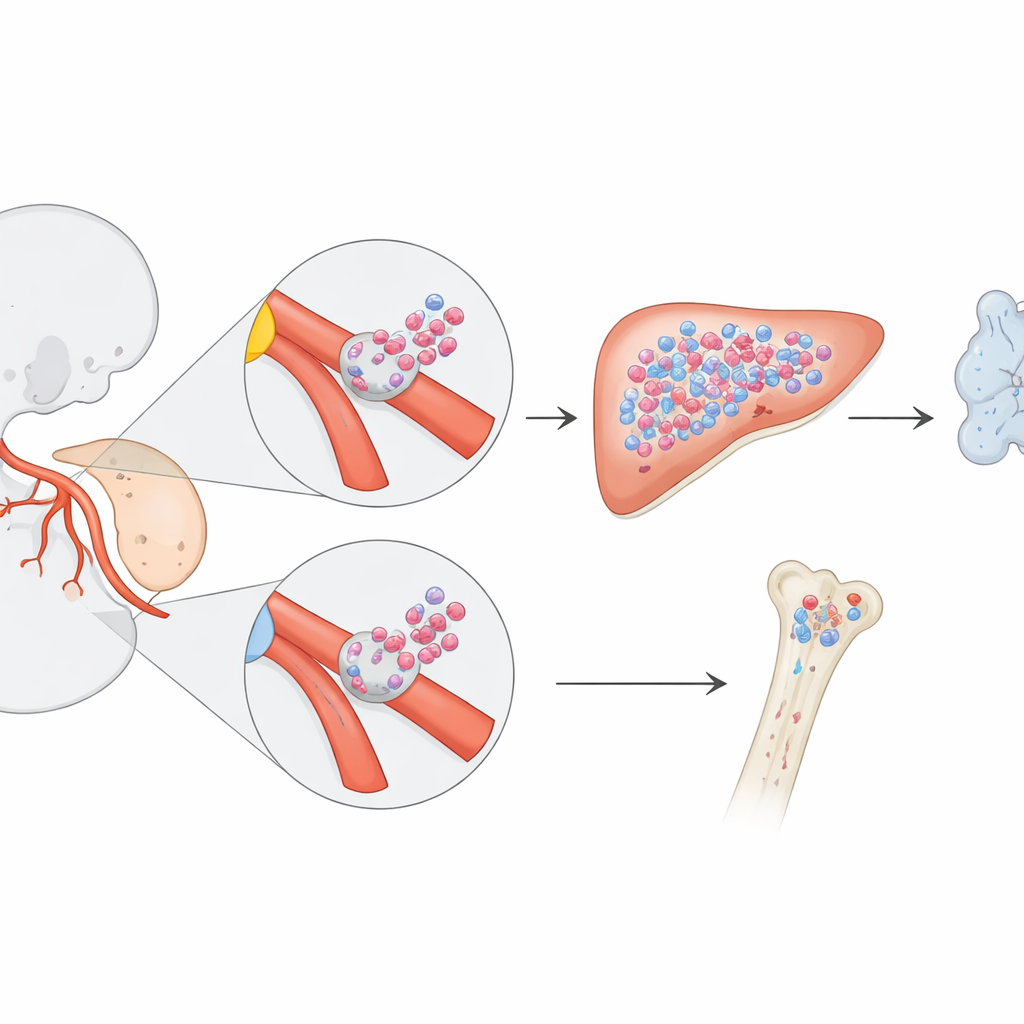
As células sanguíneas são produzidas em ondas conforme o embrião se desenvolve. Trabalhos anteriores mostraram que células‑tronco de longa duração, que sustentam a produção de sangue ao longo da vida adulta, aparecem em uma região próxima à aorta embrionária. Mas os pesquisadores suspeitavam que também poderia existir progenitores especiais exclusivos do feto — células que constroem a maior parte do sangue e do sistema imunológico antes do nascimento e depois desaparecem. Para acompanhar essas células elusivas, os autores usaram “carimbos temporais” genéticos em camundongos. Ao ativar brevemente um marcador em endotélio específico — as células que revestem os vasos sanguíneos e podem se transformar em células formadoras de sangue — eles seguiram o destino de seus descendentes desde os primeiros dias embrionários até a vida adulta.
Localizando de onde vêm as células exclusivas do feto
Ao mudar exatamente quando ativavam o marcador, a equipe pôde rotular diferentes ondas de células sanguíneas emergentes. Quando marcaram o endotélio hemogênico no dia embrionário 8,5, observaram um padrão marcante: muitas células sanguíneas e imunológicas no feto em fase tardia de gestação carregavam o rótulo, mas muito menos o faziam após o nascimento. Imagens detalhadas mostraram que esses progenitores rotulados surgiam primeiro como aglomerados de células brotando das paredes de dois vasos-chave — as artérias vitelina e umbilical, que conectam o embrião e o saco vitelínico à placenta. Esses aglomerados se formaram antes das clássicas células‑tronco de longo prazo na aorta dorsal e representaram uma fonte de células formadoras de sangue anteriormente não reconhecida.
Alimentando o sistema imune fetal, depois cedendo o lugar
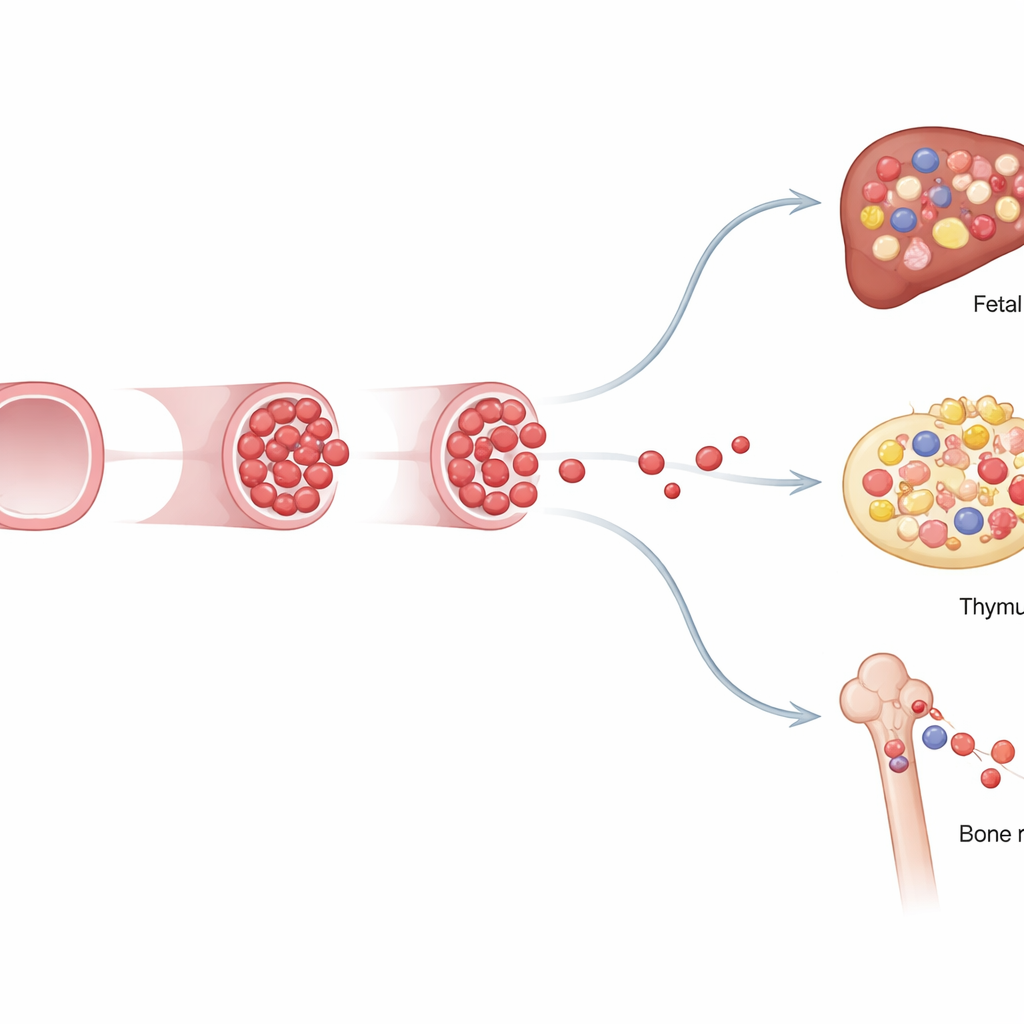
Os pesquisadores então investigaram o que esses progenitores restritos ao feto realmente fazem. Usando citometria de fluxo para examinar sangue e órgãos, eles descobriram que células marcadas ao dia 8,5 contribuíram com a maioria das células B fetais, muitas células T e uma grande parcela das células mieloides fetais — glóbulos brancos que combatem infecções e ajudam a construir tecidos. Ainda assim, após o nascimento, sua contribuição diminuiu de forma constante à medida que outra onda de células formadoras de sangue, as clássicas células‑tronco do tipo adulto marcadas em um ponto temporal mais tardio, assumiu o controle. Essa “passagem de bastão” revelou um sistema em camadas: um programa inicial otimizado para rápido crescimento fetal e semeadura imune, seguido por um programa adulto durável projetado para manutenção ao longo da vida.
Identidades distintas e poder de permanência limitado
Para sondar como esses progenitores restritos ao feto diferem das células‑tronco adultas, a equipe os transplantou em camundongos irradiados e analisou sua atividade gênica célula a célula. Os transplantes mostraram que os progenitores fetais restritos podiam reconstruir brevemente múltiplas linhagens sanguíneas e imunes nos recipientes, mas sua contribuição diminuiu em transplantes secundários, indicando pouca autorrenovação a longo prazo. Sequenciamento de RNA de célula única revelou que essas células apresentam uma identidade mista: algumas se assemelham mais a precursores imaturos com traços de célula‑tronco, enquanto outras já estão inclinadas a se tornar células imunes específicas, especialmente linfócitos. Seus padrões de atividade gênica e uso de energia também diferiram dependendo se vinham de vasos intra‑embrionários ou de artérias extraembrionárias próximas ao saco vitelínico, reforçando que a localização molda seu destino.
Por que essa onda sanguínea precoce importa
Este estudo mostra que uma onda curta, mas poderosa, de progenitores formadores de sangue surge de células especializadas que revestem vasos nas artérias vitelina e umbilical antes do aparecimento das células‑tronco clássicas. Esses progenitores restritos ao feto constroem grande parte do sistema sanguíneo e imunológico do feto e, então, gradualmente cedem lugar às células‑tronco do tipo adulto que residem na medula óssea. Para o leitor leigo, a conclusão principal é que nosso sistema sanguíneo não é construído por uma única célula‑tronco atemporal, mas por gerações sucessivas de construtores com funções e vidas úteis distintas. Reconhecer essa onda fetal precoce refina nossa compreensão de como a diversidade sanguínea e imune surge e pode ajudar a explicar por que alguns distúrbios sanguíneos infantis e leucemias remontam a eventos que ocorrem bem antes do nascimento.
Citação: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Palavras-chave: hematopoiese embrionária, células‑tronco sanguíneas fetais, artérias vitelina e umbilical, endotélio hemogênico, desenvolvimento imune fetal