Clear Sky Science · es
Los progenitores hematopoyéticos restringidos al feto surgen del endotelio hemogénico en las arterias vitelinas y umbilicales
Cómo la formación temprana de la sangre configura toda una vida
Antes de nacer, nuestros cuerpos deben construir rápidamente un sistema sanguíneo e inmunitario funcional para mantener vivo al feto en crecimiento. Este artículo explora una generación recién descrita de células formadoras de sangre en embriones de ratón que trabajan intensamente durante la vida fetal pero desaparecen en su mayor parte tras el nacimiento. Entender cómo y dónde surgen estas células de corta duración ayuda a explicar por qué la sangre y el sistema inmunitario de los niños difieren de los de los adultos, y puede arrojar luz sobre enfermedades que se inician antes del nacimiento.
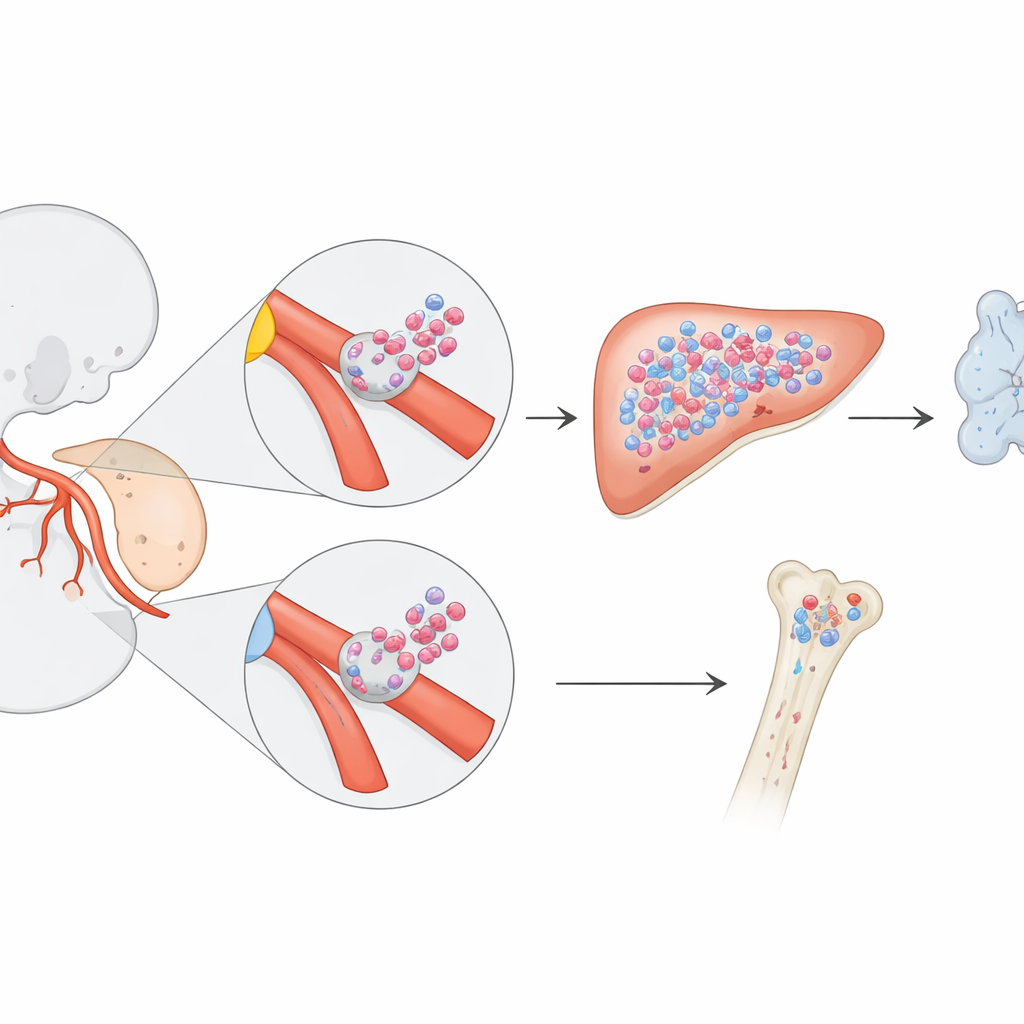
Una generación oculta de células constructoras de sangre
Las células sanguíneas se producen en oleadas a medida que el embrión se desarrolla. Trabajos previos mostraron que las células madre de larga duración, que sostienen la producción de sangre durante la vida adulta, aparecen en una región cercana a la aorta embrionaria. Pero los investigadores sospechaban que también podría existir progenitores especiales exclusivos del feto: células que construyen la mayor parte del sistema sanguíneo e inmunitario antes del nacimiento y luego se desvanecen. Para seguir el rastro de estas células elusivas, los autores usaron “marcas temporales” genéticas en ratones. Activando brevemente un marcador en células endoteliales específicas —las células que recubren los vasos sanguíneos y pueden transformarse en formadoras de sangre—, siguieron el destino de sus descendientes desde los primeros días embrionarios hasta la edad adulta.
Localizar con precisión de dónde proceden las células exclusivas del feto
Al cambiar exactamente cuándo activaban el marcador, el equipo pudo etiquetar diferentes oleadas de células sanguíneas emergentes. Cuando marcaron el endotelio hemogénico en el día embrionario 8.5, observaron un patrón llamativo: muchas células sanguíneas e inmunitarias en el feto en gestación tardía llevaban la etiqueta, pero mucho menos lo hacían tras el nacimiento. Imágenes detalladas mostraron que estos progenitores etiquetados aparecían primero como racimos de células brotando de las paredes de dos vasos clave —las arterias vitelina y umbilical—, que conectan el embrión y el saco vitelino con la placenta. Estos racimos se formaron antes que las clásicas células madre de larga duración en la aorta dorsal y representaron una fuente de células formadoras de sangre hasta entonces no reconocida.
Alimentando el sistema inmunitario fetal y luego retirándose
Los investigadores preguntaron a continuación qué hacen en realidad estos progenitores restringidos al feto. Usando citometría de flujo para examinar sangre y órganos, encontraron que las células marcadas en el día 8.5 contribuyeron a la mayoría de las células B fetales, a muchas células T y a una gran porción de las células mieloides fetales —glóbulos blancos que combaten infecciones y ayudan a construir tejidos. Sin embargo, tras el nacimiento, su contribución fue disminuyendo de forma sostenida a medida que otra oleada de células formadoras de sangre, las clásicas células madre de tipo adulto marcadas en un momento posterior, tomó el relevo. Este “traspaso” reveló un sistema capadeado: un programa temprano optimizado para el rápido crecimiento fetal y la colonización inmunitaria, seguido por un programa adulto duradero diseñado para el mantenimiento durante toda la vida.
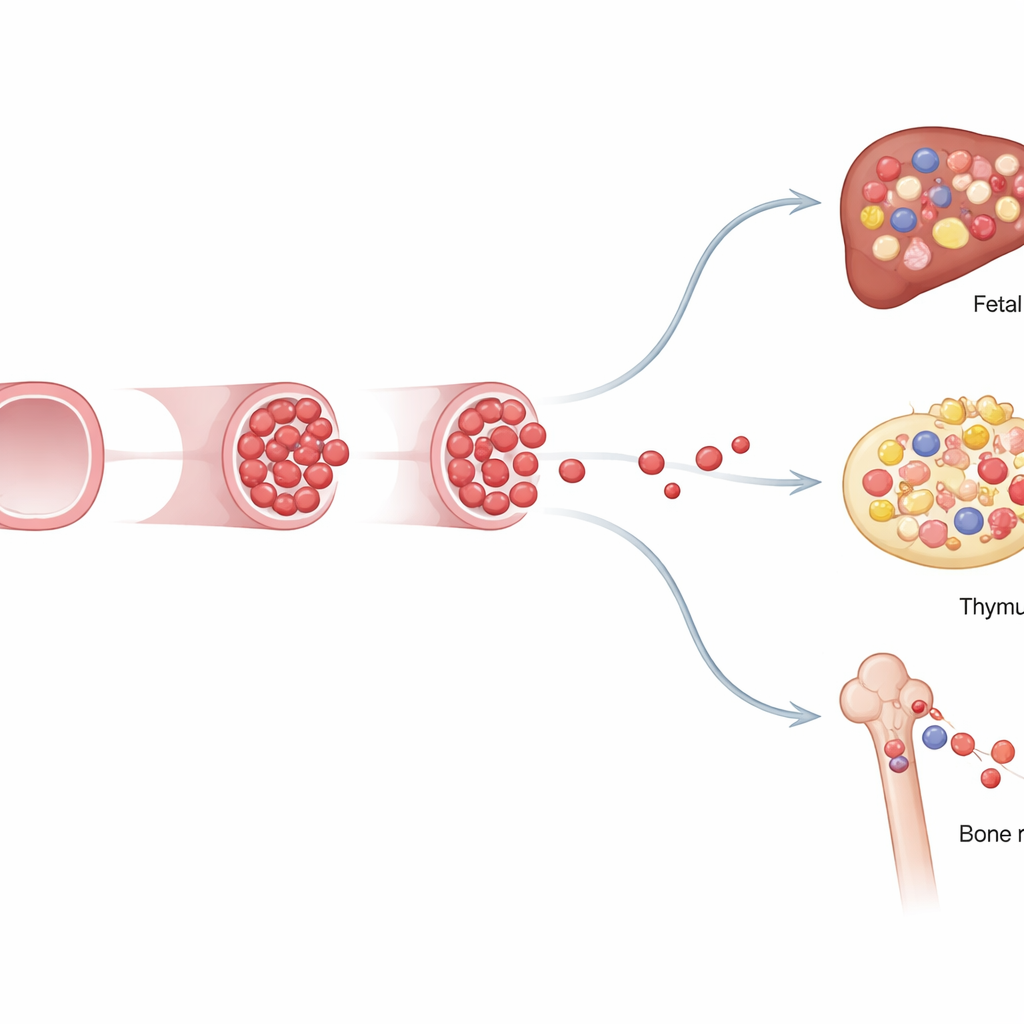
Identidades distintivas y poder de permanencia limitado
Para investigar cómo difieren estas células restringidas al feto de las células madre adultas, el equipo las trasplantó en ratones irradiados y analizó su actividad genética célula por célula. Los trasplantes mostraron que los progenitores restringidos al feto podían reconstruir brevemente múltiples linajes sanguíneos e inmunitarios en los receptores, pero su contribución se debilitó en trasplantes secundarios, lo que indica poca autorrenovación a largo plazo. La secuenciación de ARN de célula única reveló que estas células poseen una identidad mixta: algunas se parecen más a precursores inmaduros con rasgos de célula madre, mientras que otras ya están predispuestas a convertirse en células inmunitarias específicas, especialmente linfocitos. Su actividad génica y los patrones de uso energético también diferían según procedieran de vasos intraembrionarios o de arterias extraembrionarias cercanas al saco vitelino, subrayando que la localización condiciona su destino.
Por qué importa esta oleada temprana de sangre
Este estudio muestra que una oleada potente pero de corta duración de progenitores formadores de sangre surge de células especializadas que recubren los vasos en las arterias vitelina y umbilical antes de que aparezcan las células madre clásicas. Estos progenitores restringidos al feto construyen gran parte del sistema sanguíneo e inmunitario del feto y, a continuación, ceden gradualmente el paso a las células madre de tipo adulto que residen en la médula ósea. Para el lector general, la conclusión clave es que nuestro sistema sanguíneo no lo construye una única célula madre atemporal, sino generaciones sucesivas de constructores con trabajos y longevidades distintas. Reconocer esta oleada fetal temprana afina nuestra visión de cómo surge la diversidad sanguínea e inmunitaria y puede ayudar a explicar por qué algunos trastornos sanguíneos infantiles y leucemias se remontan a eventos que ocurren mucho antes del nacimiento.
Cita: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Palabras clave: hematopoyesis embrionaria, células madre sanguíneas fetales, arterias vitelinas y umbilicales, endotelio hemogénico, desarrollo inmunitario fetal