Clear Sky Science · fr
Des progéniteurs hématopoïétiques à restriction fœtale proviennent de l’endothélium hémogénique dans les artères vitellines et ombilicales
Comment la formation précoce du sang façonne toute une vie
Avant notre naissance, notre organisme doit rapidement construire un système sanguin et immunitaire opérationnel pour maintenir le fœtus en croissance. Cet article explore une « génération précoce » nouvellement découverte de cellules hématopoïétiques chez la souris qui travaillent intensément pendant la vie fœtale mais disparaissent en grande partie après la naissance. Comprendre comment et où ces cellules de courte durée apparaissent aide à expliquer pourquoi le sang et le système immunitaire des enfants diffèrent de ceux des adultes, et peut éclairer des maladies qui prennent leur origine avant la naissance.
Une génération cachée de cellules formatrices de sang
Les cellules sanguines sont produites en vagues au fur et à mesure du développement embryonnaire. Des travaux antérieurs ont montré que des cellules souches à longue durée de vie, qui soutiennent la production sanguine tout au long de la vie adulte, apparaissent dans une région proche de l’aorte embryonnaire. Mais les chercheurs soupçonnaient aussi l’existence de progéniteurs spéciaux réservés au fœtus—des cellules qui fabriquent la majeure partie du sang et du système immunitaire avant la naissance puis s’évanouissent. Pour suivre ces cellules insaisissables, les auteurs ont utilisé des « horodatages » génétiques chez la souris. En activant brièvement un marqueur dans des cellules endothéliales spécifiques—les cellules qui tapissent les vaisseaux sanguins et peuvent se transformer en cellules formatrices de sang—ils ont suivi le destin de leurs descendants des premiers jours embryonnaires à l’âge adulte.
Localiser précisément l’origine des cellules réservées au fœtus
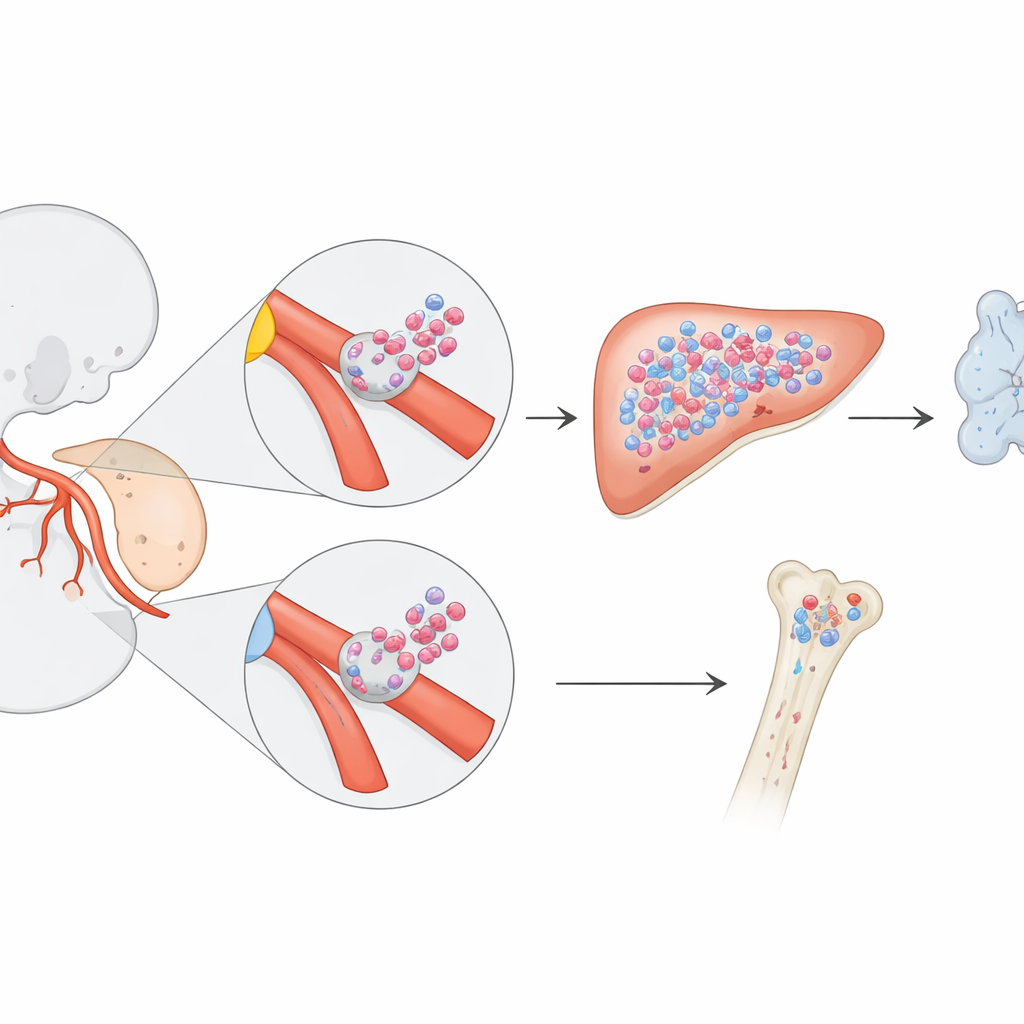
En modifiant précisément le moment d’activation du marqueur, l’équipe a pu marquer différentes vagues de cellules sanguines émergentes. Lorsqu’ils ont étiqueté l’endothélium hémogénique au jour embryonnaire 8,5, ils ont observé un schéma frappant : de nombreuses cellules sanguines et immunitaires du fœtus en fin de gestation portaient le marqueur, mais beaucoup moins après la naissance. Des images détaillées ont montré que ces progéniteurs marqués apparaissaient d’abord comme des grappes de cellules bourgeonnant depuis les parois de deux vaisseaux clés—les artères vitelline et ombilicale, qui relient l’embryon et le sac vitellin au placenta. Ces grappes se formaient plus tôt que les classiques cellules souches à long terme de l’aorte dorsale et représentaient une source de cellules hématopoïétiques jusqu’alors méconnue.
Approvisionner le système immunitaire fœtal, puis s’effacer
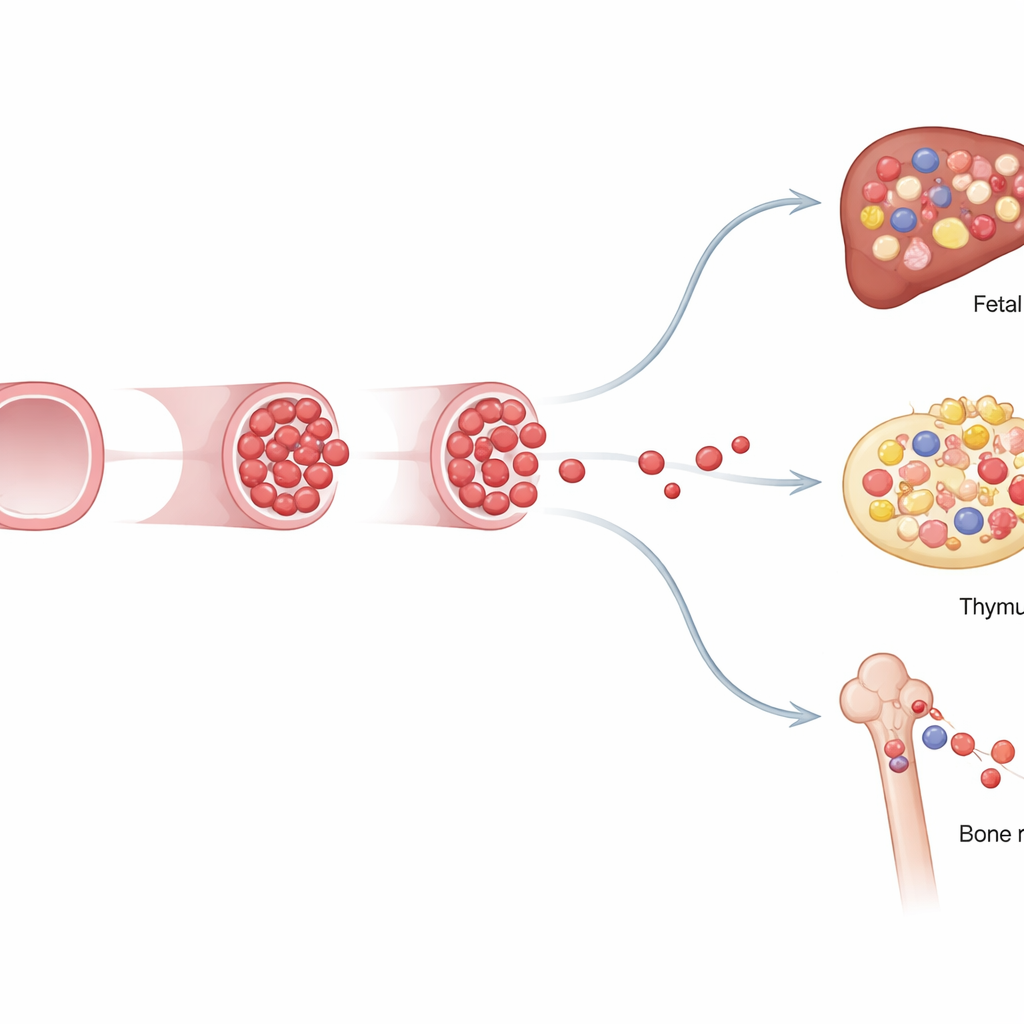
Les chercheurs se sont ensuite demandé ce que faisaient réellement ces progéniteurs à restriction fœtale. En utilisant la cytométrie en flux pour examiner le sang et les organes, ils ont constaté que les cellules marquées au jour 8,5 contribuaient à la majorité des cellules B fœtales, à de nombreux lymphocytes T, et à une large portion des cellules myéloïdes fœtales—des globules blancs qui combattent l’infection et aident à construire les tissus. Pourtant après la naissance, leur contribution a progressivement décliné à mesure qu’une autre vague de cellules hématopoïétiques, les cellules souches de type adulte classiques marquées à un stade ultérieur, prenait le relais. Ce « passage de témoin » révèle un système en couches : un premier programme optimisé pour une croissance fœtale rapide et l’ensemencement immunitaire, suivi d’un programme adulte durable conçu pour l’entretien à vie.
Identités distinctes et durée de vie limitée
Pour explorer en quoi ces cellules à restriction fœtale diffèrent des cellules souches adultes, l’équipe les a transplantées dans des souris irradiées et a analysé leur activité génétique cellule par cellule. Les transplantations ont montré que ces progéniteurs pouvaient brièvement reconstruire plusieurs lignées sanguines et immunitaires chez des receveurs, mais leur contribution diminuait lors de transplantations secondaires, indiquant une faible auto‑renouvellement à long terme. Le séquençage ARN unicellulaire a révélé que ces cellules présentent une identité mixte : certaines ressemblent davantage à des précurseurs immatures de type souche, tandis que d’autres sont déjà orientées vers des lignées immunitaires spécifiques, en particulier les lymphocytes. Leur activité génique et leurs schémas d’utilisation énergétique différaient également selon qu’elles provenaient de vaisseaux intra‑embryonnaires ou d’artères extra‑embryonnaires près du sac vitellin, soulignant que la localisation influence leur destinée.
Pourquoi cette vague sanguine précoce est importante
Cette étude montre qu’une vague puissante mais de courte durée de progéniteurs hématopoïétiques émerge de cellules spécialisées tapissant les vaisseaux des artères vitelline et ombilicale avant l’apparition des cellules souches classiques. Ces progéniteurs à restriction fœtale construisent une grande partie du sang et du système immunitaire du fœtus, puis cèdent progressivement la place aux cellules souches de type adulte qui résident dans la moelle osseuse. Pour le lecteur non spécialiste, l’idée clé est que notre système sanguin n’est pas construit par une cellule souche unique et intemporelle, mais par des générations successives d’artisans ayant des rôles et des durées de vie différents. Reconnaître cette vague fœtale précoce affine notre compréhension de la façon dont la diversité sanguine et immunitaire se forme et peut aider à expliquer pourquoi certains troubles sanguins infantiles et leucémies trouvent leur origine dans des événements survenus bien avant la naissance.
Citation: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Mots-clés: hématopoïèse embryonnaire, cellules souches sanguines fœtales, artères vitellines et ombilicales, endothélium hémogénique, développement immunitaire fœtal