Clear Sky Science · it
I progenitori ematopoietici limitati al periodo fetale derivano dall'endotelio emogenico nelle arterie vitelline e ombelicali
Come la prima formazione del sangue plasma una vita intera
Prima di nascere, il nostro organismo deve rapidamente costruire un sistema ematico e immunitario funzionante per mantenere in vita il feto in crescita. Questo articolo esplora una generazione recentemente scoperta di cellule ematopoietiche nei embrioni di topo che lavorano intensamente durante la vita fetale ma scompaiono in gran parte dopo la nascita. Capire come e dove sorgono queste cellule a breve durata aiuta a spiegare perché il sangue e il sistema immunitario dei bambini differiscono da quelli degli adulti e può fare luce su malattie che hanno origine prima della nascita.
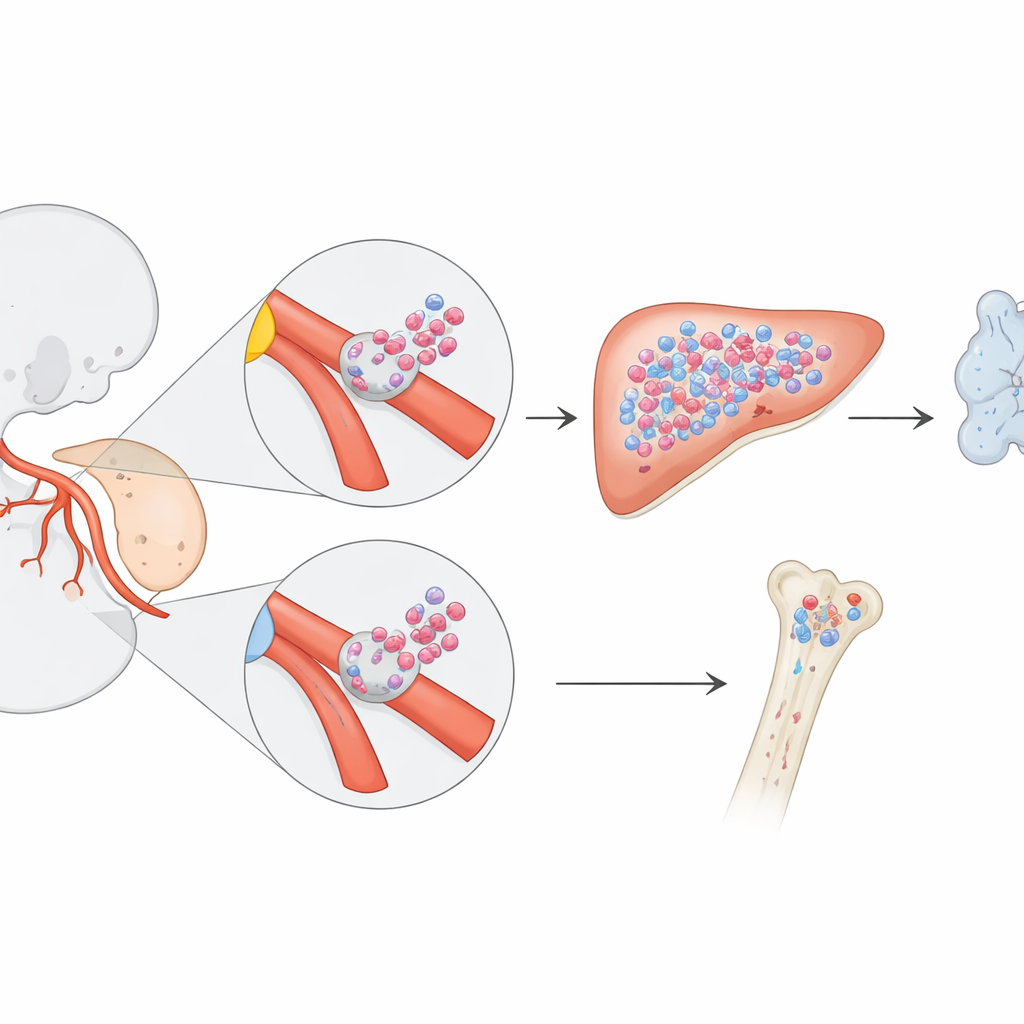
Una generazione nascosta di cellule costruttrici del sangue
Le cellule del sangue vengono prodotte in ondate durante lo sviluppo embrionale. Studi precedenti hanno mostrato che cellule staminali a lunga durata, che sostengono la produzione di sangue per tutta la vita adulta, compaiono in una regione vicino all’aorta embrionale. Ma i ricercatori sospettavano potesse esistere anche una popolazione speciale di progenitori esclusivi del periodo fetale—cellule che costruiscono gran parte del sistema ematico e immunitario prima della nascita e poi si attenuano. Per seguire queste cellule elusive, gli autori hanno usato “timbri temporali” genetici nei topi. Attivando brevemente un marcatore in specifiche cellule endoteliali—le cellule che rivestono i vasi sanguigni e possono trasformarsi in cellule ematopoietiche—hanno seguito il destino dei loro discendenti dai primi giorni embrionali fino all’età adulta.
Individuare l’origine delle cellule esclusivamente fetali
Modificando con precisione il momento in cui attivavano il marcatore, il team ha potuto etichettare diverse ondate di cellule del sangue emergenti. Quando hanno marcato l’endotelio emogenico all’ottavo giorno embrionale (E8.5), hanno osservato un quadro sorprendente: molte cellule del sangue e del sistema immunitario nel feto a fine gestazione portavano il marchio, ma molte meno lo facevano dopo la nascita. Immagini dettagliate hanno mostrato che questi progenitori etichettati apparivano inizialmente come grappoli di cellule in fase di gemmazione dalle pareti di due vasi chiave—le arterie vitelline e ombelicali, che collegano l’embrione e il sacco vitellino alla placenta. Questi ammassi si formavano prima rispetto alle classiche cellule staminali a lungo termine nell’aorta dorsale e rappresentavano una fonte di cellule ematopoietiche finora non riconosciuta.
Alimentare il sistema immunitario fetale, poi ritirarsi
I ricercatori si sono poi chiesti cosa facessero concretamente questi progenitori limitati al fetale. Usando la citometria a flusso per esaminare sangue e organi, hanno scoperto che le cellule marcate a E8.5 contribuivano alla maggioranza dei linfociti B fetali, a molti linfociti T e a una larga porzione delle cellule mieloidi fetali—globuli bianchi che combattono le infezioni e aiutano a costruire i tessuti. Tuttavia, dopo la nascita, il loro contributo diminuiva costantemente mentre un’altra ondata di cellule ematopoietiche, le classiche cellule staminali di tipo adulto marcate in un momento successivo, prendeva il sopravvento. Questo “passaggio” ha rivelato un sistema stratificato: un primo programma ottimizzato per la rapida crescita fetale e il popolamento immunitario, seguito da un programma adulto durevole progettato per il mantenimento a vita.
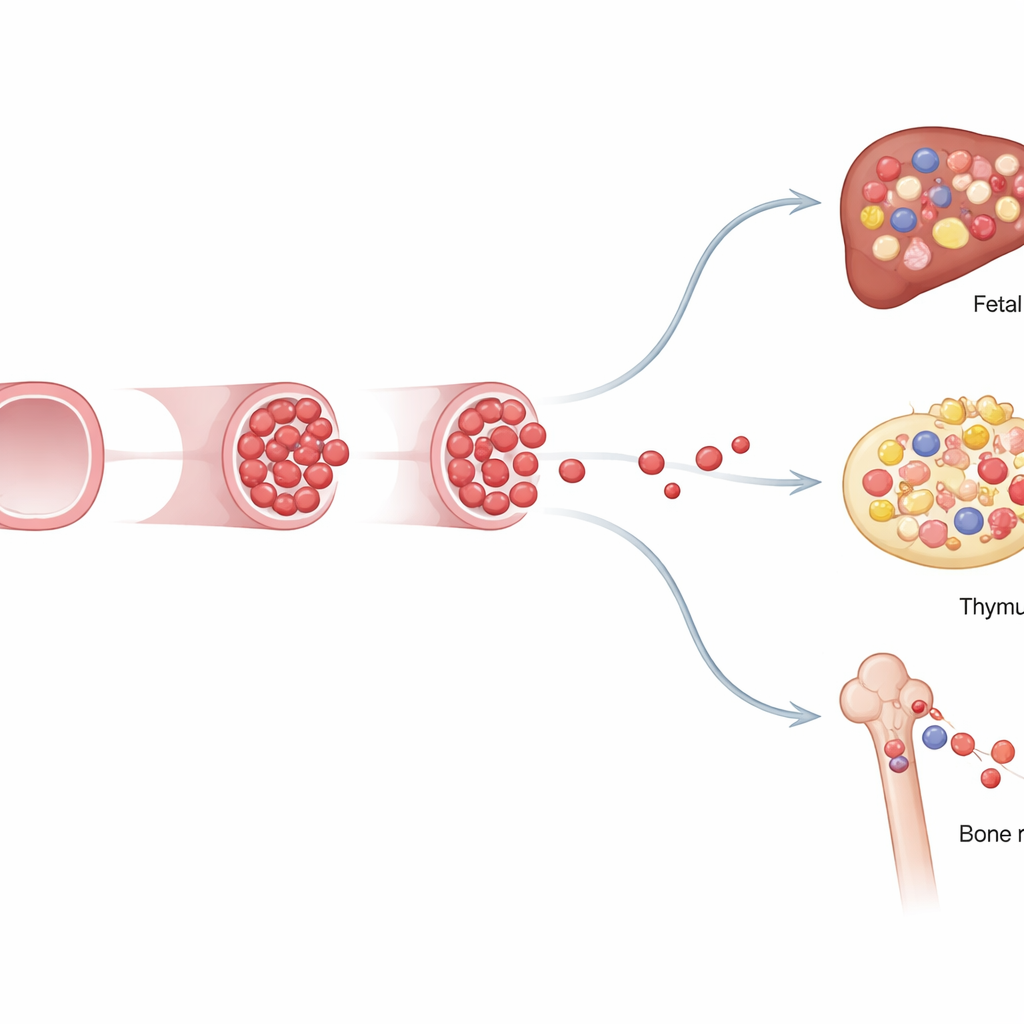
Identità distinte e limitata capacità di persistenza
Per indagare come questi progenitori fetali differiscano dalle cellule staminali adulte, il team li ha trapiantati in topi irradiati e ha analizzato l’attività genica a livello di singola cellula. I trapianti hanno mostrato che i progenitori limitati al fetale potevano ricostituire brevemente più lignaggi ematici e immunitari nei riceventi, ma il loro contributo si esauriva nei trapianti secondari, indicando scarsa auto-rinnovamento a lungo termine. Il sequenziamento dell’RNA a singola cellula ha rivelato che queste cellule presentano un’identità mista: alcune assomigliano più a precursori immaturi di tipo staminale, mentre altre sono già predisposte a diventare specifiche cellule immunitarie, in particolare linfociti. Anche i loro profili di espressione genica e i modelli di utilizzo energetico differivano a seconda che provenissero da vasi intra-embrionali o da arterie extra-embrionali vicino al sacco vitellino, sottolineando come la posizione plasmi il loro destino.
Perché questa ondata ematica precoce è importante
Questo studio mostra che un’ondata potente ma di breve durata di progenitori ematopoietici emerge da cellule specializzate che rivestono i vasi nelle arterie vitelline e ombelicali prima della comparsa delle classiche cellule staminali. Questi progenitori limitati al fetale costruiscono gran parte del sangue e del sistema immunitario del feto, per poi gradualmente lasciar spazio alle cellule staminali di tipo adulto che risiedono nel midollo osseo. Per il lettore non specialistico, il messaggio chiave è che il nostro sistema ematico non è costruito da una singola cellula staminale eterna, ma da generazioni successive di costruttori con compiti e durate diversi. Riconoscere questa ondata fetale precoce affina la nostra comprensione di come sorgono la diversità ematica e immunitaria e potrebbe aiutare a spiegare perché alcuni disordini ematici e leucemie dell’infanzia risalgono a eventi che si verificano molto prima della nascita.
Citazione: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Parole chiave: ematopoiesi embrionale, cellule staminali del sangue fetale, arterie vitelline e ombelicali, endotelio emogenico, sviluppo del sistema immunitario fetale