Clear Sky Science · pl
Progenitory hematopoetyczne ograniczone do okresu płodowego powstają z hemogenicznego śródbłonka w tętnicach żółtkowej i pępowinowej
Jak wczesna formacja krwi kształtuje całe życie
Zanim się urodzimy, nasze ciało musi szybko zbudować działający układ krwiotwórczy i odpornościowy, aby utrzymać przy życiu rozwijający się płód. W artykule opisano odkrytą niedawno „wczesną generację” komórek tworzących krew u embrionów myszy, które intensywnie działają w czasie życia płodowego, lecz w dużej części znikają po narodzinach. Zrozumienie, jak i gdzie powstają te krótkotrwałe komórki, pomaga wyjaśnić, dlaczego krew i układ odpornościowy dzieci różnią się od tych u dorosłych, oraz może rzucić światło na choroby rozpoczynające się przed narodzinami.
Ukryta generacja komórek budujących krew
Komórki krwi powstają falami w miarę rozwoju embrionu. Wcześniejsze badania wykazały, że długowieczne komórki macierzyste, które podtrzymują wytwarzanie krwi przez całe życie dorosłe, pojawiają się w rejonie pobliskim aorcie embrionalnej. Jednak badacze podejrzewali, że mogą istnieć również szczególne progenitory występujące tylko w okresie płodowym — komórki, które budują większość układu krwi i odporności przed narodzinami, a następnie zanikają. Aby śledzić te trudne do uchwycenia komórki, autorzy użyli genetycznych „znaczników czasowych” u myszy. Poprzez krótkie włączenie markera w określonych komórkach śródbłonka — komórkach wyściełających naczynia krwionośne, które mogą przekształcać się w komórki krwiotwórcze — śledzili los ich potomków od wczesnych dni embrionalnych aż do dorosłości.
Wskazanie miejsca pochodzenia komórek ograniczonych do okresu płodowego
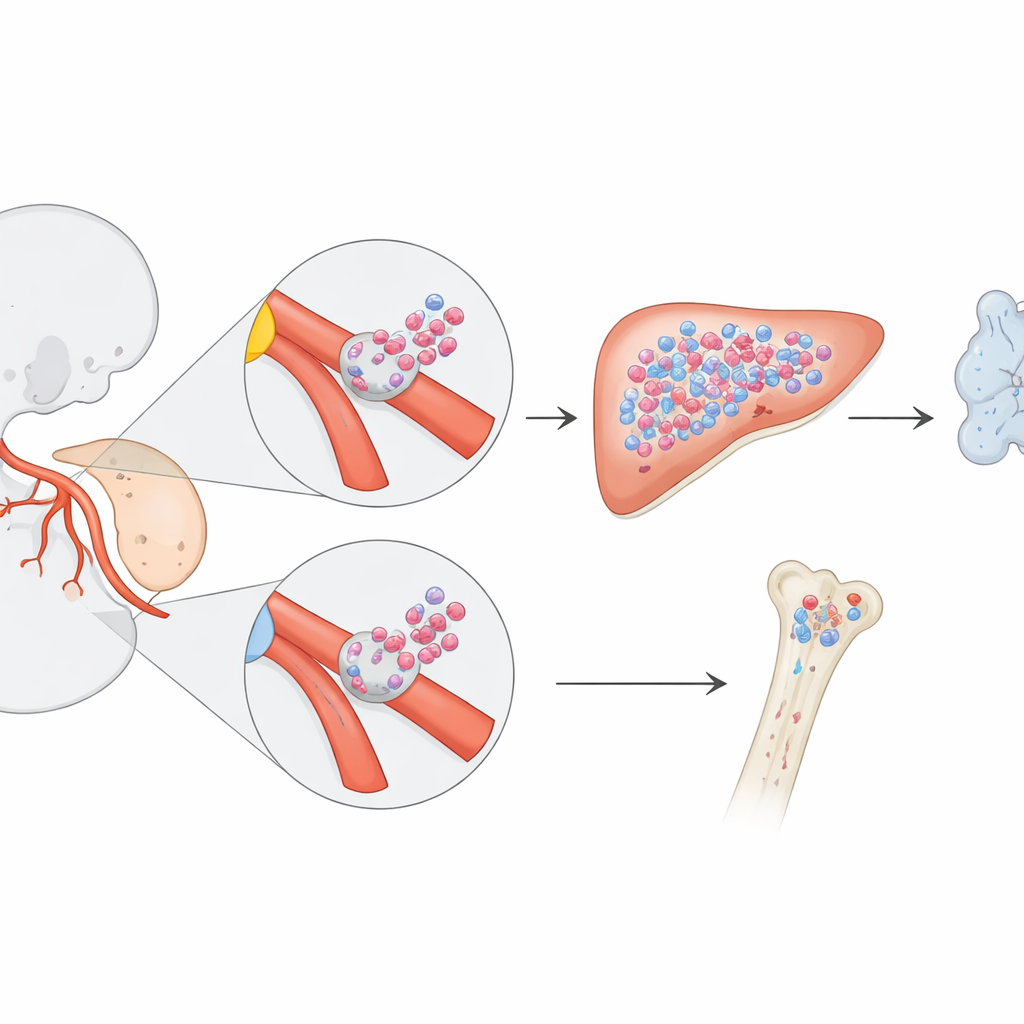
Zmieniając dokładnie moment aktywacji markera, zespół mógł znakować różne fale pojawiających się komórek krwi. Gdy oznakowali hemogeniczny śródbłonek w dniu embrionalnym 8,5, zaobserwowali uderzający wzorzec: wiele komórek krwi i układu odpornościowego u płodu w późnym stadium ciąży nosiło znacznik, lecz znacznie mniej takich komórek występowało po narodzinach. Dokładne obrazowanie wykazało, że oznakowane progenitory pojawiały się najpierw jako skupiska komórek wyrastających ze ścian dwóch kluczowych naczyń — tętnicy żółtkowej i pępowinowej, które łączą embrion i worek żółtkowy z łożyskiem. Te skupiska powstawały wcześniej niż klasyczne długoterminowe komórki macierzyste w aorcie grzbietowej i stanowiły wcześniej nierozpoznane źródło komórek krwiotwórczych.
Dostarczanie wsparcia układowi odpornościowemu płodu, a potem ustąpienie
Następnie badacze zapytali, co te progenitory ograniczone do okresu płodowego faktycznie robią. Analizując krew i narządy za pomocą cytometrii przepływowej, wykryli, że komórki oznakowane w dniu 8,5 stanowiły większość komórek B płodu, liczną część komórek T oraz dużą część mieloidalnych komórek płodu — białych krwinek walczących z infekcjami i uczestniczących w budowie tkanek. Jednak po narodzinach ich udział stopniowo malał, gdy inna fala komórek krwiotwórczych, klasyczne komórki macierzyste typu dorosłego oznaczone w późniejszym czasie, przejmowała funkcję. To „przekazanie pałeczki” ujawniło warstwowy system: wczesny program zoptymalizowany pod kątem szybkiego wzrostu płodu i zasiedlania odporności, po którym następuje trwały program dorosły zaprojektowany do utrzymania przez całe życie.
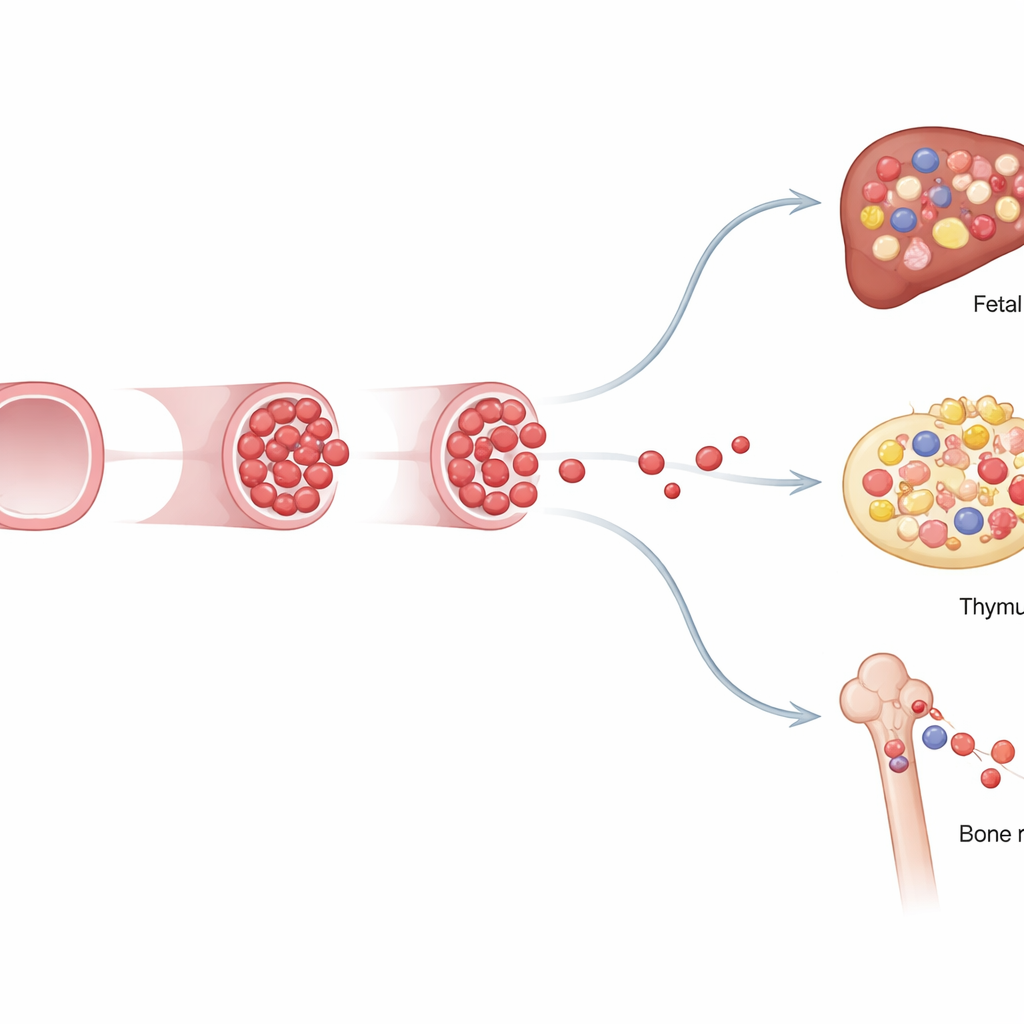
Odmienna tożsamość i ograniczona zdolność przetrwania
Aby zbadać, jak progenitory ograniczone do okresu płodowego różnią się od komórek macierzystych dorosłych, zespół przeszczepił je do napromieniowanych myszy i analizował aktywność genetyczną pojedynczych komórek. Przeszczepy wykazały, że progenitory płodowe potrafiły krótkotrwale odbudować wiele linii krwiotwórczych i odpornościowych u biorców, lecz ich wkład słabł w wtórnych przeszczepach, co wskazuje na niewielką zdolność długoterminowego samoodnawiania. Sekwencjonowanie RNA pojedynczych komórek ujawniło, że komórki te mają mieszany profil tożsamości: niektóre przypominają bardziej niedojrzałe, przypominające komórki macierzyste prekursorowe, podczas gdy inne są już ukierunkowane na zostanie określonymi komórkami odpornościowymi, szczególnie limfocytami. Ich aktywność genowa i wzorce wykorzystania energii również różniły się w zależności od tego, czy pochodziły z naczyń wewnątrzembrionalnych, czy z naczyń pozaziemnych w pobliżu worka żółtkowego, podkreślając, że lokalizacja kształtuje ich los.
Dlaczego ta wczesna fala krwi ma znaczenie
Badanie pokazuje, że krótko żyjąca, ale silna fala progenitorów krwiotwórczych powstaje z wyspecjalizowanych komórek wyściełających naczynia w tętnicach żółtkowej i pępowinowej przed pojawieniem się klasycznych komórek macierzystych. Te progenitory ograniczone do okresu płodowego budują dużą część układu krwi i odporności płodu, a następnie stopniowo ustępują miejsca komórkom typu dorosłego, które osiedlają się w szpiku kostnym. Dla czytelnika popularnonaukowego kluczowy wniosek jest taki, że nasz układ krwi nie jest budowany przez jedną, ponadczasową komórkę macierzystą, lecz przez kolejne generacje budowniczych o różnych zadaniach i długości życia. Uznanie istnienia tej wczesnej fali płodowej doprecyzowuje obraz powstawania różnorodności krwi i odporności oraz może pomóc wyjaśnić, dlaczego niektóre dziecięce zaburzenia krwi i białaczki mają swoje początki w zdarzeniach zachodzących na długo przed narodzinami.
Cytowanie: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Słowa kluczowe: embriogenna hematopoeza, płodowe komórki macierzyste krwi, tętnice żółtkowa i pępowinowa, hemogeniczny śródbłonek, płodowy rozwój układu odpornościowego