Clear Sky Science · de
Fetal eingeschränkte hämatopoetische Vorläufer entstehen aus hämogenem Endothel in Dottersack- und Nabelarterien
Wie frühe Blutbildung ein ganzes Leben prägt
Bevor wir geboren werden, muss unser Körper rasch ein funktionierendes Blut- und Immunsystem aufbauen, um den wachsenden Fetus am Leben zu erhalten. Dieser Artikel beleuchtet eine neu entdeckte „frühe Generation“ blutbildender Zellen in Mausembryonen, die während des Fetallebens intensiv arbeiten, nach der Geburt jedoch größtenteils verschwinden. Zu verstehen, wie und wo diese kurzlebigen Zellen entstehen, hilft zu erklären, warum sich Blut- und Immunsysteme von Kindern von denen Erwachsener unterscheiden, und kann Aufschluss über Krankheiten geben, die vor der Geburt beginnen.
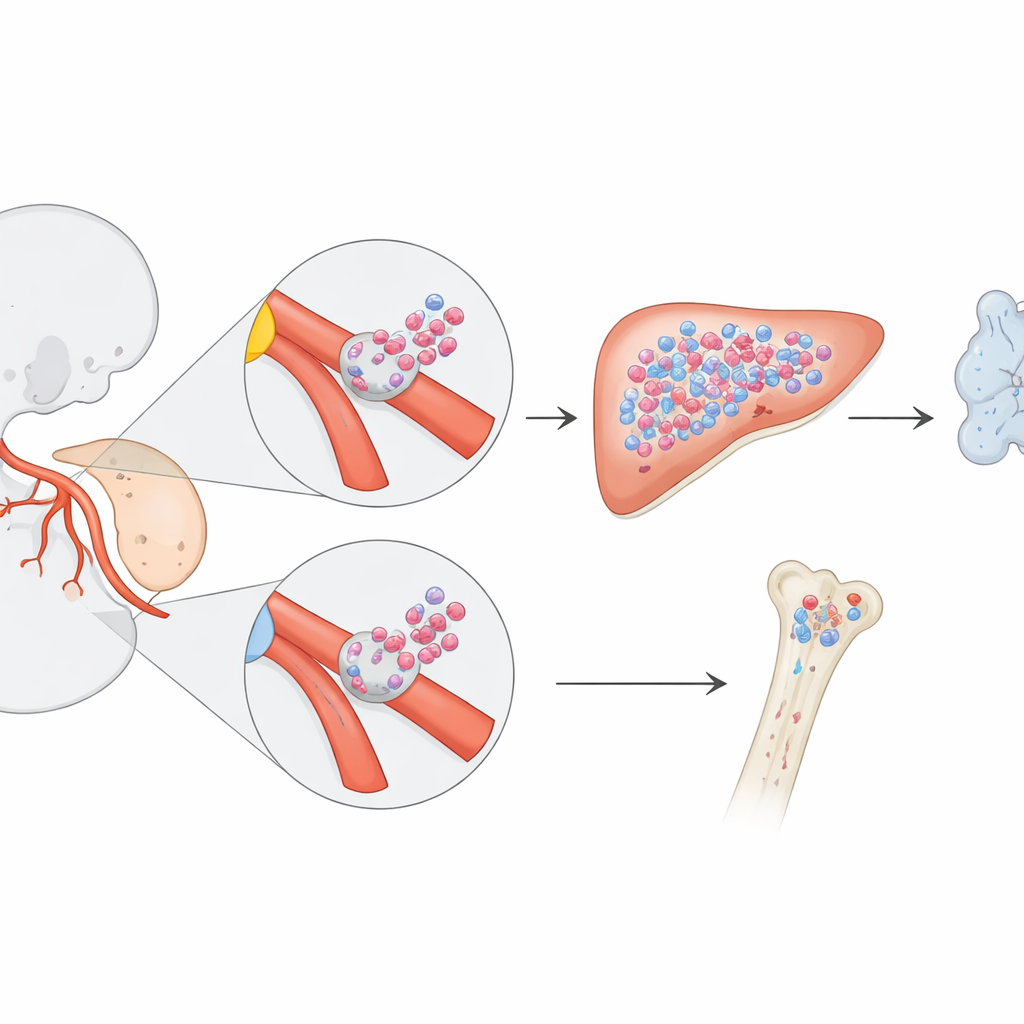
Eine verborgene Generation blutbildender Zellen
Blutzellen werden in Wellen gebildet, während sich ein Embryo entwickelt. Frühere Arbeiten zeigten, dass langlebige Stammzellen, die die Blutproduktion im erwachsenen Leben aufrechterhalten, in einer Region in der Nähe der embryonalen Aorta erscheinen. Forscher vermuteten jedoch, dass es auch spezielle, nur im Fetus vorkommende Vorläufer geben könnte — Zellen, die den Großteil des Bluts und Immunsystems vor der Geburt aufbauen und dann zurückgehen. Um diese schwer fassbaren Zellen zu verfolgen, nutzten die Autoren genetische „Zeitstempel“ bei Mäusen. Indem sie kurzzeitig einen Marker in bestimmten Endothelzellen einschalteten — den Zellen, die Blutgefäße auskleiden und sich in blutbildende Zellen verwandeln können — verfolgten sie das Schicksal ihrer Nachkommen von frühen Embryotagen bis ins Erwachsenenalter.
Feststellen, woher die nur fetalen Zellen stammen
Indem das Team genau veränderte, wann sie den Marker aktivierten, konnte es unterschiedliche Wellen entstehender Blutzellen markieren. Als sie das hämogene Endothel am Embryonaltag 8,5 markierten, zeigten sich ein deutliches Muster: Viele Blut- und Immunzellen im späten Fetus trugen das Etikett, nach der Geburt jedoch deutlich weniger. Detaillierte Bildgebung zeigte, dass diese markierten Vorläufer zuerst als Zellcluster sichtbar wurden, die aus den Wänden zweier wichtiger Gefäße absprossen — der Dottersack- und der Nabelarterie, die Embryo und Dottersack mit der Plazenta verbinden. Diese Cluster bildeten sich früher als die klassischen langzeitigen Stammzellen in der dorsalen Aorta und stellten eine zuvor unbekannte Quelle blutbildender Zellen dar.
Die fetale Immunversorgung übernehmen — und dann aussteigen
Die Forscher fragten als Nächstes, was diese fetal eingeschränkten Vorläufer tatsächlich leisten. Mit Durchflusszytometrie zur Untersuchung von Blut und Organen fanden sie, dass die am Tag 8,5 markierten Zellen den Großteil der fetalen B-Zellen, viele T-Zellen und einen großen Anteil der fetalen myeloiden Zellen beitrugen — weiße Blutkörperchen, die Infektionen bekämpfen und beim Gewebeaufbau helfen. Nach der Geburt nahm ihr Beitrag jedoch stetig ab, während eine andere Welle blutbildender Zellen, die klassischen adulten Stammzellen, die zu einem späteren Zeitpunkt markiert wurden, die Kontrolle übernahm. Diese „Übergabe“ offenbarte ein geschichtetes System: ein frühes Programm, optimiert für rasches fetales Wachstum und die Besiedlung des Immunsystems, gefolgt von einem dauerhaften Erwachsenenprogramm, das auf lebenslange Erhaltung ausgelegt ist.
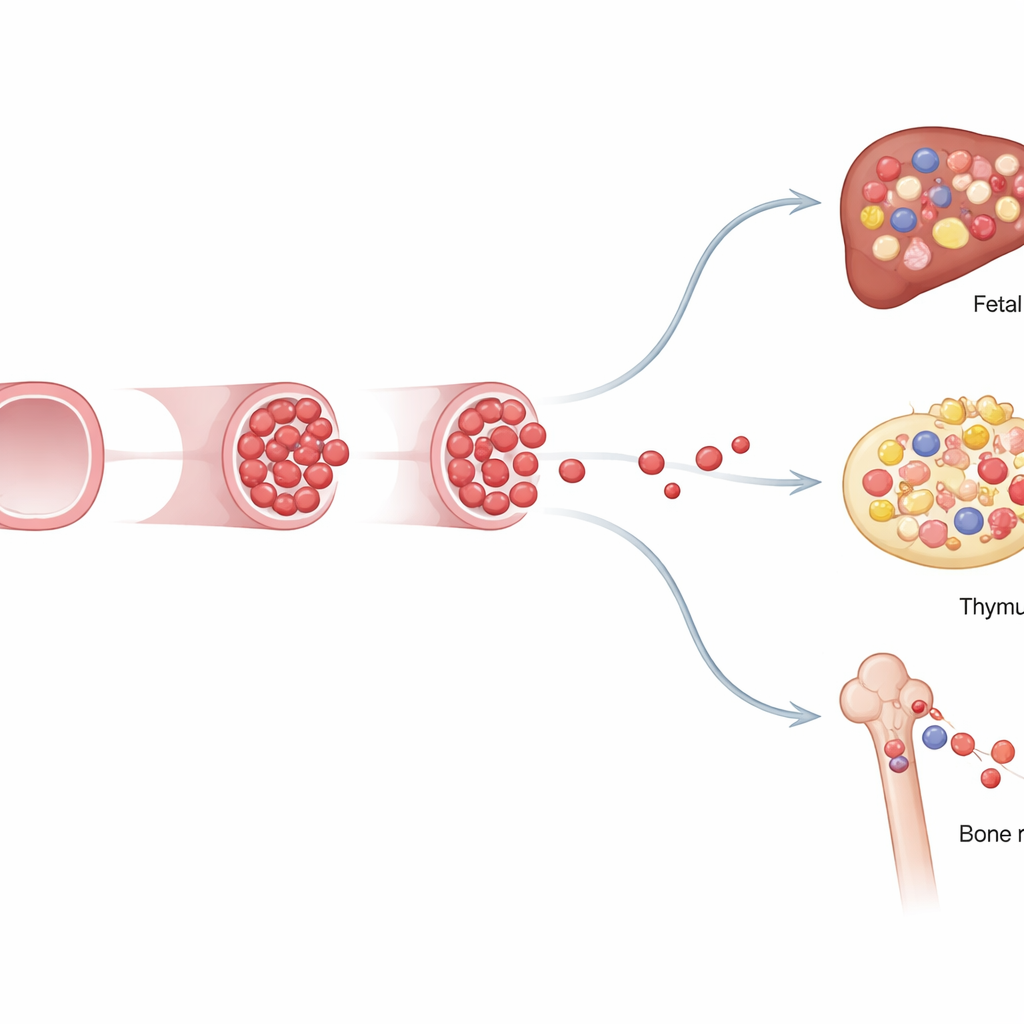
Unterschiedliche Identitäten und begrenzte Bleibedauer
Um zu untersuchen, wie sich diese fetal eingeschränkten Zellen von adulten Stammzellen unterscheiden, transplantierte das Team sie in bestrahlte Mäuse und analysierte ihre genetische Aktivität auf Einzelzellniveau. Transplantationen zeigten, dass die fetal eingeschränkten Vorläufer kurzzeitig mehrere Blut- und Immunlinien bei den Empfängern rekonstruieren konnten, ihr Beitrag jedoch bei Sekundärtransplantationen nachließ, was auf nur geringe langfristige Selbst-Erneuerung hindeutet. Einzelzell-RNA-Sequenzierung ergab, dass diese Zellen eine gemischte Identität tragen: Einige ähneln mehr unreifen, stammzellähnlichen Vorläufern, andere sind bereits darauf programmiert, bestimmte Immunzellen zu werden, besonders Lymphozyten. Ihre Genaktivität und Energieverbrauchsmuster unterschieden sich ebenfalls je nachdem, ob sie aus intraembryonalen Gefäßen oder extraembryonalen Arterien in der Nähe des Dottersacks stammten, was unterstreicht, dass der Ort ihr Schicksal beeinflusst.
Warum diese frühe Blutwelle wichtig ist
Die Studie zeigt, dass eine kurzlebige, aber leistungsstarke Welle blutbildender Vorläufer aus spezialisierten Gefäßauskleidungszellen in den Dottersack- und Nabelarterien entsteht, bevor die klassischen Stammzellen erscheinen. Diese fetal eingeschränkten Vorläufer bauen einen Großteil des Bluts und Immunsystems des Fetus auf und weichen dann allmählich adulten Stammzellen, die im Knochenmark residieren. Für den allgemeinen Leser ist die wichtigste Erkenntnis, dass unser Blutsystem nicht von einer einzigen, zeitlosen Stammzelle aufgebaut wird, sondern von aufeinanderfolgenden Generationen von Bautrupps mit unterschiedlichen Aufgaben und Lebensdauern. Die Anerkennung dieser frühen fetalen Welle verfeinert unser Bild davon, wie Blut- und Immunvielfalt entstehen, und könnte helfen zu erklären, warum einige kindliche Bluterkrankungen und Leukämien auf Ereignisse zurückzuführen sind, die weit vor der Geburt stattfinden.
Zitation: Barone, C., Quattrini, G., Muratore, A. et al. Fetal-restricted hematopoietic progenitors arise from hemogenic endothelium in vitelline and umbilical arteries. Nat Cardiovasc Res 5, 308–327 (2026). https://doi.org/10.1038/s44161-026-00793-8
Schlüsselwörter: embryonale Hämatopoese, fetale Blutstammzellen, Dottersack- und Nabelarterien, hämogenes Endothel, fetale Immunentwicklung