Clear Sky Science · zh
将 synechan 生物合成与调控途径转移至 Synechococcus elongatus PCC 7942 以实现硫酸化多糖的生产
把阳光变成有用的糖
硫酸化多糖是带有硫酸基的长链糖类分子,因其特殊性质而备受关注:它们能大量保水、形成凝胶,并以特定方式与细胞相互作用,这些特性使其在药物和化妆品中很有用。目前,许多此类化合物来自猪、鲨鱼等动物或海藻,带来成本、可持续性与伦理方面的问题。本研究探索是否可以将简单的光合微生物——蓝细菌——改造为直接从阳光和二氧化碳合成这些有价值分子,指向更可持续的高价值原料生产途径,可用于医疗和工业领域。
为什么这些特殊糖很重要
硫酸化多糖在日常生活中扮演着低调但重要的角色。像肝素这样的变体有助于防止血栓,相关分子也因其舒缓和保水功能被添加到护肤霜和眼药水中。不过在工业上,它们仍多从家畜和海洋生物中获取,使供应依赖于畜牧和渔业。化学方法在工厂中将硫酸基连接到糖分子上是可行的,但成本高昂,主要因为活化的硫酸供体分子价格昂贵。若有一种活细胞能在自身内组装糖链并完成硫酸化修饰,并以阳光为能源,这将提供一种更清洁、更便宜的替代方案。
将蓝细菌作为微小的糖工厂
蓝细菌是以阳光为能量的微小生物,常被称为“蓝绿藻”。许多物种天然围绕自身形成复杂的粘性糖质包膜,这些包膜可包括硫酸化多糖。研究者此前在一种模型蓝细菌 Synechocystis sp. PCC 6803 中发现了一种新的硫酸化胞外多糖,命名为 synechan。他们绘制出构建 synechan 并调控其产生的大型基因群——称为 xss 簇。在新研究中,他们询问是否能将这一完整的遗传程序转移到另一种被广泛研究但通常不产生硫酸化多糖的蓝细菌 Synechococcus elongatus PCC 7942 中。如果可行,这将作为一种概念验证,表明此类途径可以像模块化工具包一样在微生物间移动。 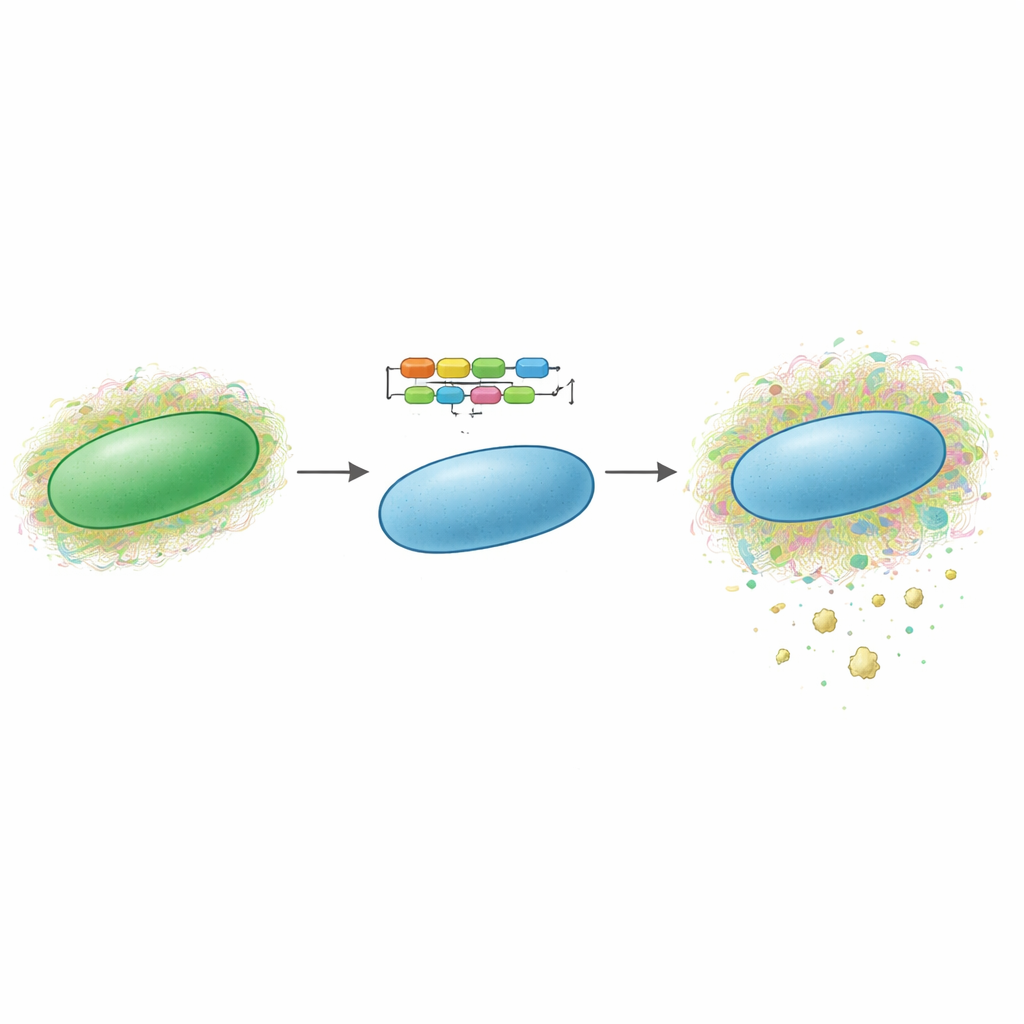
借来并装入复杂的代谢途径
为实现这一目标,团队将 synechan 系统分为两部分:构建并分泌糖聚合物的基因,以及作为这些构建者开关的调控基因。他们将生物合成基因插入到一枚穿梭质粒上,并将一个关键基因置于强可诱导启动子的控制下,以便通过添加化学信号(IPTG)触发产物合成。随后他们将调控基因整合到宿主染色体的中性位点中,同样置于可诱导控制下。当他们开启该系统时,工程菌株的生长明显变慢,细胞开始聚集。电子显微镜显示细胞表面被长纤维状物质覆盖。选择性染色专门标记硫酸化多糖,结果在细胞外出现明显的蓝色聚集体,化学检测也确认无论是细胞结合的还是释放到外部的胞外糖含量都比对照菌株增加。
新糖在内外的样貌
研究者接着检验新产生的物质是否确实类似 synechan。通过分解聚合物并分析其构件,他们发现工程细胞产生了一种由葡萄糖、半乳糖和甘露糖组成的硫酸化多糖,其硫酸化含量与天然 synechan 相近,但糖类比例不同。与主要释放到周围液体中的 synechan 不同,新聚合物大部分仍与细胞表面相关联。这表明虽然后转移的基因组能发挥作用,但并未完全重现原始结构;宿主自身的代谢与运输系统塑造出一种“像 synechan 的”产物。全基因组 RNA 测序显示开启 xss 基因组后细胞行为发生了全局改写:压力相关因子上升,光合与营养摄取基因下降,以及糖与硫代谢通路的调整,这些变化均与细胞将资源转向制造这种高能消耗的胞外包膜一致。 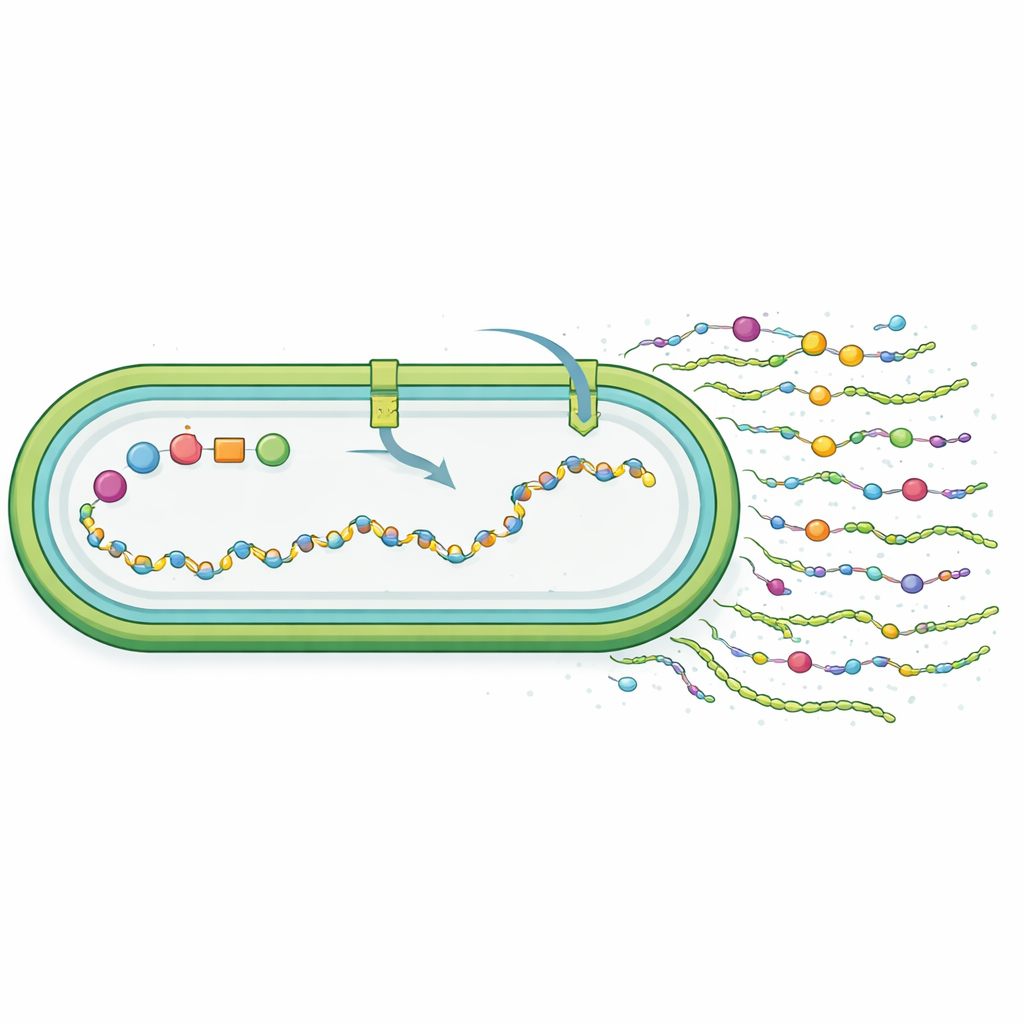
迈向绿色分子设计
从非专业角度看,核心信息是科学家们成功将一套大型、膜结合的生物合成机器从一种微生物移植到另一种,并使受体产生了一种新型的硫酸化糖质包膜。该产物并非原有聚合物的精确拷贝,但这种差异反而具有前景价值:它表明可以通过改变宿主细胞和遗传设计来调节这些分子的细节。长期来看,这种方法有望催生“太阳能驱动”的微生物工厂,将二氧化碳、光和简单营养物转化为一系列可定制的硫酸化多糖,具有特定质地和生物活性,从而减少对动物来源的依赖,并为可持续的医药、化妆品和功能性食品开辟新途径。
引用: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
关键词: 硫酸化多糖, 蓝细菌工程, 胞外多糖, 光合生物制造, 合成生物学