Clear Sky Science · de
Übertragung des synechan-Biosynthese- und Regulationswegs ermöglicht die Produktion sulfatisierter Polysaccharide in Synechococcus elongatus PCC 7942
Wie Sonnenlicht in nützliche Zucker verwandelt wird
Sulfatisierte Polysaccharide sind lange, zuckerbasierte Moleküle mit angehängten Sulfatgruppen, die ihnen bemerkenswerte Eigenschaften verleihen: sie können viel Wasser binden, Gele bilden und mit unseren Zellen auf Weisen interagieren, die sie in Medizin und Kosmetik nützlich machen. Heute stammen viele dieser Verbindungen von Tieren wie Schweinen und Haien oder von Meeresalgen, was Kosten-, Nachhaltigkeits- und Ethikfragen aufwirft. In dieser Studie wird untersucht, ob einfache photosynthetische Mikroben – Cyanobakterien – so umprogrammiert werden können, dass sie diese wertvollen Moleküle direkt aus Sonnenlicht und Kohlendioxid herstellen, und damit auf nachhaltigere Methoden zur Produktion hochwertiger Inhaltsstoffe für Gesundheit und Industrie hinweisen.
Warum besondere Zucker wichtig sind
Sulfatisierte Polysaccharide spielen bereits leise, aber wichtige Rollen im Alltag. Varianten wie Heparin helfen, Blutgerinnsel zu verhindern, und verwandte Moleküle werden Hautcremes und Augentropfen zur Beruhigung und Wasserbindung zugesetzt. Industriell werden sie jedoch meist noch aus Nutztieren und Meeresorganismen gewonnen, wodurch ihre Versorgung an Tierhaltung und Fang gebunden ist. Sulfatgruppen chemisch an Zucker anzuhängen ist zwar im Labor möglich, aber teuer, hauptsächlich weil das aktivierte Sulfatdonormolekül kostspielig ist. Eine lebende Zelle, die sowohl die Zuckerketten als auch die Sulfatdekorationen selbst montieren kann und dabei Sonnenlicht als Energiequelle nutzt, könnte eine sauberere, günstigere Alternative bieten.
Cyanobakterien als winzige Zuckerfabriken
Cyanobakterien sind mikroskopische, sonnengetriebene Organismen, oft „Blaualgen“ genannt. Viele Arten umgeben sich natürlich mit komplexen, schleimigen Zuckerschichten, die sulfatisierte Polysaccharide enthalten können. Die Autoren entdeckten zuvor ein neues sulfatisiertes Exopolysaccharid, genannt synechan, das von einem Modellcyanobakterium, Synechocystis sp. PCC 6803, produziert wird. Sie kartierten den großen Genkomplex – genannt xss‑Cluster – der synechan aufbaut und dessen Produktion steuert. In der neuen Studie fragten sie, ob dieses gesamte genetische Programm in ein anderes, gut untersuchtes Cyanobakterium, Synechococcus elongatus PCC 7942, übertragen werden kann, das normalerweise keine sulfatisierten Polysaccharide bildet. Wenn ja, wäre das ein Proof of Concept dafür, dass solche Wege wie modulare Werkzeugsätze zwischen Mikroben verschoben werden können. 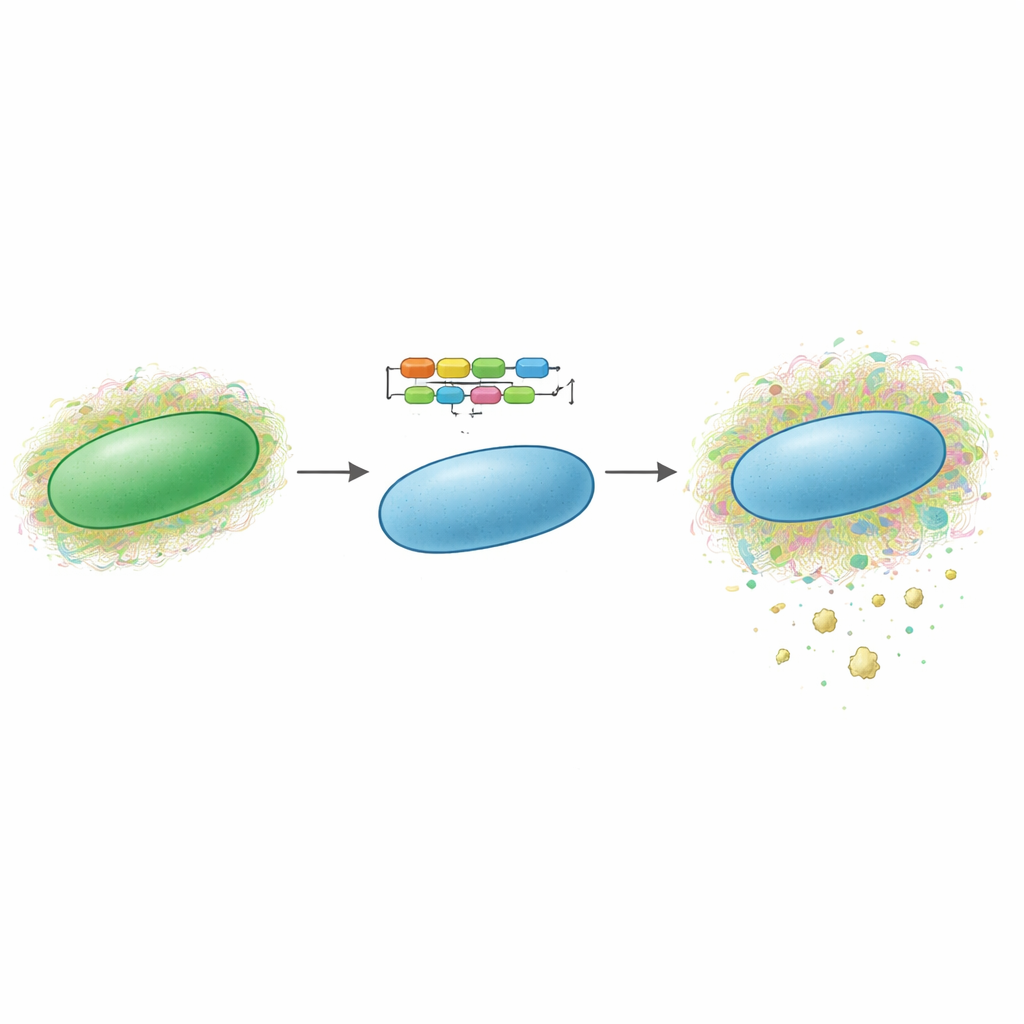
Ein komplexen Weg ausleihen und installieren
Um dies zu erreichen, teilte das Team das synechan‑System in zwei Hauptteile: die Gene, die das Zuckerpolymer aufbauen und sekretieren, und die Gene, die als An‑/Aus‑Schalter für diese Baumeister fungieren. Sie setzten die Biosynthesegene in ein Shuttle‑Plasmid ein und stellten ein Schlüsselgen unter die Kontrolle eines starken, induzierbaren Promotors, sodass ein zugefügtes chemisches Signal (IPTG) die Produktion auslösen würde. Die Regulatorgene integrierten sie in eine neutrale Stelle des Wirtschromosoms, ebenfalls unter induzierbarer Kontrolle. Sobald das System eingeschaltet wurde, verlangsamte sich das Wachstum des gentechnisch veränderten Stamms deutlich und die Zellen begannen zu verklumpen. Elektronenmikroskopie zeigte langfaseriges Material, das die Zelloberflächen überzog. Spezielle Färbungen, die sulfatisierte Polysaccharide gezielt sichtbar machen, zeigten klare blaue Aggregate außerhalb der Zellen, und chemische Tests bestätigten, dass sowohl zellgebundene als auch freigesetzte extrazelluläre Zucker im Vergleich zu Kontrollstämmen zunahmen.
Wie der neue Zucker innen und außen aussieht
Die Forscher untersuchten anschließend, ob das neue Material wirklich synechan ähnelt. Durch den Abbau der Polymere und die Analyse ihrer Bausteine stellten sie fest, dass die gentechnisch veränderten Zellen ein sulfatisiertes Polysaccharid aus Glukose, Galaktose und Mannose produzierten, mit einem Sulfatgehalt ähnlich dem des nativen synechan, jedoch mit einem anderen Zuckeranteilsverhältnis. Anders als synechan, das größtenteils ins umgebende Flüssigkeitsmedium freigesetzt wird, blieb ein großer Teil des neuen Polymers an der Zelloberfläche gebunden. Das deutet darauf hin, dass obwohl der übertragene Genkomplex funktionierte, er die ursprüngliche Struktur nicht perfekt reproduzierte; stattdessen formten der Stoffwechsel und die Transportsysteme des Wirts ein „synechan‑ähnliches“ Produkt. Genomweite RNA‑Sequenzierung zeigte, dass das Einschalten der xss‑Gene das Zellverhalten global umkrempelte: Stressbezogene Faktoren stiegen, Photosynthese‑ und Nährstoffaufnahmegene fielen, und Wege für Zucker‑ und Schwefelverarbeitung wurden angepasst – alles konsistent mit einer Umleitung von Ressourcen zur Herstellung einer energetisch aufwendigen extrazellulären Hülle. 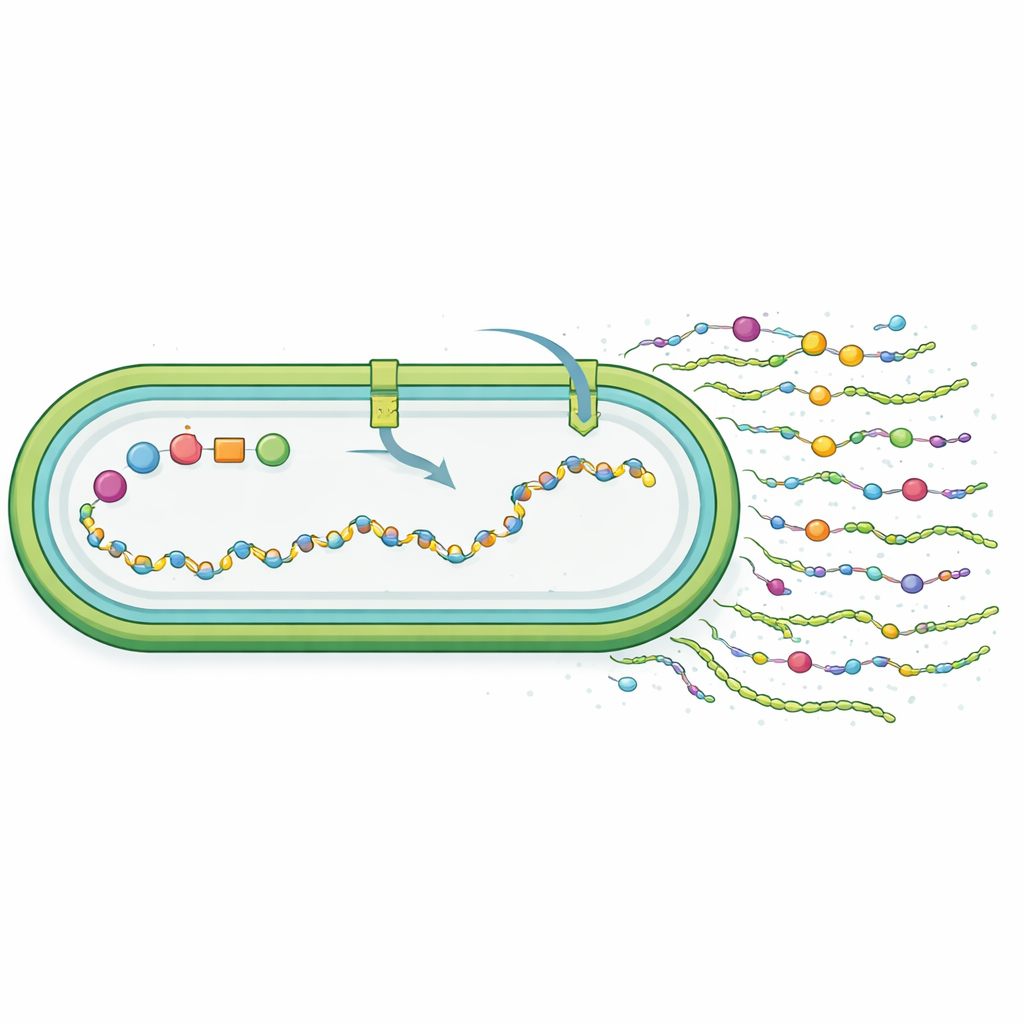
Auf dem Weg zu grünem Moleküldesign
Aus laienhafter Sicht ist die zentrale Botschaft, dass es den Wissenschaftlern gelungen ist, eine große, membrangebundenen biosynthetischen Maschine von einem Mikroben in einen anderen zu übertragen – und den Empfänger dazu zu bringen, eine neue Art sulfatischer Zuckerschicht zu produzieren. Das Produkt ist keine exakte Kopie des Originals, doch genau diese Abweichung ist vielversprechend: Sie zeigt, dass die feinen Details dieser Moleküle durch Änderung des Wirts und des genetischen Designs feinabgestimmt werden können. Langfristig könnte dieser Ansatz „solarbetriebene“ Mikrobenfabriken ermöglichen, die Kohlendioxid, Licht und einfache Nährstoffe in Bibliotheken maßgeschneiderter sulfatisierter Polysaccharide mit spezifischen Texturen und biologischen Aktivitäten verwandeln, die Abhängigkeit von tierischen Quellen reduzieren und neue Wege für nachhaltige Arzneimittel, Kosmetika und funktionelle Lebensmittel eröffnen.
Zitation: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Schlüsselwörter: sulfatisierte Polysaccharide, Ingenieurwesen von Cyanobakterien, Exopolysaccharide, photosynthetische Bioproduktion, synthetische Biologie